
����Ŀ�������ϩ��һ�ֻ���ԭ�ϣ�������ת����ϵ��

��֪��

�ش��������⣺
(1)A������(ϵͳ����)��_____��B��C�ķ�Ӧ������_________��
(2)B�Ľṹ��ʽ��____��D�ĺ˴Ź���������________��塣
(3)���������л�Ϊͬϵ�����________________(��������)��
(4)F����PHB�Ļ�ѧ����ʽ��___________________
(5)E��ͬ���칹���У����ܷ���������Ӧ��Ҳ����̼��������Һ��Ӧ�Ĺ���________��(�����������칹)��
(6)F���˺ϳ�PHB�⣬���ɾ���_________���������ۺ�������Ӧ�ϳ�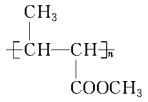 ��һ�������л����������ϣ����ڴ��������£���������Ӧ�Ļ�ѧ����ʽ��___________________��
��һ�������л����������ϣ����ڴ��������£���������Ӧ�Ļ�ѧ����ʽ��___________________��
���𰸡� 2������1,3������ϩ �ӳɷ�Ӧ(��ԭ��Ӧ) 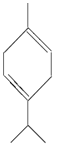 3 D�� E
3 D�� E 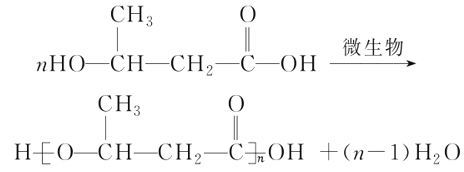 12 ��ȥ
12 ��ȥ 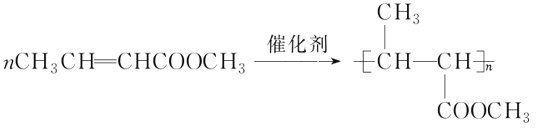
����������1��A�к���2��̼̼˫����1��ȡ������������˿�ʼ��ţ�����A������Ϊ2-��-1��3-����ϩ��A��3-��-1-��Ȳ�����ӳɷ�Ӧ����BΪ����ϩ������B�����������ӳɷ�Ӧ����C����2��������֪��Ϣ�ٿ�֪B�Ľṹ��ʽΪ![]() ��D�Ľṹ��ʽ��CH3-CO-CH2-COOH�������ڶԳƽṹ�����Է����к���3��Hԭ���ڣ���˴Ź���������3��壻��3��ͬϵ����ָ�ṹ���ƣ����������������ɸ�-CH2���л���Ļ��ƣ�D��E�ķ����ж������ʻ����Ȼ����ҷ���������2��-CH2����ͬϵ���ѡDE����4��D�е��ʻ������������ӳɷ�Ӧ����F�Ľṹ��ʽ��CH3-CHOH-CH2-COOH��F�������Ӽ�����۷�Ӧ����PHB��ˮ����ѧ����ʽ��
��D�Ľṹ��ʽ��CH3-CO-CH2-COOH�������ڶԳƽṹ�����Է����к���3��Hԭ���ڣ���˴Ź���������3��壻��3��ͬϵ����ָ�ṹ���ƣ����������������ɸ�-CH2���л���Ļ��ƣ�D��E�ķ����ж������ʻ����Ȼ����ҷ���������2��-CH2����ͬϵ���ѡDE����4��D�е��ʻ������������ӳɷ�Ӧ����F�Ľṹ��ʽ��CH3-CHOH-CH2-COOH��F�������Ӽ�����۷�Ӧ����PHB��ˮ����ѧ����ʽ��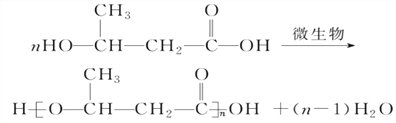 ����5��E��ͬ���칹���У����ܷ���������Ӧ��Ҳ����̼��������Һ��Ӧ������л����к���ȩ�����Ȼ�����ȩ����Ϊȡ������ȡ����������е������ϵ�Hԭ�ӣ������ͬ���칹����4�֣��ֱ��������ᡢ2-�����ᡢ3-�����ᡢ2��2-�������ᣬ�����е�Hԭ����������ȥ�Ȼ���Hԭ�ӣ��ֱ���4��4��3��1�����Թ���12�֣���6����������Ľṹ��ʽ�жϣ�F������ȥ��Ӧ����CH3-CH=CH-COOH������״�����������Ӧ��������������Ӿ۷�Ӧ���ɲ���ڴ��������£������Ӿ۷�Ӧ�Ļ�ѧ����ʽ��
����5��E��ͬ���칹���У����ܷ���������Ӧ��Ҳ����̼��������Һ��Ӧ������л����к���ȩ�����Ȼ�����ȩ����Ϊȡ������ȡ����������е������ϵ�Hԭ�ӣ������ͬ���칹����4�֣��ֱ��������ᡢ2-�����ᡢ3-�����ᡢ2��2-�������ᣬ�����е�Hԭ����������ȥ�Ȼ���Hԭ�ӣ��ֱ���4��4��3��1�����Թ���12�֣���6����������Ľṹ��ʽ�жϣ�F������ȥ��Ӧ����CH3-CH=CH-COOH������״�����������Ӧ��������������Ӿ۷�Ӧ���ɲ���ڴ��������£������Ӿ۷�Ӧ�Ļ�ѧ����ʽ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Na3N��3H2O��3NaOH��NH3������NaH��H2O��NaOH��H2��������������ȷ����
A. ���Ӱ뾶��Na+��N3-��H+
B. ��Ӧ����������������ԭ��Ӧ
C. ��Ӧ��ÿ����1 mol H2��ת�Ƶĵ�����ΪNA
D. Na3N��NaH�����ᷴӦ��ֻ����һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƶ���ȷ����
A. pH=6.5����Һһ��������
B. 0.1mol L-1��Na2CO3��Һ�У�c(CO32-)+c(HCO3-)=0.1mol L-1
C. �����£��������0.2 mol L-1��������0.2 mol L-1������������Һ��ϣ�������Һ��pH=13
D. �����£�ij��Һ��ˮ�������c(OH-)=l��10-12 mol L-1������ҺpH һ������2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������( )

A. �� ͼ��֪��a��Kw����ֵ��b��Kw����ֵ��
B. �ұ�ʾ����ͬ���ܱ������У���ͬ�¶��µķ�Ӧ���÷�Ӧ�Ħ�H<0
C. ����ʾ0.100 0 mol��L��1 NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L��1������Һ�ĵζ�����
D. ����ͼ������ȥCuSO4��Һ�е�Fe3�����ɼ���CuO����pH��3��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����ȡ����Ӧ���ǣ� ��
A.�Ҵ���ͭ����������������Ӧ
B.��ͪ��������Ӧ
C.���������������ƵĴ���Һ����
D.�ױ���������Ϲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ۺ�������������ĩ������ȼ����ֳ����ȷݣ�һ���ڸ�����ǡ�÷�Ӧ����������ϡ���ᷴӦ�� ��������aL����һ��ֱ�ӷ�����������������Һ�г�ַ�Ӧ����ͬ��������������bL����a��bΪ�� ��
A. 1��1 B. 3��4 C. 4��3 D. 8��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к���C��N��Mn��Ԫ�أ�ʵ���г��ù��������������ⶨ�������̵ĺ�������Ӧԭ��Ϊ2Mn2++5S2O82-+8H2O![]() 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
��1��Mnԭ�ӵļ۲���ӵĹ���Դ�ʽ�������Ų�ͼ��Ϊ______��
��2����֪H2S2O8�Ľṹ��ʽ��ͼ��ʾ��
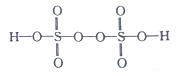
��H2S2O8��S�Ĺ���ӻ���ʽΪ______��H��O��S����Ԫ���У��縺������Ԫ����_________����Ԫ�ط��ţ���
��S��̬ԭ���е��ӵ��˶�״̬��_________�֡�
��������Ӧ��S2O82-���ѵĹ��ۼ�����Ϊ________������Ҽ����м���) ��ÿ����1molMnO4-,���ѵĹ��ۼ���ĿΪ_________NA��
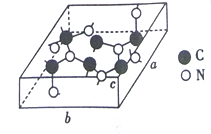
��3��C��N���γɶ��ֽṹ�ľ��塣һ�����͵ij�Ӳ���������ڽ��ʯ�Ľṹ����Ӳ�ȱȽ��ʯ���侧����ͼ��ʾ��ͼʾԭ�Ӷ������ھ����ڣ����仯ѧʽΪ________����֪��������a=0.64nm, b=0.55nm��c=0.24nm����þ�����ܶ�Ϊ________���г�ʽ�Ӽ��ɣ���ʽ���в�������ĸ��g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���巴Ӧ��ƽ�ⳣ���ɱ�ʾΪK=c(CH3OCH3)c(H2O)/c2(CH3OH)���÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ����400����K=32��500����K=44����ش��������⣺
��1��д��������Ӧ�Ļ�ѧ����ʽ��_________________________________ ��
��2���÷�Ӧ����H _________0��
��3����֪���ܱ������У����ijʱ�̸���ֵ�Ũ�����£�
���� | CH3OH(g�� | CH3OCH3(g�� | H2O(g�� |
Ũ��/��molL-1�� | 0.54 | 0.68 | 0.68 |
�ٴ�ʱ�¶�400�棬��ijʱ������_______���������������ͬ����
�������¶�Ϊ�����꣬�Ը��¶���ƽ��̬�״����ʵ���nΪ�����꣬��ʱ��Ӧ����ͼ���λ����ͼ��____�㣬�Ƚ�ͼ��B��D��������Ӧ������Ӧ������B_______��D��������____��

��4��һ��������Ҫ��߷�Ӧ���ת���ʣ����Բ��õĴ�ʩ��___________��
a�������¶� b��������� c��ѹ�����������
d������ˮ������Ũ�� e����ʱ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ؾ������ܺá����������ŵ㣬�䷴Ӧԭ����NiO(OH)+ MH==NiO+M + H2O��MH������Ϊ����Ͻ�M�����ս����ԭ�ӣ�����˵������ȷ����

A. MH�缫�Ǹ���
B. OH-��MH���ƶ�
C. �����缫��Ӧʽ��NiO(OH)+e-=NiO+OH-
D. ���Ӵ�MH�缫����NiO(OH)�缫����KOH��Һ����MH��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com