
【题目】如图为Zn-Cu原电池的示意图,请回答:

(1)锌片为原电池的_____极,铜片为原电池的____极(填“正”或“负”)
(2)锌电极反应式是_______,属于______反应(填“氧化”或“还原”);铜电极反应式是______,属于______反应(同上)。
(3)______(填“电子”或“电流”)从锌片通过导线流向铜片,溶液中H+在______(填“锌片”或“铜片”)获得电子。
(4)若锌片减轻0.1mol,则另一极放出气体的物质的量为_____mol。
【答案】负 正 Zn-2e-=Zn2+ 氧化 2H++2e-=H2↑ 还原 电子 铜片 0.1
【解析】
锌比铜活泼,为原电池的负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为原电池的正极,发生还原反应,电极反应式为2H++2e-=H2↑,电池总反应为Zn+2H+=Zn2++H2↑,结合原电池原理分析解答。
(1)锌比铜活泼,为原电池的负极,铜片为原电池的正极,故答案为:负;正;
(2)锌比铜活泼,为原电池的负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为原电池的正极,发生还原反应,电极反应式为2H++2e-=H2↑,故答案为:Zn-2e-=Zn2+;氧化;2H++2e-=H2↑;还原;
(3)锌比铜活泼,为原电池的负极,锌失去电子,电子从锌片通过导线流向铜片,铜做正极,溶液中氢离子在铜片上得到电子生成氢气,发生还原反应,故答案为:电子;铜片;
(4)根据Zn-2e-=Zn2+,n(Zn)=0.1mol,转移电子0.2mol,根据2H++2e-=H2↑,转移0.2mol电子,生成氢气0.1mol,故答案为:0.1。


科目:高中化学 来源: 题型:
【题目】氧化亚铜是一种附加值较高的铜类物质,下列流程是利用再生资源回收高品质氧化亚铜。某兴趣小组通过查阅资料得知CuCI可溶于![]() 浓度较大的体系,能被硝酸氧化,在碱性条件下易水解转化为
浓度较大的体系,能被硝酸氧化,在碱性条件下易水解转化为![]() ,
,![]() 在酸性条件下可歧化为
在酸性条件下可歧化为![]() 和Cu。据此设计了如下实验方案。下列说法正确是( )
和Cu。据此设计了如下实验方案。下列说法正确是( )

A.生成CuCl的离子方程式为![]()
B.为确保![]() 完全沉淀,应向含铜废液中加入过量的NaCl
完全沉淀,应向含铜废液中加入过量的NaCl
C.检验制得的![]() 中是否含有CuCl,可用硝酸银和硝酸
中是否含有CuCl,可用硝酸银和硝酸
D.可直接向含铜废液中加入葡萄糖,在碱性条件下制得![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如下:
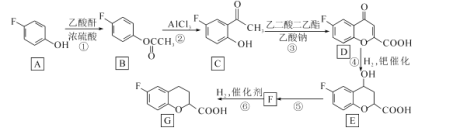
已知:乙酸酐的结构简式为![]() 。请回答下列问题:
。请回答下列问题:
(1)G中含氧官能团的名称是______________
(2)反应①的化学方程式为__________________
(3)反应⑤所需的试剂和条件是____,该反应类型是______________
(4)写出满足下列条件的C的同分异构体的结构简式________________________。
I.苯环上只有两种取代基;Ⅱ,核磁共振氢谱图中只有4组吸收峰;Ⅲ.能与NaHCO3溶液反应生成CO2。
(5)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。则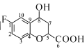 中的手性碳是____(填碳原子的数字标号)。
中的手性碳是____(填碳原子的数字标号)。
(6)设计以![]() 为原料制备
为原料制备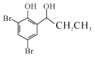 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。
_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分为Al2O3,还有少量杂质)中提取铝的工艺流程及步骤如下:
试回答下列问题。
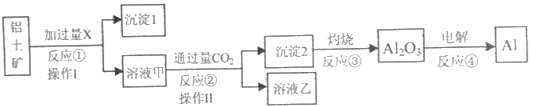
(1)试剂X为___;反应①的离子方程式为___。
(2)操作Ⅰ、操作Ⅱ均为___(填操作名称)。反应①②③④中属于氧化还原反应的是___(填数字序号)。
(3)反应②的离子方程式为___。
(4)金属铝与氧化铁的混合物在高温下会发生剧烈的反应,该反应的化学方程式为___。(5)电解熔融氧化铝制取金属铝,若有0.6mol电子发生转移,理论上能得到金属铝的质量是___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
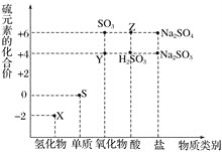
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______________(填化学式)。
(2)将X与Y混合,可生成淡黄色固体。该反应中氧化剂与还原剂的物质的量之比为_____________。
(3)检验物质Y的方法是______________________________。
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为____________。
(5)Na2S2O3是重要的化工原料,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是_____________(填字母)。
a.Na2S+S b.Na2SO3+S
c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24mL 0.05mol·L-1的Na2SO3溶液与 20mL 0.02mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为用石墨电极电解氯化铜溶液的装置:

(1)与电源正极相连的电极称为____ 极,电极反应式_______;
(2)与电源负极相连的电极称为____ 极,电极反应式_______;
(3)总反应:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。下列叙述正确的是( )
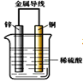
A. 该装置将化学能转变为电能
B. 电流从锌片流向铜片
C. 一段时间后,铜片质量减轻
D. 锌片发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将①50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:

(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2) 若将盐酸换成同浓度和同体积的醋酸,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用40 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上
述实验相比,所放出的热量_________(填“比①大”、 “比①小”或“相等”),理由是_____________________________________________;所求中和热的数值会________(填“相等”或“不相等”),理由是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[
CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[![]() ]和水碳比[
]和水碳比[![]() ]投料时二氧化碳转化率的情况。
]投料时二氧化碳转化率的情况。
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为____。
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由_____。
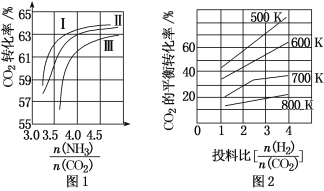
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
①该反应的化学平衡常数的表达式为_____。
②该反应的ΔS___0,ΔH___0(填“>”或“<”)。
③700K投料比[![]() ]=2时,H2的平衡转化率为_____。
]=2时,H2的平衡转化率为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com