
【题目】将一定质量的Na2CO3和NaHCO3的固体混合物充分加热至恒重,共收集到CO2为2.24L。充分冷却后,向残留的固体中逐滴加入稀盐酸至没有气体放出为止,恰好用去稀盐酸100mL,又收集到CO2为4.48L(假设气体的体积均在标准状况下测定;反应后溶液的体积仍为100mL)。试计算:
⑴原固体混合物中Na2CO3与NaHCO3的物质的量之比为_____________________
⑵反应后的溶液中溶质的物质的量浓度为______________________________
【答案】 1:2 4.00 mol/L
【解析】⑴.将一定质量的Na2CO3和NaHCO3的固体混合物充分加热至恒重,只有NaHCO3发生分解反应,方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O,此时收集到标准状况下CO22.24L,则CO2为2.24L÷22.4L/mol=0.1mol,根据方程式可知原固体混合物中含有0.2mol的NaHCO3,同时得到0.1mol的Na2CO3;
Na2CO3+CO2↑+H2O,此时收集到标准状况下CO22.24L,则CO2为2.24L÷22.4L/mol=0.1mol,根据方程式可知原固体混合物中含有0.2mol的NaHCO3,同时得到0.1mol的Na2CO3;
因残留的固体中只有Na2CO3,则加入盐酸后的反应方程式是:Na2CO3+2HCl=2NaCl+CO2↑+H2O,向残留的固体中逐滴加入稀盐酸至没有气体放出为止,又收集到标准状况下CO24.48L,即CO2为4.48L÷22.4L/mol=0.2mol,根据反应方程式可知Na2CO3的物质的量是0.2mol,同时生成NaCl0.4mol,因NaHCO3分解生成的Na2CO3是0.1mol,则原固体混合物中的Na2CO3是0.2mol-0.1mol=0.1mol,所以原固体混合物中Na2CO3与NaHCO3的物质的量之比为0.1mol:0.2mol=1:2,故答案是:1:2;
⑵.因残留固体与稀盐酸恰好完全反应,则反应后的溶液中只有NaCl,根据上述分析可知,NaCl的物质的量是0.4mol,则c(NaCl)=0.4mol÷0.1L=4.00mol/L,故答案是:4.00mol/L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】欲用下图装置对所制备的气体进行除杂检验,其设计方案合理的是
制备气体 | X(除杂试剂) | Y(检验试剂) |
| |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 | |
B | 电石与NaCl水溶液 | H2O | Br2的水溶液 | |
C | C2H5OH与浓硫酸加热至170℃ | 饱和NaHSO3溶液 | K2Cr2O7酸性溶液 | |
D | 生石灰与浓氨水 | 浓硫酸 | 红色石蕊试纸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A. 制取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 冶炼铝:铝土矿![]() NaAlO2
NaAlO2![]() 无水AlCl3
无水AlCl3![]() Al
Al
C. 制溴:浓缩海水![]() Br2
Br2![]() HBr(aq)
HBr(aq) ![]() Br2
Br2
D. 制碘:海带![]() 海带灰
海带灰![]() I2(aq)
I2(aq) ![]() I2
I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
主要化合价 | +1 | +2 | +1 | +3 | +5、﹣3 | +7、﹣1 | +5、﹣3 | ﹣2 |
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族);
(2)8个元素的最高价氧化物的水化物中,酸性最强的是(填化学式);
(3)元素⑤、⑦、⑧分别形成的简单气态氢化物中,⑦的电子式为 , 稳定性最强的氢化物的结构式为;
(4)写出①、④的最高价氧化物对应的水化物之间发生反应的离子方程式;
(5)用电子式表示元素①与⑥形成化合物的过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,成为化学史上的重要里程碑之一。下列说法中,不正确的是
A. 元素周期表有七个周期
B. 元素周期表有7个主族,7个副族
C. 氧元素位于第二周期ⅥA族
D. 稀有气体元素原子的最外层电子数均为8个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的物质的量为_______mol,NO2的物质的量为________mol。
(2)待产生的气体全部释放后,向溶液加入VmL、amolL-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中企部转化为NaNO3,至少需耍30%的双氧水______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
(1)x值等于________________;
(2)A的转化率为________;
(3)如果增大反应体系的压强,则平衡体系中C的质量分数________(增大、减小、不变)
(4)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4 /3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入B物质___ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如图所示。关于EGC的下列说法中正确的是
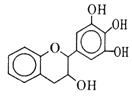
A. 遇FeCl3溶液不发生显色反应
B. 1 mol EGC与4 mol NaOH恰好完全反应
C. 易发生氧化反应和取代反应,难发生加成反应
D. 分子中所有的原子共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com