
【题目】工业电解饱和食盐水模拟装置的结构如图所示:


(1)写出电解饱和食盐水的化学方程式____,该工业称___工业。
(2)实际生产中使用的盐往往含有一些杂质,在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液,操作正确的顺序是____(选填字母)
a.①④②⑤③ b.⑤②④①③ c.②⑤④①③ d.⑤②④③①
(3)在该装置中写出装NaOH溶液试管中所发生的化学反应方程式_____。
(4)工业上用____(写物质名称)和电解产物____反应可制得漂粉精, 漂粉精敞口放置于空气中易失效,原因是(用化学方程式表示)___、____。
(5)工业上用两种电解产物在如图合成塔中合成氯化氢,A处通入___,B处通入___,后将氯化氢溶于水中即可得到盐酸,其电离方程式为___。
【答案】2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑ 氯碱 bc Cl2+2NaOH=NaCl+NaClO+H2O 氢氧化钠 氯气或Cl2 Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 2HClO=2HCl+O2↑ 氢气或H2 氯气或Cl2 HCl=H++Cl-
2NaOH+Cl2↑+H2↑ 氯碱 bc Cl2+2NaOH=NaCl+NaClO+H2O 氢氧化钠 氯气或Cl2 Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 2HClO=2HCl+O2↑ 氢气或H2 氯气或Cl2 HCl=H++Cl-
【解析】
(1)解氯化钠饱和溶液产物是氢氧化钠和氢气和氯气,电解方程式为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑,该工业称为氯碱工业,
2NaOH+Cl2↑+H2↑,该工业称为氯碱工业,
故答案为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑;氯碱;
2NaOH+Cl2↑+H2↑;氯碱;
(2)要先除硫酸根离子,然后再除钙离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加氢氧化钠除去镁离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,氢氧化钠除杂必须要在加盐酸之前即可,只要将三种离子除完,再进行过滤,最后加盐酸除去过量的氢氧根离子和碳酸根离子,顺序为:②⑤④①③或⑤②④①③。
答案选bc;
(3)氯气可以和氢氧化钠之间发生反应生成氯化钠、次氯酸钠和水,即Cl2+2NaOH=NaCl+NaClO+H2O;
答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)工业上用石灰乳和氯气反应可知的漂粉精,漂白粉露置在空气中失效的原因是Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO;2HClO=2HCl+O2↑ 。
答案为:氢氧化钠;氯气;Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO;2HClO=2HCl+O2↑ ;
(5)为了能将氯气包围,使氯气充分反应,减小环境污染,故A处通氢气,B处通氯气,氯化氢溶于水后的电离方程式为HCl=H++Cl-;
答案为:氢气或H2;氯气或Cl2;HCl=H++Cl-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】稠环芳烃如萘![]() 、菲
、菲 、芘
、芘 等均为重要的有机化工原料。下列说法正确的是
等均为重要的有机化工原料。下列说法正确的是
A. 萘、菲、芘互为同系物B. 萘、菲、芘的一氯代物分别为2、5、3种
C. 萘、菲、芘中只有萘能溶于水D. 萘、菲、芘的所有原子不可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液和FeCl36H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl36H2O。下列有关实验说法正确的是( )
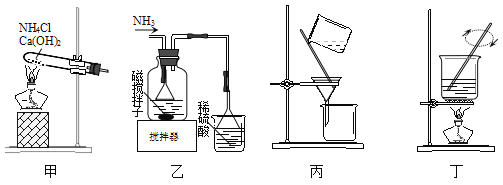
A. 用H2O2氧化废蚀刻液的离子方程式为:2H++2Fe2++H2O2=2Fe3++2H2O
B. 用装置甲可以制备Cu(NH3)4Cl2并沉铁
C. 用装置乙可以分离Cu(NH3)4Cl2溶液和Fe(OH)3
D. 用装置丁由FeCl3溶液制备FeCl36H2O需要经蒸发浓缩、冷却结晶、过滤洗涤等步骤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从粗铜精炼的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:(已知TeO2微溶于水,易溶于强酸和强碱) 下列有关说法正确的是

A. “氧化浸出”时为使碲元素沉淀充分,应加入过量的硫酸
B. “过滤”用到的玻璃仪器:分液漏斗、烧杯、玻璃棒
C. “还原”时发生的离子方程式为2SO32-+Te4++4OH-=Te↓+2SO42-+2H2O
D. 判断粗碲洗净的方法:取少量最后一次洗涤液,加入BaCl2溶液,没有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色固体)。

(1)Fe(OH)3中铁元素化合价为______,该脱氧反应中还原剂是_________。
(2)某化学兴趣小组用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g氯化钠)进行如下两个实验。
实验Ⅰ: 请回答:
①操作Ⅰ的名称是________,溶液丙中一定含有的金属阳离子是__________(写离子符号);
实验Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如下图(部分产物略去)。

②写出反应②的离子方程式,并用双线桥法表示电子转移的方向和数目_________;
③向溶液C中加入BaCl2溶液,有白色沉淀产生,其离子方程式为____________;反应③的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,其中X、Y、Z三种元素中,可形成含二种元素的10电子微粒m、n、p、q,且有反应m+n![]() p↑+q;M的最高价氧化物对应的水化物为最强酸。则下列说法不正确是
p↑+q;M的最高价氧化物对应的水化物为最强酸。则下列说法不正确是
A. 简单离子半径X<Z<Y<M
B. 由X、Y、Z三种元素组成的化合物可以是离子化合物
C. X、Y、Z三种元素组成的化合物的水溶液一定呈酸性
D. MZ2可用于自来水的杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
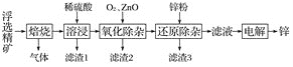
相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
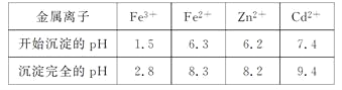
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为__________。
(2)滤渣1的主要成分除SiO2外还有________;氧化除杂工序中ZnO的作用是_____________,若不通入氧气,其后果是___________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为__________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为__________;沉积锌后的电解液可返回________工序继续使用。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com