
【题目】常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-) 、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )

A. AgCl的沉淀溶解平衡常数Ksp数量级为10-10
B. 为防止指示剂失效,溶液应维持中性或弱碱性
C. 滴定中指示剂的有效浓度应维持在2.0×10-2 mol/L
D. 滴定完后加入1mL 0.01mol/L H2SO4会产生新的沉淀
【答案】D
【解析】A.根据图像,硝酸银溶液的体积为25mL时,pAg=pCl =5,则AgCl的沉淀溶解平衡常数Ksp=1.0×10-5×1.0×10-5= 10-10,故A正确;B. K2CrO4中存在2CrO4 2-+ 2H+ =Cr2O7 2-+ H2O平衡,为防止指示剂失效,溶液应维持中性或弱碱性,故B正确;C. 溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,因此沉淀完全时,溶液中的c(Cl-)=c(Ag+)=1.0×10-5 mol/L,滴定中指示剂的有效浓度应维持在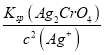 =
=![]() =2.0×10-2 mol/L,故C正确;D. 滴定完溶液中的c(Ag+)=1.0×10-5 mol/L,后加入1mL0.01mol/L H2SO4,c(SO42-)=
=2.0×10-2 mol/L,故C正确;D. 滴定完溶液中的c(Ag+)=1.0×10-5 mol/L,后加入1mL0.01mol/L H2SO4,c(SO42-)=![]() ≈0.004 mol/L,此时Qc= c2(Ag+)×c(SO42-)=4×10-13<1.4×10-5,不会产生新的沉淀,故D错误;故选D。
≈0.004 mol/L,此时Qc= c2(Ag+)×c(SO42-)=4×10-13<1.4×10-5,不会产生新的沉淀,故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】下列溶液中,Cl﹣离子浓度最大的是( )
A.0.5molL﹣1HCl溶液
B.1molL﹣1MgCl2溶液
C.2molL﹣1NaCl溶液
D.1molL﹣1FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
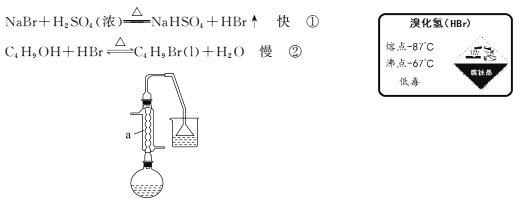
【题目】1-溴丁烷可用作稀有元素萃取剂。实验室制取1-溴丁烷的原理如下:
【产品制备】
如图,在125 mL烧瓶中加入10 mL水,然后加入12 mL(0.22 mol)浓硫酸,摇匀冷却至室温,再加入7.5 mL(0. 08 mol)正丁醇,混合后加入10.3 g(0. 10 mol)溴化钠晶体,充分振荡,加入几粒沸石,在石棉网上用小火加热烧瓶并回流半小时。
(1)仪器a的名称为____,用恰当的化学原理解释能发生反应①的原因是____。
(2)烧杯中所用试剂为水,其主要目的是吸收 ___(填化学式);
(3)制备过程中烧瓶中溶液逐渐出现浅黄色,为此,有人提出用浓H3PO4代替浓H2SO4,其理由是____。
【初步提纯】
已知:醇类可与浓硫酸作用生成![]() 盐溶于浓硫酸中(
盐溶于浓硫酸中(![]() 盐难溶于有机溶剂)。
盐难溶于有机溶剂)。
![]()
步骤①:加热蒸馏出烧瓶中所有的溴丁烷粗品。
步骤②:将粗品用5mL浓硫酸洗涤。
步骤③:将步骤②中有机层依次分别用水、饱和碳酸氢钠溶液和水各10 mL洗涤。
步骤④:将步骤③有机物移入蒸馏烧瓶中,加热蒸馏,得到产品6. 85 g。
(4)步骤①的目的是分离出产品中的无机物,判断溴丁烷是否完全蒸馏出来的方法是:用一支试管收集几滴馏出液,向其中加入少许水并摇动,如果____表明溴丁烷已经被 完全蒸馏出来。
(5)步骤②用5mL浓硫酸洗涤的目的是除去___ ;第一次水洗可以除去大部分硫酸,第二次水洗的目的是____。
(6)实验的产率为____(M(C4H9Br) =137 g/mol);制备过程中,有利于提高产品产率的措施有适当延长回流时间及____(选填字母)。
A.回流时适时搅拌溶液 B.将块状NaBr研细使用
C.将正丁醇分次加入 D.对正丁醇进行干燥处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。充电时总反应为LiAO2 + nC = Li1-xAO2 + LixCn(0<x<1),工作原理如下图所示,则以下说法正确的是( )
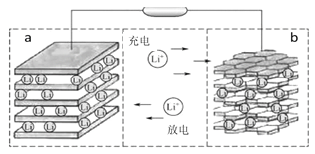
A. 放电时Ni元素最先失去电子
B. 放电时电子从a电极由导线移向b电极
C. 充电时的阳极反应式为LiAO2 - xe-= Li1-xAO2 + xLi+
D. 充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为________。
(2)某学生欲用上述浓盐酸和蒸馏水配制250 mL物质的量浓度为0.7 mol/L的稀盐酸。
①该学生用量筒量取________mL上述浓盐酸进行配制;
②所需的实验仪器有:
①胶头滴管、②烧杯、③量筒、④玻璃棒,配制稀盐酸时,还缺少的仪器有________。
③下列操作导致所配制的稀盐酸物质的量浓度偏低的是________(填字母)。
A.用量筒量取浓盐酸时俯视凹液面
B.未恢复到室温就将溶液注入容量瓶并进行定容
C.容量瓶用蒸馏水洗后未干燥
D.定容时仰视液面
E.未洗涤烧杯和玻璃棒
(3)若在标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________mol/L。(填选项字母)
a.![]() b.
b.![]() c.
c. ![]() d.
d. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,①6.72L NH3 ②1.204×1023个 H2S ③6.4g CH4 ④0.5mol HCl ,下列关系正确的是
A. 体积大小: ④>③>②>① B. 原子数目: ③>①>④>②
C. 密度大小: ④>②>③>① D. 质量大小: ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从含Br-废水中提取Br2的过程,包括过滤、氧化、正十二烷萃取及蒸馏等步骤。己知:
Br2 | CCl4 | 正十二烷 | |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
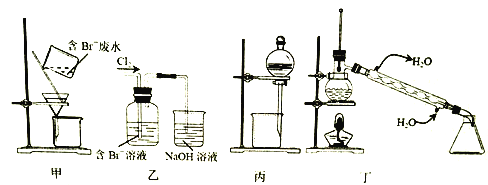
下列说法正确的是
A. 用甲装置过滤时,需不断搅拌
B. 丙装置中用正十二烷而不用CCl4,是因为其密度小
C. 用乙装置将Br-氧化为Br2
D. 可用装置丁进行蒸馏,先收集正十二烷再收集Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如下图所示位置,V甲:V乙=4:1(两侧温度、压强均相同)。则混合气体中CO和CO2的物质的量比为( )

A. 1:1 B. 1:3 C. 3:1 D. 2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com