
ijУ��ѧС��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ����ʵ�飬�����ò����һ����ȡ
FeCl3��6H2O���塣��ͼ�мгּ�β������װ�þ�����ȥ��
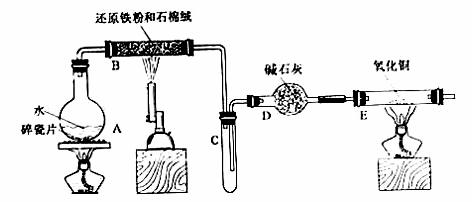
��1��װ��B�з�����Ӧ�Ļ�ѧ����ʽ��___________________________��
��2��װ��B�е�������________________________________________��
��3��ֹͣ��Ӧ����B����ȴ��ȡ���еĹ��壬�������ϡ�����ַ�Ӧ�����ˡ�����������Һ��Fe3+�IJ���������________________________��
��4����С��ѧ������������Һ��ȡFeCl3��6H2O���壬����������£�
��Һ FeCl3��Һ
FeCl3��Һ FeCl3��6H2O����
FeCl3��6H2O����
�ٲ������ͨ��Cl2��������____________________________________��
�ڲ�����FeCl3ϡ��Һ�еõ�FeCl3��6H2O�������Ҫ����������
_____________________________________________________________��
�۸��������豣�������������Ҫԭ���ǣ�������ӷ���ʽ��Ҫ˵����
_____________________________________________________________��
���𰸡�
��1��3Fe+4H2O(g)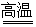 Fe3O4+4H2
Fe3O4+4H2
��2����ɫ�����죬�Ҷ˹ܱ���ˮ��
��3��ȡ������Һ�����뼸��KSCN��Һ���۲���Һ�Ƿ���ɫ
��4���ٽ�Fe2+������Fe3+
�ڼ���Ũ������ȴ�ᾧ������
��Fe3++3H2O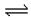 Fe(OH)3+3H+��������������FeCl3ˮ��
Fe(OH)3+3H+��������������FeCl3ˮ��
��������װ���и����ֵ����ü����ܷ����ķ�Ӧ��
A.����ˮ���������Ƭ���ֹ���е�����
B.ˮ�����ڸ�������Fe��Ӧ��3Fe��4H2O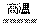 Fe3O4��4H2
Fe3O4��4H2
C.���塢��ȴ������ʹ�����е�H2O��������
D.�������ɵ�H2
E.H2�ڼ��������»�ԭCuO��H2��CuO Cu��H2O
Cu��H2O
Fe3O4�������Fe3O4��8HCl==2FeCl3��FeCl2��4H2O������Fe3���ܺ�SCN����Ӧ������Ѫ��ɫ��Һ��Fe3����3SCN��==Fe��SCN��3��
����Һ��ͨ��Cl2�ܽ�Fe2��ת���Fe3����2Fe2����Cl2==2Fe3����2Cl����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�У���Ӧ������������ص���
A������ͨ�����ȵ�Cu0��ĩ
B��������̼ͨ��Na202��ĩ
C������Fe203�������ȷ�Ӧ
D����п��Ͷ��Cu(N03)2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������������ɢϵ�ı��������ǣ� ����
A������ķ�ɢ��������ֽ
B�������ܲ������������
C�������ɢ������ֱ����1��100nm֮��
D�������Ǵ����������ɢϵ�ǻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��CO2��H2��ɵĻ������ͬ�¡�ͬѹ���뵪�����ܶ���ͬ����û��������CO2��H2����������Ϊ�� ����
A��29��8 B��22��1 C��13��8 D��8��13
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�ȥ���ʵ�ʵ�鷽����ȷ����
A.��ȥCO������O2��ͨ�����ȵ�Cu�������ռ�����
B.��ȥK2CO3����������NaHCO3�����������м���
C.��ȥ�������е��������ӣ���������Ũ��ˮ��Ӧ�����
D.��ȥFeCl3������Һ��������FeCl2�������Թ���˫��ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ����ϣ�����ѧ���ֱ���ͼʾ�ס�����װ�ã�̽����NaHCO3��Na2CO3��ϡ����ķ�Ӧ���������е��Լ�����������ͬ�����£������������еĹ����ĩͬʱ�����Թ��У�װ�õ��������Ѽ�飩��
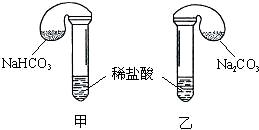
��ش�
��1�����鷴Ӧ��ʼʱ��________װ���е���������ȱ��װ���з�Ӧ�����ӷ���ʽ��___________________________��
��2�����Թ��в�������������ʱ������ʵ����ֲ�ͬ������д�±��Ŀո�
| �Լ����� | ʵ������ ����������仯�� | ����ԭ�� | |
| �� �� �� | 0.42 g NaHCO3 0.53 g Na2CO3 3 mL 4 mol/L���� | ������������������������� | �ס������������ n��NaHCO3��=n��Na2CO3�� V����CO2��=V����CO2�� |
| �� �� �� | 0.3 g NaHCO3 0.3 g Na2CO3 3 mL 4 mol/L���� | ����������������������� | |
| �� �� �� | 0.6 g NaHCO3 0.6 g Na2CO3 3 mL 2 mol/L���� | ����������������������� | |
| Ƭ�̺�������������С���������������������� | �������ӷ���ʽ��ʾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ƣ�Na2FeO4�����Զ�����ˮ���о����������������з����Ƶã��� Fe2O3+3Na2O2  2Na2FeO4+Na2O�����ڸ÷�Ӧ˵����ȷ����
2Na2FeO4+Na2O�����ڸ÷�Ӧ˵����ȷ����
��A��Na2FeO4���ڹ��ۻ����� ��B����Ӧ��Na2O2��������
��C������1 mol Na2FeO4����6 mol ����ת��
��D����Na2FeO4��FeΪ+4�ۣ�����ǿ�����ԣ�������ɱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
H2O2�ڹ�ҵ��ũҵ��ҽҩ�϶��й㷺����;��
��1���������ʶ�������H2O2�ֽ�Ĵ�����һ�ֹ۵���Ϊ���ڷ�Ӧ�����д����ȱ�H2O2��������ԭ�������ֱ�H2O2��ԭ�������������������ʶ�����H2O2�ֽ�Ĵ������ڷ�Ӧ�������ȱ���������ԭ���������������������������� ��
a�� I���� ��������b�� Fe3������ ����c�� Cu2���� ������d�� Fe2��
��2���ü�������ȼ�ϵ�غϳ�H2O2������Ч�ʸߣ�����Ⱦ���ص㡣����ܷ�ӦΪ��
H2 + O2 + OH����H2O + HO2����д��������Ӧʽ�������������������������������������� ��
��3��H2O2��һ�ֻ����Ѻõ�ǿ����������Ʒ�ˮ����Ҫ��Cu2����Ni2������������Fe3����Fe2����Cr3�� �ȣ��Ʊ���������һ���������£�

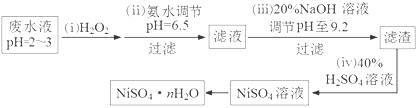
���ٵڣ�������������H2O2��Ӧ�����ӷ���ʽ������������������������������������ ��
��Ϊ�ⶨNiSO4��nH2O����ɣ���������ʵ�飺��ȡ 2.627g��Ʒ�����Ƴ�250.00 mL��Һ��ȷ��ȡ���Ƶ���Һ25.00 mL����0.04000 mol��L��1��EDTA��Na2H2Y������Һ�ζ�Ni2+�����ӷ���ʽΪNi2��+ H2Y2����NiY2��+ 2H����������EDTA����Һ25.00 mL��������������Ļ�ѧʽΪ���������� ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��̬������A�����ֶ�����Ԫ����ɣ�����ˮ�������ֽⷴӦ������ͬѧ����27ͼװ�ã��г�װ���ԣ��������̽��ʵ�顣
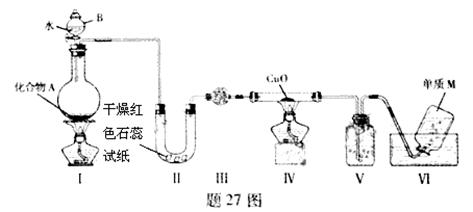
��1������B��������____________��
��2�������У����е���ֽ���������к�ɫ��ĩ��Ϊ��ɫ����M���ɣ�����е��Լ�Ϊ
__________________����������Ӧ�Ļ�ѧ����ʽΪ____________�����е��Լ�Ϊ____________________��
��3������ͬѧ����ͬ��ʵ�飬��װ������˳��Ϊ������������������������ʱ��������Ϊ________��ԭ����__________________��
��4����������Ӧ��2.5g ������A�����Ͽɵ�0.56L����״����M����A�Ļ�ѧʽΪ________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com