
 科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质.
科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质. 代表氢原子,
代表氢原子, 代表碳原子)和水,该有机物的结构简式为
代表碳原子)和水,该有机物的结构简式为 ,该烷烃的名称为
,该烷烃的名称为 ,该烷烃的名称为:2,3-二甲基戊烷,分子中有6中氢原子,故一溴代物有6种,
,该烷烃的名称为:2,3-二甲基戊烷,分子中有6中氢原子,故一溴代物有6种,

科目:高中化学 来源: 题型:
| A、晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B、沸点由高到低:Na>Mg>Al |
| C、硬度由大到小:金刚石>SiC>晶体硅 |
| D、晶格能由大到小:MgF2>NaCl>NaBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
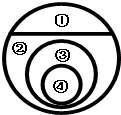 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物物质之间的包含与不包含关系,若整个大圆代表纯净物,则①③所属的类别是( )
如图表示的是纯净物、单质、化合物、含氧化合物、氧化物物质之间的包含与不包含关系,若整个大圆代表纯净物,则①③所属的类别是( )| A、①单质、③氧化物 |
| B、①单质、③含氧化合物 |
| C、①化合物、③氧化物 |
| D、①化合物、③含氧化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、反应中只有CuO是氧化剂 |
| B、该反应中Cu2S是还原剂 |
| C、该反应中,氧元素氧化了硫元素 |
| D、该反应中,Cu2S既是还原剂又是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 有A、B、C、D四中元素,其中A的基态原子核外电子有11中运动状态,B的基态原子得一个电子喉3p轨道就处于全充满状态,C的最常见气态氢化物呈碱性,D与A能形成离子化合物A2D且D2-比A+多一个电子层.
有A、B、C、D四中元素,其中A的基态原子核外电子有11中运动状态,B的基态原子得一个电子喉3p轨道就处于全充满状态,C的最常见气态氢化物呈碱性,D与A能形成离子化合物A2D且D2-比A+多一个电子层.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com