
【题目】为探究Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:


定性分析:(1)如图甲所示可通过观察____________________,定性比较得出结论.
(2)有同学提出试剂的选择不妥,应将FeCl3改为更为_____________合理。
(3)H2O2在二氧化锰作用下发生的反应可分为两步,第一步的方程式为:2MnO2+H2O2=2HMnO3,第二步的化学方程式为:___________________________,若第一步反应慢第二步反应快,则总反应速率由_____________(填“第一步”或“ 第二步”)决定。
定量分析:(4)如图乙所示,以实验时均生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是:_____________________________.
【答案】 两支试管中产生气泡的快慢 Fe2(SO4)3 2HMnO3+H2O2=2MnO2+2H2O+O2↑ 第一步 产生40ml气体所需要的时间
【解析】(1)该反应中产生气体,所以可根据生成气泡的快慢判断,即可通过观察两支试管中产生气泡的快慢定性比较得出结论;(2)氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用,因此为消除阴离子的干扰,应将FeCl3改为更为Fe2(SO4)3合理;(3)双氧水在二氧化锰作用下生成水和氧气,所以反应方程式为2H2O2=2H2O+O2↑,因此第二步的化学方程式为2HMnO3+H2O2=2MnO2+2H2O+O2↑;总反应速率由反应最慢的那一步决定,所以总反应速率由第一步决定。(4)该反应是通过生成气体的反应速率分析判断的,所以根据v=△V÷△t知,需要测量的数据是产生40mL气体所需要的时间。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(含有Cu2O(主要)、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知:Cu2O+2H+=Cu+Cu2++H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是______________.
(2)反应Ⅰ完成后,铁元素的存在形式为_____________.(填离子符号)请写出生成该离子的离子方程式_________________________.
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为_____________。
(4)书写出由沉淀C制备铝的化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,该反应达到平衡状态所需时间是_________。

(2)上图中表示NO2的浓度变化曲线是_______________。
(3)用NO表示从0~2s内该反应的平均速率v=________。
(4)v(NO):v(O2) = ______________。
(5)达到平衡状态时O2的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四瓶溶液分别是FeCl3溶液、NaCl溶液、(NH4)2SO4溶液、MgSO4溶液,下列试剂中可用于鉴别它们的是
A.氨水 B.NaOH溶液 C.稀盐酸 D.BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【物质结构与性质】
铝及其化合物在工农业生产生活中有着重要的用途。
(1)离子镀钛氮化铝是一种高强度的保护层,Ti基态核外电子排布式为 。
(2)AlCl3是有机反应中常用的催化剂。

有机物①碳原子的杂化类型为 。1 mol有机物②分子中含有σ键的数目为 mol。
(3)一定条件下用Al2O3和CCl4反应制备COCl2,写出与COCl2互为等电子体的阴离子的化学式:
。
(4)双聚物Al2Cl6结构如图甲所示。在Al2Cl6中存在的相互作用有 (填字母)。
a.范德华力 b.离子键 c.共价键 d.氢键 e.配位键
(5)氮化铝(其晶胞如图乙所示) 晶体中离铝原子最近的氮原子的个数为 。


甲 乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质是一类在水溶液或熔融状态下能够导电的化合物。下列物质属于电解质的是
A. Cl2 B. NaOH C. C2H5OH D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)污染也跟冬季燃煤密切相关。SO2、CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)反应过程能量变化如图所示:
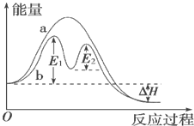
下列说法正确的是_____。
A.反应过程a有催化剂参与
B.该反应为放热反应,热效应等于ΔH
C.改变催化剂,能改变该反应的活化能和反应热
D.有催化剂条件下,反应的活化能等于E1
(2)己知:CH3OH、H2的燃烧热(ΔH)分别为﹣726.5kJ/mol、﹣285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是 。
(3)工业上还可以通过下列反应制备甲醇:CO(g)+2H2(g)![]() CH3OH(g)。在一容积可变的密闭容器 中充入10mol CO和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH(g)。在一容积可变的密闭容器 中充入10mol CO和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。

①下列说法不能判断该反应达到化学平衡状态的是_________(填字母)。
a.H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA__________PB(填“>、<、=”)。
③若达到化学平衡状态A时,容器的体积为20L。如果反应开始时仍充入10molCO和20molH2,则在平衡状态B时容器的体积V(B)=__________L。
(4)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀银的装置示意图:

①该电池的负极反应式是 。
②当甲中消耗标况下1.12L氧气时,乙中 极(填a或b)增重_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com