
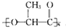
 ,它能代替聚苯乙烯.它是由乳酸(一种有机酸)缩聚而成,能在乳酸菌的作用下降解而不会污染环境.下列关于聚乳酸的说法正确的是( )
,它能代替聚苯乙烯.它是由乳酸(一种有机酸)缩聚而成,能在乳酸菌的作用下降解而不会污染环境.下列关于聚乳酸的说法正确的是( )| A、聚乳酸是一种纯净物 |
B、聚乳酸的单体是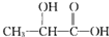 |
| C、聚乳酸是一种羧酸 |
| D、聚乳酸是由其单体通过加聚反应合成的 |
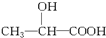 ,故B正确;
,故B正确;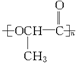 ,同时有小分子物质水生成,不属于加聚反应,故D错误;
,同时有小分子物质水生成,不属于加聚反应,故D错误;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、实验中所用到的滴定管、容量瓶在使用前均需要查漏 |
| B、若选用100 mL容量瓶配制标准酸溶液,需用密度为1.84g/mL、98%的浓硫酸5.4mL |
| C、中和滴定实验,若滴定前平视读数、滴定结束俯视读数,则导致实验结果偏大 |
| D、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑 | 浓硫酸有吸水性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将NH3通过灼热的氧化铜固体 | 固体变红 | 氨气具有还原性 |
| D | 过量的SO2通入到含有少量NaOH的酚酞溶液中 | 溶液红色逐渐褪去 | SO2具有漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢化物沸点:HI>HBr>HCl>HF |
| B、分子稳定性:HF>H2O>H2S |
| C、离子半径:K+>Cl->S2- |
| D、单质的熔点:Li<Na<K<Rb |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,在体积为10L的固定容器中发生反应:
一定条件下,在体积为10L的固定容器中发生反应:| A、t1 min时正、逆反应速率相等 | ||
| B、X曲线表示NH3的物质的量随时间变化的关系 | ||
C、0~8 min,H2的平均反应速率v(H2)=
| ||
| D、10~12 min,升高温度使反应速率加快,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.镍行业发展蕴藏着巨大潜力.
目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.镍行业发展蕴藏着巨大潜力. 分子内的作用力有
分子内的作用力有 ④HCHO等,其中分子属于平面结构的有
④HCHO等,其中分子属于平面结构的有 中C的杂化方式为
中C的杂化方式为查看答案和解析>>
科目:高中化学 来源: 题型:

| Cu2O/ZnO |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com