
【题目】已知某无色溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、AlO2-、CO32-、SO42-、I-、SiO32-,MnO4-中的N种离子组成。某化学兴趣小组通过下列实验确定了其组成:
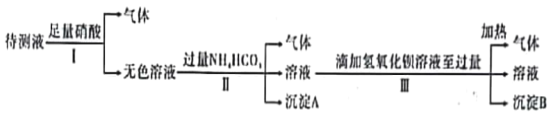
回答下列问题:
(1)不用做实验就可以肯定原溶液X中不存在的离子是_______________(填离子符号)。
(2)通过上述实验知,X溶液中一定存在__________种离子(填数字;不考虑H+、OH-)。
(3)在上述滴加氢氧化钡溶液过程中,开始阶段发生反应的离子方程式一定有_____________
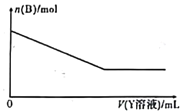
(4)该化学兴趣小组的同学为了进一步确定白色沉淀B的成分,取一定量经洗涤后的B与Y溶液反应,沉淀B的物质的量与Y溶液体积之间的关系如图所示。Y可能为____________。B的组成为__________________
【答案】Cu2+、Fe2+、MnO4- 3 Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2O HNO3(或HCl、HI、HClO4等) BaCO3和BaSO4
【解析】
已知溶液为无色溶液,则不存在有颜色的离子,即可确定没有Cu2+(蓝色)、Fe2+(浅绿色)、MnO4-(紫红色);取适量该溶液,加入足量硝酸,有气体生成,则溶液中一定存在CO32,根据离子共存知,一定不存在与CO32发生反应的Mg2+、Ag+、Ba2+、Al3+离子;同时得到无色溶液,则一定不存在I、SiO32,再根据溶液呈电中性判断原溶液中一定存在唯一阳离子K+;无色溶液中再加入过量NH4HCO3溶液,有气体生成,同时析出沉淀A,说明溶液中一定存在Al3+,原溶液中一定存在AlO2,反应的离子方程式为:Al3+ + 3HCO3- = Al(OH)3↓+3CO2↑,在所得溶液中含有过量的碳酸氢铵,继续滴加氢氧化钡溶液至过量,加热会有氨气生成,沉淀可能为碳酸钡或碳酸钡和硫酸钡的混合物,则X溶液中一定存在CO32、K+、AlO2,据此解答。
(1)已知溶液为无色溶液,则不存在有颜色的离子,即可确定没有Cu2+(蓝色)、Fe2+(浅绿色)、MnO4-(紫红色);
故答案为:Cu2+、Fe2+、MnO4-;
(2)取适量该溶液,加入足量硝酸,有气体生成,则溶液中一定存在CO32,该气体为二氧化碳,根据离子共存知,一定不存在与CO32发生反应的Mg2+、Ag+、Ba2+、Al3+离子;同时得到无色溶液,则一定不存在I、SiO32,再根据溶液呈电中性判断原溶液中一定存在唯一阳离子K+;无色溶液中再加入过量NH4HCO3溶液,有气体生成,同时析出沉淀A,说明溶液中一定存在Al3+,原溶液中一定存在AlO2,反应的离子方程式为:Al3+ + 3HCO3- = Al(OH)3↓+3CO2↑,在所得溶液中含有过量的碳酸氢铵,继续滴加氢氧化钡溶液至过量,加热会有氨气生成,沉淀可能为碳酸钡或碳酸钡和硫酸钡的混合物,则X溶液中一定存在CO32、K+、AlO2,共3种离子;
故答案为:3;
(3)在上述滴加氢氧化钡溶液过程中,开始阶段OH-先与HCO3-反应生成CO32-和H2O,同时生成BaCO3沉淀,此时氢氧化钡的量少,以氢氧化钡为1mol配平该离子方程式,则开始阶段发生反应的离子方程式一定有Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2O;
故答案为:Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2O;
(4)由图像可知沉淀B部分溶于Y溶液,BaCO3溶于HNO3(或HCl、HI、HClO4等),则Y可能为于HNO3(或HCl、HI、HClO4等),则B中一定含有BaCO3、BaSO4;
故答案为:HNO3(或HCl、HI、HClO4等);BaCO3和BaSO4。


科目:高中化学 来源: 题型:
【题目】有以下物质:①石墨;②水银;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧冰酷酸(CH3COOH);⑨氧化钠固体; ⑩液态氯化氢。
(1)其中能导电的是_________; 属于非电解质的是_________; 属于电解质的是____________
(2)等质量④和⑤中氢原子的数目之比为_____; 若④和⑤中所含氢原子数相等, 在相同条件下④和⑤的体积之比为____________
(3)向⑥中加入少量⑦请写出离子方程式:____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氟利昂-12(CF2Cl2)是甲烷的氯、氟卤代物,它有2种同分异构体
B.对甲基苯甲醛(![]() )使高锰酸钾酸性溶液褪色,说明它含有醛基
)使高锰酸钾酸性溶液褪色,说明它含有醛基
C.溴水可以区分苯和乙酸
D.糖类是食物组成中的重要部分,也是产生能量最高的营养物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. ![]() σ键和π键比例为7:1
σ键和π键比例为7:1
B. 某元素气态基态原子的逐级电离能(kJmol﹣1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+
C. C22﹣与O22+互为等电子体,1 mol O22+中含有的π键数目为2NA, O22+的电子式可表示为 ![]()
D. 已知反应N2O4(l)+2N2H4(l)═3N2(g)+4H2O(l),若该反应中有4 mol N﹣H键断裂,则形成的π键数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某离子晶体的晶胞示意图如下图所示,其摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,晶体的密度为d g·cm-3。
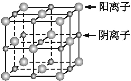
下列说法中正确的是
A. 晶体晶胞中阴、阳离子的个数都为1
B. 晶体中阴、阳离子的配位数都是4
C. 该晶胞可能是NaCl的晶胞
D. 该晶体中两个距离最近的阳离子的核间距为M/d cm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示阴阳膜组合电解装置用于循环脱硫,用NaOH溶液在反应池中吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解又制得NaOH。其中a、b离子交换膜将电解槽分为三个区域,电极材料为石墨,产品C为H2SO4溶液。下列说法正确的是( )

A. b为只允许阳离子通过的离子交换膜
B. 阴极区中B最初充入稀NaOH溶液,产品E为氧气
C. 反应池采用气、液逆流方式,目的是使反应更充分
D. 阳极的电极反应式为SO32-+2e-+H2O===2H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油画所用的颜料有许多天然矿石成分,矿石中往往含有B、C、O、Na、P、Cl等元素,它们在科学研究和工业生产中具有许多用途。请回答下列有关问题:
(1)现代化学中,常利用_________上的特征谱线来鉴定元素。
(2)CH3+、-CH3、CH3-都是重要的有机反应中间体。CH3+中碳原子的杂化方式为_________,CH3-的空间构型为_______。
(3) Na+和Ne互为等电子体,电离能I2(Na)______I1(Ne)(填“>”或“<”)。
(4)氢卤酸(HX)的电离过程如图。ΔH1和ΔH2的递变规律都是HF>HCl>HBr>HI,其中ΔH1(HF)特别大的原因为__________,从原子结构分析影响ΔH2递变的因素为__________。

(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。
① 磷化硼晶体晶胞如图甲所示:其中实心球为磷原子。已知晶胞中最近的B、P原子的距离为apm,阿伏加德罗常数为NA。则磷化硼晶体的密度为___________g/cm3。(列出计算式即可,不必化简)
② 磷化硼晶胞沿着体对角线方向的投影(图乙中![]() 表示P原子的投影),用
表示P原子的投影),用![]() 画出B原子的投影位置____。
画出B原子的投影位置____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、如图所示,高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是______________。
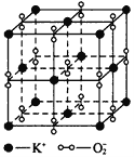
A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O![]()
B.晶体中每个K+周围有8个O![]() ,每个O
,每个O![]() 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中,0价氧与-2价氧的数目比为3∶1
II、有A、B、C三种晶体,分别由C、H、Na、Cl四种元素中的一种或几种形成,对这3种晶体进行实验,结果如表所示:
项目 | 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与Ag+反应 |
A | 811 | 较大 | 易溶 | 水溶液(或熔融)导电 | 白色沉淀 |
B | 3500 | 很大 | 不溶 | 不导电 | 不反应 |
C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
(1)晶体A的化学式为____________________。
(2)晶体B的晶体类型为____________________。
(3)晶体C中粒子间的作用力为____________________。
III、砷化镓是优良的半导体材料,可用于制作微型激光器或太阳能电池等。
(1)砷化镓的晶胞结构如下图所示,则砷化镓的化学式为____。

(2)基态As原子的核外电子排布式为_________。
(3)第一电离能:Ga____As(填“>”或“<”)。
(4)GaF3的熔点高于1 000 ℃,GaCl3的熔点为77.9 ℃,其原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氯水的叙述不正确的是( )
A.新制氯水可使pH试纸先变红,后褪色B.氯水放置数天后,溶液的酸性逐渐减弱
C.新制的氯水只含Cl2、H2O和HClO三种分子D.光照氯水有气泡逸出,该气体是O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com