
【题目】氮族元素及其化合物应用广泛。如合成氨、磷肥等化学肥料促进了粮食产量的极大提高。
(1)在基态31P原子中,核外存在_____对自旋相反的电子,核外电子占据的最高能级的电子云轮廓图为_____形。与31P同周期且相邻的元素的第一电离能由大到小的顺序为_____。
(2)液氨中存在电离平衡2NH3![]() NH4++NH2﹣,体系中三种微粒中N原子的杂化方式为_____,NH2﹣的立体构型为_____,与NH4+互为等电子体的分子为_____。
NH4++NH2﹣,体系中三种微粒中N原子的杂化方式为_____,NH2﹣的立体构型为_____,与NH4+互为等电子体的分子为_____。
(3)苯胺 ![]() 与甲苯
与甲苯 ![]() 的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣95℃)、沸点(110.6℃),原因是_____。
的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣95℃)、沸点(110.6℃),原因是_____。
(4)我国科学工作者实现世界首次全氮阴离子(N5﹣)金属盐Co(N5)2(H2O)44H2O的合成,其结构如图所示,Co2+的配位数为_____;N5﹣的化学键类型为_____。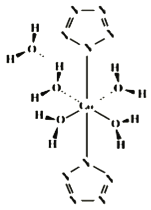
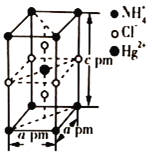
(5)把特定物质的量之比的NH4Cl和HgCl2在密封管中一起加热时,生成晶体X,其晶胞的结构图及晶胞参数如图所示。则晶体X的密度为_____ g/cm3(设阿伏加德罗常数的值为NA,列出计算式)。
【答案】6 哑铃(纺锤) P>S>Si sp 3 杂化 V 形 CH4、SiH4 苯胺分子间存在氢键 6 σ键、π键 ![]()
【解析】
(1)、根据31P原子的电子排布1s22s22p63s23p2解答;
(2)、根据价层电子对互斥理论解答;
(3)、同为分子晶体,且相对分子质量差较小,而熔沸点相差较大,则可能是存在分子间氢键;
(4)、根据图示可以确定物质中存在的化学键;
(5)、由均摊法可知,1个晶胞中Hg2+数目为1,NH4+数目为1,Cl﹣数目为3,晶体密度ρ=![]() ,据此计算。
,据此计算。
(1)31P原子的电子排布是1s22s22p63s23p2,可知核外存在6对自旋相反的电子,最外层为p轨道,电子云轮廓图为哑铃(纺锤)形。与P同周期相邻的元素为Si、S,同周期随原子序数增大,元素第一电离能呈增大趋势,P元素原子3p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:P>S>Si。
故答案为:6;哑铃(纺锤); P>S>Si;
(2)NH3中心原子N电子对数=![]() (5﹣1×3)+3=4,杂化方式为sp 3;NH4+中心原子N电子对数=
(5﹣1×3)+3=4,杂化方式为sp 3;NH4+中心原子N电子对数=![]() (5﹣1﹣1×4)+4=4,杂化方式为sp 3;NH2﹣中心原子N电子对数=
(5﹣1﹣1×4)+4=4,杂化方式为sp 3;NH2﹣中心原子N电子对数=![]() (5+1﹣1×2)+2=4,杂化方式为sp 3,孤电子对数为2,空间构型为V形。等电子体为原子数相等和电子数相等的原子团,NH4+含有5个原子,电子数为10,与NH4+互为等电子体的分子为CH4、SiH4等
(5+1﹣1×2)+2=4,杂化方式为sp 3,孤电子对数为2,空间构型为V形。等电子体为原子数相等和电子数相等的原子团,NH4+含有5个原子,电子数为10,与NH4+互为等电子体的分子为CH4、SiH4等
故答案为:sp 3 杂化; V 形;CH4、SiH4;
(3)苯胺![]() )的晶体类型是分子晶体,构成微粒为分子,苯胺与甲苯(
)的晶体类型是分子晶体,构成微粒为分子,苯胺与甲苯(![]() )的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣95.0℃)、沸点(110.6℃),原因是苯胺分子之间存在氢键,
)的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣95.0℃)、沸点(110.6℃),原因是苯胺分子之间存在氢键,
故答案为:苯胺分子间存在氢键;
(4)由图知,Co(N5)2(H2O)44H2O中Co2+连接2个(N5﹣)和4个H2O,其配位数为6,N5﹣存在的化学键为σ键、π键。
故答案为:6; σ键、π键;
(5)由均摊法可知,1个晶胞中Hg2+数目为1,NH4+数目为8×![]() =1,Cl﹣数目为4×
=1,Cl﹣数目为4×![]() +2=3,晶胞质量m=
+2=3,晶胞质量m=![]() =
=![]() ,晶胞体积V=a×10﹣10×a×10﹣10×c×10﹣10=a2c×10﹣30,晶体X的密度ρ=
,晶胞体积V=a×10﹣10×a×10﹣10×c×10﹣10=a2c×10﹣30,晶体X的密度ρ=![]() =
=![]() g/cm3,
g/cm3,
故答案为:![]() 。
。


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注。一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g)![]() CaS(s)+3CO2(g) △H=-394.0kJ/mol。保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):
CaS(s)+3CO2(g) △H=-394.0kJ/mol。保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):
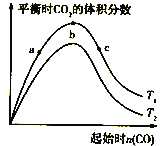
下列有关说法正确的是
A. T1比T2高 B. b点SO2转化率最高
C. b点后曲线下降是因CO体积分数升高 D. 减小压强可提高CO、SO2转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中充入CO2与H2进行反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
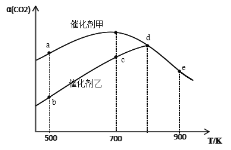
下列叙述正确的是
A. 该可逆反应的ΔH>0
B. 催化剂甲作用下反应的活化能比催化剂乙作用下反应的活化能大
C. 500K下达到平衡时,反应在催化剂甲作用下的转化率比在催化剂乙作用下的转化率高
D. d、e两点反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积为1 L的密闭容器中发生可逆反应:Fe(s)+H2O(g) ![]() FeO(s)+H2(g) ΔH>0。在1 000℃时,H2O(g)的平衡转化率(α)与体系总压强(p)关系如图所示。
FeO(s)+H2(g) ΔH>0。在1 000℃时,H2O(g)的平衡转化率(α)与体系总压强(p)关系如图所示。
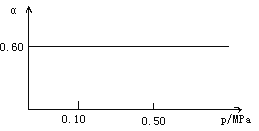
(1)写出该反应的平衡常数表达式K=__________。当反应达到平衡后,再向容器中加入铁粉和水蒸气,则K__________,(填“增大”、“减小”或“不变”,下同);升高温度,则K__________。
(2)在1 000℃时,若向上述容器中加入0.80 mol铁粉和1.00 mol水蒸气,达到平衡时,容器中c(H2)=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下两个热化学方程式:
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220 kJ·mol-1
试回答下列问题:
(1)H2的燃烧热为______,C3H8的燃烧热为________。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧所释放的热量为________。
(3)现有H2和C3H8的混合气体共1 mol,完全燃烧时放出的热量为769.4 kJ,则在混合气体中H2和C3H8的体积比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用下图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式:2KMnO4+16HCl(浓) == 2KCl+2MnCl2 + 5Cl2↑+ 8H2O ]

【实验探究】
(1)A装置中a仪器的名称是_____________。
(2)制取氯气反应中KMnO4所起的作用是_____(填“氧化剂”或“还原剂”)。
(3)实验进行一段时间后,可观察到______(填“B”或“C”)装置中有色布条褪色,其褪色原因是______________________________________。
(4)当氯气进入D装置后,可观察到溶液颜色变为_______(填“红色”或“蓝色”),写出相关反应的化学方程式___________________________________。
(5)E装置中NaOH溶液的作用是_____________________________________。
(6)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____L氯气。(KMnO4的摩尔质量为158 g·mol—1)
【知识拓展】
(7)近年来,某些含氯的化合物(如ClO2、NaClO等)在生产、生活中应用广泛。
①高效净水剂ClO2中氯元素的化合价为_____________。
②NaClO是一种强氧化剂。某种家用洗涤剂含有NaClO,请写出NaClO在洗涤过程中的一种作用___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量不超过100的有机物A,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 A完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现A的氢谱如下:

(1)A的分子式为___________________________________;
(2)A的结构简式为:___________________________________;
(3)A是否存在顺反异构?___________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒定温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A (g)+2B (g)4C (?)+2D (?),“?”代表状态不确定。反应一段时间后达到平衡,测得生成 1.6 mol C,且反应前后压强之比为5:4,则下列说法正确的是
A.增加C,B的平衡转化率不变
B.此时B的平衡转化率是35%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.该反应的化学平衡常数表达式是K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据元素性质、相对原子质量等进行排列,预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法错误的是

A.乙元素位于现行元素周期表第四周期第ⅥA族B.原子半径:甲>乙> Si
C.乙的简单气态氢化物的稳定性弱于CH4D.推测乙的单质可以用作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com