
【题目】工业、上常用钛铁矿[主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质]作原料,制取二氧化钛及铁红,其生产流程如图:
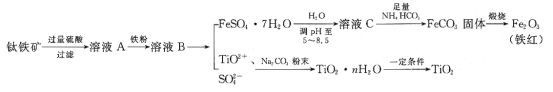
已知:TiO2+易水解,只能存在于强酸性溶液中。
回答下列问题:
(1)钛铁矿用硫酸溶解时,过滤所得滤渣的成分是__(填化学式)。
(2)从溶液B中得到FeSO4·7H2O晶体的操作是__、过滤、洗涤、干燥。
(3)溶液C中加入NH4HCO3,发生反应的离子方程式是__。
(4)煅烧FeCO3,发生反应的化学方程式是__。
(5)流程中加入Na2CO3粉末得到固体TiO2·nH2O。请结合TiO2+的水解平衡原理解释其原因:__。
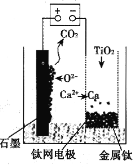
(6)用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制取金属钛。阳极反应式是__,反应过程中CaO的物质的量__(填“减小”“不变”或“增大”)。
【答案】SiO2 蒸发浓缩、冷却结晶 Fe2++2HCO3 =FeCO3↓+CO2↑+H2O 4FeCO3+O2![]() 2Fe2O3+4CO2 TiO2++(n+1)H2OTiO2·nH2O+2H+,加入Na2CO3粉末消耗H+,平衡正向移动,生成TiO2·nH2O C+2O2-4e===CO2↑ 不变
2Fe2O3+4CO2 TiO2++(n+1)H2OTiO2·nH2O+2H+,加入Na2CO3粉末消耗H+,平衡正向移动,生成TiO2·nH2O C+2O2-4e===CO2↑ 不变
【解析】
钛铁矿[主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质]加过量硫酸,FeTiO3溶于过量硫酸,生成Fe2+、TiO2+、H2O,Fe2O3溶于过量硫酸,生成Fe3+离子,SiO2杂质不溶于酸,滤液A主要阳离子为Fe2+、TiO2+、Fe3+;加入铁粉,发生了反应:2Fe3++Fe═3Fe2+,溶液B主要阳离子为Fe2+ 、TiO2+,蒸发浓缩冷却结晶得绿矾和TiO2+、SO42-,加入碳酸钠粉末生成TiO2nH2O,一定条件下得到TiO2;绿矾加水溶解,调节pH至5~8.5防止水解,溶液C溶质主要为FeSO4,加入足量的NH4 HCO3,生成FeCO3,经过煅烧后得到Fe2O3 。
(1)根据分析可知滤渣主要为不溶于酸的SiO2;
(2)从溶液中得到晶体的一般操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(3)加入碳酸氢铵后,Fe2+与碳酸氢根电离出的碳酸根结合生成碳酸亚铁沉淀,促进碳酸氢根的电离,氢离子浓度增大,氢离子浓度增大后又促进碳酸氢根的水解,生成二氧化碳,所以离子方程式为:Fe2++2HCO3 =FeCO3↓+CO2↑+H2O;
(4)煅烧FeCO3生成三氧化二铁和二氧化碳,Fe2+别氧化,结合元素守恒可知氧化剂为O2,根据电子守恒可得方程式为:4FeCO3+O2![]() 2Fe2O3+4CO2;
2Fe2O3+4CO2;
(5)溶液中存在平衡TiO2++(n+1)H2OTiO2·nH2O+2H+,加入Na2CO3粉末消耗H+,平衡正向移动,生成TiO2·nH2O;
(6)与正极相连的是阳极,据图可知石墨电极为阳极,反应过程中C被氧化生成CO2,所以电极方程式为:C+2O2-4e===CO2↑;阴极上电极反应式为:2Ca2++4e-═2Ca,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变。


科目:高中化学 来源: 题型:
【题目】下列混合物的物质的量一定时,组内各物质按任意比混合,完全燃烧耗O2的量不变的是
A.甲烷、甲醇、甲醛;B.乙炔、苯、1,3-丁二烯
C.丙烯、2-丁烯、环已烷D.乙醇、乙烯、丙烯酸(CH2=CH-COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题:
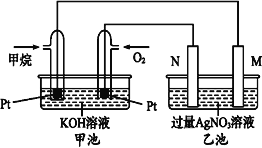
(1)M电极的材料是_____, 其电极反应式为:_______。N的电极名称是_____,其电极反应式为:_____。
(2)通入O2的铂电极的电极反应式为:________。
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为_____L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
B.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,生成H2的体积为112mL
C.常温常压下,3.2 g O2所含的原子数为0.2NA
D.标准状况下,2.24 LH2O含有的H2O分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语回答下列问题。

(1)元素①的原子结构示意图为_________。
(2)元素③和⑥可形成化合物,用电子式表示形成其过程_________。
(3)元素②、③形成简单离子的半径(填离子符号)_________>_________。
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)______>_______;元素③、④形成的最高价氧化物水化物的碱性_________>_________。
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一 《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二 公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)某研究性学习小组用如图所示试验装置对绿矾的焙烧反应进行探究。
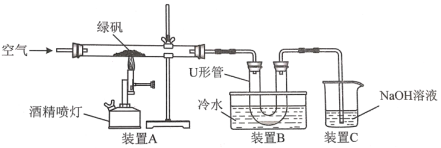
①实验过程中,装置A玻管中可观察到的实验现象是__。
②装置C的作用是__。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入__(填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有SO42-的方法是__。
(2)某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,计算理论上所需绿矾的质量,写出计算过程。___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯并环己酮是合成萘(![]() )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如图所示:
)或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如图所示:
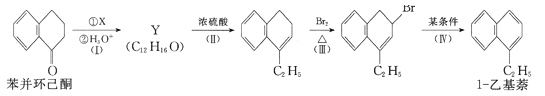
已知: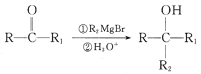
回答下列问题:
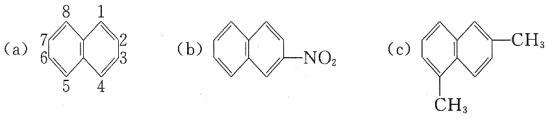
(1)萘环上的碳原子的编号如(a)式,根据系统命名法,(b)式可称为2-硝基萘,则化合物(c)的名称应是__。
(2)有机物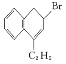 含有的官能团是__(填名称),X的结构简式是__。
含有的官能团是__(填名称),X的结构简式是__。
(3)步骤III的反应类型是__,步骤IV的反应类型是__。
(4)反应II的化学方程式是__。
(5)1-乙基萘的同分异构体中,属于萘的取代物的有__种(不含1-乙基蔡)。W也是1-乙基萘的同分异构体,它是含一种官能团的苯的取代物,核磁共振氢谱显示W有3种不同化学环境的氢,峰面积比为1:1:2,W的结构简式为__。
(6)写出用CH3COCH3和CH3MgBr为原料制备 的合成路线(其他试剂任选)。__。
的合成路线(其他试剂任选)。__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·![]() 。请回答下列问题:
。请回答下列问题:
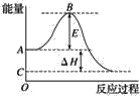
(1)图中A、C分别表示__,E的大小对该反应的反应热__(填“有”或“无”)影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点__(填“升高”或“降低”),ΔH__(填“变大”“变小”或“不变”)。
(2)图中ΔH=__kJ·![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的密闭容器中存在如下反应A(g)+3B(g)2C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出下列关系曲线(如图):
Ⅰ.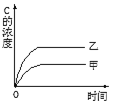 Ⅱ.
Ⅱ.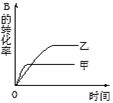 Ⅲ.
Ⅲ.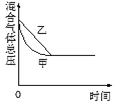
下列判断正确的是( )
①图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
②图Ⅱ研究的是压强对反应的影响,且甲的压强较高
③图Ⅱ研究的是温度对反应的影响,且甲的温度较高
④图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂的效率较高
A.①②B.①③C.②③D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com