
【题目】辉钼矿主要含MoS2,还含有Ca、Si、Cu、Zn、Fe等元素。利用辉钼矿制备仲钼酸铵的新一代清洁生产工艺如下图所示:
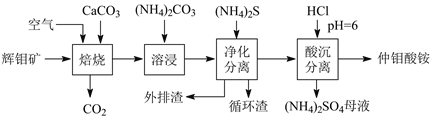
回答下列问题:
(1)焙烧温度为400℃,MoS2转化为CaMoO4和CaSO4,则反应中每摩MoS2转移的电子数为_________。仲钼酸铵(七钼酸铵)中的阴离子是Mo7O24n-,则n=_______。
(2)传统焙烧是在650℃下,使MoS2直接与空气中的O2反应生成MoO3和SO2。图示清洁生产工艺加入CaCO3的优点是______________。
(3)溶浸时,CaMoO4发生复分解反应的化学方程式是___________。循环渣的主要成分是CaCO3,则外排渣主要是________和Cu、Zn、Fe的硫化物。
(4)已知:常温下Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=9.1×10-6。在(NH4)2SO4母液中添加循环渣(CaCO3),可以使硫酸铵转化为碳酸铵(返回溶浸循环使用),原因是_______。
(5)电氧化分解钼精矿时,用惰性电极电解钼精矿和NaCl的混合浆液,电解槽无隔膜,控制溶液pH=9。阴极生成物为________,混合浆液中,阳极产物转化生成的NaClO氧化MoS2生成MoO42-和SO42-的离子方程式是______________。
【答案】18mol或18NA 6 能耗低,无SO2排放造成的环境污染 CaMoO4+(NH4)2CO3 = (NH4)2MoO4+CaCO3 SiO2 硫酸铵溶液中NH4+水解显酸性,促进CaCO3溶解 H2(或氢气) 9ClO-+MoS2+6OH- = MoO42-+2SO42-+9Cl-+3H2O
【解析】
辉钼矿与碳酸钙混合在空气中焙烧,MoS2转化为CaMoO4和CaSO4,其他杂质元素转化为相应的氧化物,之后溶浸并加入碳酸铵,CaMoO4与(NH4)2CO3发生复分解反应转化为(NH4)2MoO4和碳酸钙,硫酸钙转化为碳酸钙,再加入硫化铵得到杂质金属元素的硫化物沉淀以及SiO2,分离沉淀,其中碳酸钙可循环使用;之后向滤液中加入HCl调节pH为6得到仲钼酸铵沉淀。
(1)MoS2中S为-1价,Mo为+2价,产物CaMoO4和CaSO4中Mo为+6价,S为+6价,MoS2中各元素共升高18价,所以反应中每摩MoS2转移的电子数为18NA;Mo7O24n-中Mo为+6价,O为-2价,所以n=2×24-7×6=6;
(2)传统焙烧温度高,能耗高,产生污染物SO2,图示流程焙烧温度400℃,能耗较低,且无SO2排放造成的环境污染;
(3)溶浸时加入的物质为(NH4)2CO3,根据复分解反应的特点可知方程式应为CaMoO4+(NH4)2CO3 = (NH4)2MoO4+CaCO3;辉钼矿中的杂质元素有Ca、Si、Cu、Zn、Fe等,焙烧时杂质元素生成相应的氧化物,溶浸后Ca最终转化为碳酸钙沉淀,溶浸后又加入硫化铵,所以Cu、Zn、Fe转化为相应的硫化物沉淀,SiO2不溶于酸,所以外排渣主要是SiO2和Cu、Zn、Fe的硫化物;
(4)硫酸铵溶液中NH4+水解显酸性,促进CaCO3溶解,所以在(NH4)2SO4母液中添加循环渣(CaCO3),可以使硫酸铵转化为碳酸铵;
(5)电解槽无隔膜,所以电解时阴极水电离出的氢离子放电生成氢气;阳极氯离子放电生成氯气,溶液显碱性,氯气反应生成次氯酸根,NaClO氧化MoS2生成MoO42-和SO42-,MoS2整体化合价升高18价,ClO-转化为Cl-降低2价,结合电子守恒和元素守恒可得离子方程式为:9ClO-+MoS2+6OH-= Mo42-+2SO42-+9Cl-+3H2O。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】(1)物质的量各为0.1mol钠、镁、铝单质,分别投入足量盐酸溶液中,生成相同条件下氢气的体积比为___。
(2)物质的量各为0.2mol的铝、铁、锌,分别与100ml1mol/L的硫酸溶液反应,生成相同条件下氢气的体积比为___。
(3)等质量的两份铝分别与足量的盐酸溶液和氢氧化钠溶液反应,消耗盐酸和氢氧化钠的物质的量比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是( )
A.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.试剂X可以是氢氧化钠溶液,也可以是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如下图所示。
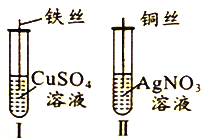
回答下列问题:
(1)写出AgNO3的电离方程式__________________________。
(2)已知实验Ⅰ、Ⅱ的现象和结论如下表:
实验编号 | 实验现象 | 实验结论 |
Ⅰ | ① | 氧化性:Cu2+>Fe2+ |
Ⅱ | 溶液变蓝色 | ② |
①实验Ⅰ的现象是_____________________
②实验Ⅱ的结论是______________________________。
③写出实验Ⅱ的离子方程式______________________________。
(3)Cu、Fe、CuSO4溶液、AgNO3溶液均能导电,其中属于纯净物有_________种,CuSO4溶液、AgNO3溶液均能导电的原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g) ![]() 2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是
2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1。对此反应速率的正确表示是
A. 用A表示的反应速率是0.8 mol·L-1·s-1
B. 分别用B、C、D表示反应的速率,其比值是3∶1∶2
C. 在2 min末时的反应速率,用产物C来表示是0.2mol·L-1·min-1
D. 在这2 min内用B和C表示的反应速率的值都是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活中的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
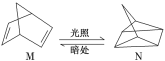
ΔH=+88.6 kJ/mol则M、N相比,较稳定的是_____________。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+12O2(g)=CO2(g)+2H2(g) ΔH=-a kJ/mol,则a________238.6(填“>”“<”或“=”)。
(3)将Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:__________________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是________(填原子或分子)晶体,31 g白磷与足量的氧气完全燃烧释放出745.5 kJ的热量,请写出白磷燃烧的热化学反应方程式:______________________________________。
(2)已知白磷和氯酸溶液可发生如下反应:________P4+___HClO3+___ ______→____HCl+____H3PO4,配平并完成上述反应方程式______________,该反应的氧化剂是___________。
(3)白磷有毒,实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O==20Cu3P+24H3PO4+60H2SO4,该反应的氧化产物是________,若有11 mol P4反应,则有________ mol电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3molA气体和1.5molB气体在3L的容器中混合并在一定条件发生如下反应: 2A(g)+B(g) ![]() 2C(g)。经2s后测得C的浓度为0.3mol/L,则下列计算正确的是:
2C(g)。经2s后测得C的浓度为0.3mol/L,则下列计算正确的是:
①用A表示的平均反应速率为0.3mol/(L·s)
②2s时物质A的浓度为0.7mol/L
③用B表示的平均反应速率为0.15mol/(L·s)
④2s时物质B的转化率为30%
A.②④B.①④C.②③D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,NO跟![]() 可以发生反应:
可以发生反应:![]() ,关于该反应下列说法中不正确的是()
,关于该反应下列说法中不正确的是()
A.![]() 既不是氧化产物也不是还原产物
既不是氧化产物也不是还原产物
B.该反应中被氧化和被还原的氮元素的质量比是2:3
C.若有![]() 完全反应,共转移12mol电子
完全反应,共转移12mol电子
D.NO是氧化剂,![]() 是还原剂
是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com