
【题目】科学研究发现,具有高度对称的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为化学界关注的热点。立体烷烃中有一系列对称结构的烃,如:![]() (正四面体烷C4H4)、
(正四面体烷C4H4)、![]() (棱晶烷C6H6)、
(棱晶烷C6H6)、![]() 立方烷C8H8)等,下列有关说法正确的是
立方烷C8H8)等,下列有关说法正确的是
A. 立体烷烃的C原子都形成4个单键,因此它们都属于烷烃
B. 上述一系列物质互为同系物,它们的通式为C2nH2n(n≥2)
C. 棱晶烷与立方烷中碳原子均为饱和碳原子,其二氯代物的种数不同
D. 苯、盆烯(![]() )与棱晶烷属于同分异构体
)与棱晶烷属于同分异构体
【答案】D
【解析】
A. 立体烷烃中有一系列对称结构的烃,如:![]() (正四面体烷C4H4)、
(正四面体烷C4H4)、![]() (棱晶烷C6H6)、
(棱晶烷C6H6)、![]() 立方烷C8H8)等,立体烷烃的C与碳原子之间都形成3个单键,还有一条C与H形成的共价键,它们都属于环烷烃,故A错误;
立方烷C8H8)等,立体烷烃的C与碳原子之间都形成3个单键,还有一条C与H形成的共价键,它们都属于环烷烃,故A错误;
B. ![]() (正四面体烷C4H4)、
(正四面体烷C4H4)、![]() (棱晶烷C6H6)、
(棱晶烷C6H6)、![]() 立方烷C8H8),他们不属于同系物,故B错误;
立方烷C8H8),他们不属于同系物,故B错误;
C. 棱晶烷二氯代物的同分异构体有三种,立方烷的二氯代物的同分异构体也有三种,所以棱晶烷与立方烷中碳原子均为饱和碳原子,其二氯代物的种数相同,故C错误;
D.苯分子式为C6H6、盆烯(![]() )分子式为C6H6;棱晶烷分子式为C6H6,所以他们属于同分异构体,故D正确;
)分子式为C6H6;棱晶烷分子式为C6H6,所以他们属于同分异构体,故D正确;
所以答案:D。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】科学家模仿植物的光合作用,开发出了利用太阳光、水及二氧化碳(CO2)合成甲烷(CH4)的人工光合系统,其工作原理如图所示。下列说法错误的是( )
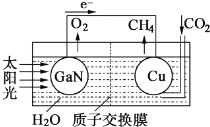
A. GaN为负极,Cu为正极 B. 该装置中只存在两种能量的转化
C. GaN电极的电极反应式为2H2O-4e-=4H++O2↑ D. 该装置工作时,H+向Cu电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)计算在0.2 g H2中含有____个H原子,2 mol CO(NH2)2中含___mol C,___mol N,___mol H,标准状况下,44.8 L O2的体积为___mol。
(2) 2.3 g Na中含___mol e-,在与足量水反应中产生标准状况下的H2___L。
(3) 0.4 mol Al2(SO4)3的溶液中,含__mol SO42—,Al3+物质的量__0.8 mol(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒被誉为“合金的维生素”。从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示:

已知:
步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)![]() RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)
回答下列问题:
(1)步骤D酸浸过程中发生氧化还原反应的化学方程式为______________________。
(2)萃取时应加入适量碱的作用是___________________。
(3)步骤④中反应的离子方程式为___________________。
(4)步骤⑤加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<_____mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。所得NH4VO3为离子化合物,NH4+的电子式为_______。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为V0+,则V2O5与氢碘酸反应的离子方程式为_________________。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=_______mol/L(萃取的量=![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中的NO3对人类健康会产生危害,为了降低饮用水中NO3的浓度,可以在碱性条件下用铝粉将NO3还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,被氧化的元素_________,还原产物是________。
(2)用“双线桥法”表示反应中电子转移的方向和数目:_______________。
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(3)反应中每生成标况下22.4L N2,转移_______mol电子。
(4)请配平下列离子方程式。
____Fe2++____H+ +____NO3=____Fe3+ +____N2O↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,分布在三个不同周期。X、Y、Z、W为这些元素形成的化合物,X为二元化合物且为强电解质,W的水溶液呈碱性,物质的转化关系如图所示。下列说法中正确的是
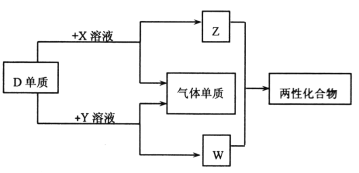
A. 对应的简单离子半径:C>D>B
B. D、E形成的化合物为含有极性共价键的共价化合物
C. 电解C、E形成的化合物水溶液,可生成C、E对应的单质
D. 由A、B、E形成的化合物都含有共价键,溶液都呈强酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.配制480 mL 0.2mol/L NaOH溶液。具体如下:
(1)需______gNaOH。
(2)配制过程中,下列仪器不会用到的是__________(填序号),尚缺少的玻璃仪器是______________。
A.托盘天平 B.250mL容量瓶 C.玻璃棒 D.胶头滴管
(3)实验过程中两次用到玻璃棒,其作用分别是:______________、_________。
(4)定容操作:将蒸馏水注入所选的容器中,直到其中液面接近其刻度线____________处时,改用____________滴加蒸馏水至溶液的__________正好与刻度线_______。将瓶塞子盖好,反复____________摇匀。
(5)下列操作的正确顺序是(用字母表示)B→_____→________→______→__________→_____→G。
A.转移 B.称量 C.定容 D.洗涤 E.冷却 F.溶解 G.摇匀
II.乙同学用18.4mol/l浓硫酸配制100ml 3.6mol/L的稀硫酸。
用100 ml 量筒量取20 ml 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 ml 刻度线,再搅拌均匀。
指出其中错误之处____________________________。
III.在配制一定物质的量浓度溶液时,下列操作出现的后果是(填:“偏低”.“偏高”.“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。_____________。
(2)配制氢氧化钠溶液时,容量瓶中有少量水。______________。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度____________。
(4)转移时不慎将溶液倒在瓶外;____________;
(5)定容时俯视容量瓶刻度线:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(NOx)是大气污染物之一。工业上在一定的温度和催化剂条件下,可用NH3来消除NOx的污染,生成两种对环境无害的物质。
(1)请写出NH3与NO2反应的化学方程式____。
(2)①写出实验室中由固体物质制取氨气的化学方程式__;
②欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为:发生装置→____(按气流方向,用小写字母表示)
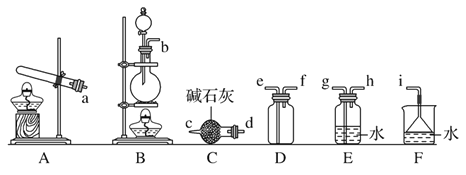
(3)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。若用NO2气体进行模拟电解法吸收实验。

①写出电解时NO2发生反应的电极反应式:___。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒元素(Se)是第4周期ⅥA族元素,单质有红硒、黑硒和灰硒,灰硒是良好的半导体材料,硒最特殊的性质是在光照射下导电性可提高近千倍,可用于制造光电管。请回答下列问题:
(1)基态Se原子价电子的轨道表示式为__。
(2)As和Se是同一周期元素,As的第一电离能比Se大,原因是___。
(3)硒在空气中燃烧能生成SeO2,常温下,SeO2是易挥发的白色固体,熔点为340~350℃,315℃时升华,则SeO2固体是___晶体;写出一种与SeO2互为等电子体的阴离子的化学式__。
(4)H2SeO4和H2SO4相似,是一种不易挥发的强酸。SeO42-的空间构型为___,中心原子的杂化方式为___。
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,Zn原子的配位数为___,若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1,用NA代表阿伏加德罗常数,则晶胞参数a(即晶胞的边长)为___nm。
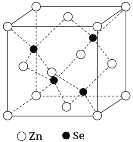
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com