
ЎҫМвДҝЎҝФЪCl-ЕЁ¶ИОӘ0.5 molЎӨLЈӯ1өДДіОЮЙ«іОЗеИЬТәЦРЈ¬»№ҝЙДЬә¬УРПВұнЦРөДИфёЙЦЦАлЧУЎЈ
СфАлЧУ | KЈ« ЎЎAgЈ«ЎЎ Mg2Ј« ЎЎBa2Ј« Fe3+ |
ТхАлЧУ | NO3-ЎЎ CO32- ЎЎSiO32- ЎЎSO42- |
МбКҫЈәSiO32-Ј«2HЈ«=H2SiO3Ўэ(H2SiO3КЗ°ЧЙ«іБөн)ЎўH2SiO3![]() SiO2Ј«H2O
SiO2Ј«H2O
ПЦИЎёГИЬТә100 mLҪшРРИзПВКөСй(ЖшМеМе»эҫщФЪұкЧјЧҙҝцПВІв¶Ё)ЎЈ
РтәЕ | КөСйДЪИЭ | КөСйҪб№ы |
ўс | ПтёГИЬТәЦРјУИлЧгБҝПЎСОЛб | ІъЙъ°ЧЙ«іБөнІў·ЕіцұкЧјЧҙҝцПВ0.56 LЖшМе |
ўт | Ҫ«ўсөД·ҙУҰ»мәПТә№эВЛЈ¬¶ФіБөнПҙөУЎўЧЖЙХЦБәгЦШЈ¬іЖБҝЛщөГ№ММеЦКБҝ | №ММеЦКБҝОӘ2.4 g |
ўу | ПтўтөДВЛТәЦРөОјУBaCl2ИЬТә | ОЮГчПФПЦПу |
Зл»ШҙрПВБРОКМвЎЈ
(1)НЁ№эТФЙПКөСйДЬИ·¶ЁТ»¶ЁІ»ҙжФЪөДСфАлЧУКЗ______Ј¬Т»¶ЁІ»ҙжФЪөДТхАлЧУКЗ________ЎЈ
(2)НЁ№эКөСйўсЎўўтЎўўуәНұШТӘјЖЛгЈ¬ЗлРҙіцТ»¶ЁҙжФЪөДТхАлЧУј°ЖдЕЁ¶И(І»Т»¶ЁТӘМоВъ)
ТхАлЧУ | ўЩ___ | ўЪ___ | ||
c/molЎӨLЈӯ1 | ____ | ___ |
(3)ЕР¶ПKЈ«КЗ·сҙжФЪЈ¬ИфҙжФЪЗуЖдЧоРЎЕЁ¶ИЈ¬ИфІ»ҙжФЪЛөГчАнУЙЈә_______________ЎЈ
Ўҫҙр°ёЎҝAgЈ«ЎўMg2Ј«ЎўBa2Ј«ЎўFe3+ SO42- CO32- SiO32- 0.25 0.4 ҙжФЪЈ¬ЧоРЎЕЁ¶ИОӘ1.8molЎӨLЈӯ1
ЎҫҪвОцЎҝ
УЙМвТвЦӘИЬТәОӘОЮЙ«іОЗеИЬТәЈ¬Т»¶ЁІ»ә¬Fe3+Ј¬ЗТИЬТәЦРә¬УРөДАлЧУұШРлДЬҙуБҝ№ІҙжЈ®УЙКөСйўсҝЙЦӘЈ¬ёГИЬТәЦРТ»¶Ёә¬УРCO32-Ј¬ЖдЕЁ¶ИОӘ![]() ==0.25mol/LЈ¬ФтТ»¶ЁГ»УРAg+ЎўMg2+ЎўBa2+Ј»УЙЙъіЙ°ЧЙ«іБөнЕР¶ПИЬТәЦРТ»¶Ёә¬УРSiO32-Ј¬·ўЙъ·ҙУҰSiO32-+2H+=H2SiO3ЎэЈ¬SiO32-өДЕЁ¶ИОӘ
==0.25mol/LЈ¬ФтТ»¶ЁГ»УРAg+ЎўMg2+ЎўBa2+Ј»УЙЙъіЙ°ЧЙ«іБөнЕР¶ПИЬТәЦРТ»¶Ёә¬УРSiO32-Ј¬·ўЙъ·ҙУҰSiO32-+2H+=H2SiO3ЎэЈ¬SiO32-өДЕЁ¶ИОӘ![]() ==0.4mol/LЈ®УЙКөСйўуҝЙЦӘИЬТәЦРІ»ә¬SO42-Ј¬ёщҫЭөзәЙКШәг2cЈЁCO32-Ј©+2cЈЁSiO32-Ј©+cЈЁCl-Ј©=2ЎБ0.25mol/L+2ЎБ0.4mol/L+0.5molL-1=1.8mol/LЈ¬ТтҙЛИЬТәЦРТ»¶Ёә¬УРK+Ј¬ЗТЖдЕЁ¶ИЦБЙЩОӘ1.8mol/LЈ¬І»ДЬИ·¶ЁNO3-КЗ·сҙжФЪЈ¬ТФҙЛАҙҪвҙрЎЈ
==0.4mol/LЈ®УЙКөСйўуҝЙЦӘИЬТәЦРІ»ә¬SO42-Ј¬ёщҫЭөзәЙКШәг2cЈЁCO32-Ј©+2cЈЁSiO32-Ј©+cЈЁCl-Ј©=2ЎБ0.25mol/L+2ЎБ0.4mol/L+0.5molL-1=1.8mol/LЈ¬ТтҙЛИЬТәЦРТ»¶Ёә¬УРK+Ј¬ЗТЖдЕЁ¶ИЦБЙЩОӘ1.8mol/LЈ¬І»ДЬИ·¶ЁNO3-КЗ·сҙжФЪЈ¬ТФҙЛАҙҪвҙрЎЈ
ЈЁ1Ј©(1)НЁ№эТФЙПКөСйДЬИ·¶ЁТ»¶ЁІ»ҙжФЪөДСфАлЧУКЗAgЈ«ЎўMg2Ј«ЎўBa2Ј«ЎўFe3+Ј¬Т»¶ЁІ»ҙжФЪөДТхАлЧУКЗSO42-Ј»
ҙр°ёЈәAgЈ«ЎўMg2Ј«ЎўBa2Ј«ЎўFe3+ SO42-
ЈЁ2Ј©УЙЙПКц·ЦОцҝЙЦӘЈ¬cЈЁCO32-Ј©=0.25mol/LЈ¬cЈЁSiO32-Ј©=0.4mol/LЈ¬
ҙр°ёЈәCO32- SiO32- 0.25 0.4
ЈЁ3Ј©УЙ2cЈЁCO32-Ј©+2cЈЁSiO32-Ј©+cЈЁCl-Ј©=2ЎБ0.25mol/L+2ЎБ0.4mol/L+0.5molL-1=1.8mol/LЈ¬ёщҫЭөзәЙКШәгҝЙЦӘИЬТәЦРТ»¶Ёә¬УРK+Ј¬ЗТЖдЕЁ¶ИЦБЙЩОӘ1.8mol/LЈ¬
ҙр°ёЈәҙжФЪЈ¬ЧоРЎЕЁ¶ИОӘ1.8molЎӨLЈӯ1


 МмМмПтЙПТ»ұҫәГҫнПөБРҙр°ё
МмМмПтЙПТ»ұҫәГҫнПөБРҙр°ё РЎС§Йъ10·ЦЦУУҰУГМвПөБРҙр°ё
РЎС§Йъ10·ЦЦУУҰУГМвПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЕрЗв»ҜГМ![]() ҝЙТФУГЧчҙўЗвІДБПЈ¬ТІДЬУГУЪҝЖС§СРҫҝЎЈТФё»ГМФь(ә¬60% MnOЈ¬»№ә¬УРSiO2ЎўAl2O3ЎўCaOЎўFeO)ОӘФӯБПЦЖұёЕрЗв»ҜГМөД№ӨТХБчіМИзПВЎЈ
ҝЙТФУГЧчҙўЗвІДБПЈ¬ТІДЬУГУЪҝЖС§СРҫҝЎЈТФё»ГМФь(ә¬60% MnOЈ¬»№ә¬УРSiO2ЎўAl2O3ЎўCaOЎўFeO)ОӘФӯБПЦЖұёЕрЗв»ҜГМөД№ӨТХБчіМИзПВЎЈ
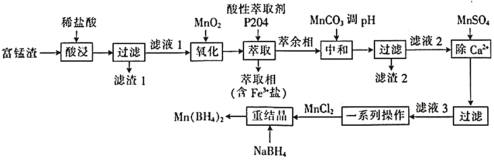
ТСЦӘјёЦЦЗвСх»ҜОпөДKsp өДЦөИзПВұнЈә
ЗвСх»ҜОп |
|
|
|
|
Ksp |
|
|
|
|
Зл»ШҙрПВБРОКМвЈә
(1) NaBH4ЦРBөД»ҜәПјЫОӘ________јЫЎЈ
(2)ПВБРОпЦКЦРУлВЛФь1І»·ўЙъ·ҙУҰ(ёЯОВ»тіЈОВПВ)өДКЗ________(МоЧЦДё)ЎЈ
AЈ®ЕЁПхЛб BЈ®ЗвСх»ҜДЖИЬТә CЈ®МјЛбДЖ DЈ®Зв·ъЛб
(3)Ў°Сх»ҜЎұЦР·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ________________Ј¬ёГ·ҙУҰЦРСх»ҜРФЈә![]() ________(МоЎ°
________(МоЎ°![]() Ўұ»тЎ°
Ўұ»тЎ°![]() Ўұ) MnO2ЎЈ
Ўұ) MnO2ЎЈ
(4)Ў°ЦРәНЎұКұЈ¬өчҪЪpHФјОӘ________ЎЈ(өұИЬТәЦРөДАлЧУЕЁ¶ИРЎУЪ![]() КұЈ¬іБөнҙпөҪНкИ«Ј¬Ҫб№ыұЈБф2О»УРР§КэЧЦ)
КұЈ¬іБөнҙпөҪНкИ«Ј¬Ҫб№ыұЈБф2О»УРР§КэЧЦ)
(5) Mn(BH4)2ДЬУлПЎСОЛб·ҙУҰЙъіЙH3BO3Ј¬ёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘ________________ЎЈ
(6)Ів¶Ёё»ГМФьЦРМъөДә¬БҝЈәИЎ20gё»ГМФьЈ¬ҫӯ№эЙПКцЎ°ЛбҪюЎұЎ°№эВЛЎұЎ°Сх»ҜЎұЎ°ЭНИЎЎұәуЈ¬Ҫ«ЭНИЎПа(јЩЙиFe3+span>И«Іҝұ»ЭНИЎ)ЧӘИлЙХұӯЦРЈ¬јУИлЧгБҝПЎБтЛбЈ¬ід·Ц·ҙУҰәуҫІЦГЎў·ЦТәЈ¬ФЩПтә¬Fe3+өДИЬТәЦРјУИлЧгБҝKIЈ¬ід·Ц·ҙУҰәуЈ¬Ҫ«ИЬТәЕдЦЖіЙ500mLЈ¬ИЎ25mLУЪЧ¶РОЖҝЦРІўјУИлөн·ЫЦёКҫјБЈ¬ЧоәуУГ![]() өДNa2S2O3ұкЧјТәөО¶ЁЈ¬ҪшРРИэҙОЖҪРРКөСйЈ¬ІвөГПыәДNa2S2O3ұкЧјТәөДМе»эИзұнЛщКҫЎЈ
өДNa2S2O3ұкЧјТәөО¶ЁЈ¬ҪшРРИэҙОЖҪРРКөСйЈ¬ІвөГПыәДNa2S2O3ұкЧјТәөДМе»эИзұнЛщКҫЎЈ
КөСйҙОКэ | 1 | 2 | 3 |
Na2S2O3ұкЧјТәМе»э/ | 23.20 | 24.80 | 25.20 |
ТСЦӘЈәI2+2Na2S2O3==2NaI+Na2S4O6
ўЩөО¶ЁҙпөҪЦХөгКұИЬТәөДСХЙ«ұд»ҜОӘ________ЎЈ
ўЪё»ГМФьЦРМъөДә¬БҝОӘ________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝijѧУКөСйРЎЧйУыМҪҫҝБт·ЫУлМъ·ЫөД·ҙУҰЈ¬ІўСйЦӨ·ҙУҰәуөДІъОпЦРМъФӘЛШөД»ҜәПјЫЈ¬ИзНјКЗМъ·ЫәНБт·Ы·ҙУҰөДЧ°ЦГНјЎЈ
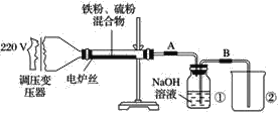
(1)Ҫ«Бт·ЫәНМъ·Ы°ҙОпЦКөДБҝЦ®ұИ1ЎГ1ід·Ц»мәПЎЈ
(2)°ҙЧ°ЦГНјҪ«ТЗЖчБ¬ҪУәГЎЈ
(3)____________ЎЈ
(4)Ҫ«»мәПОпҫщФИөШ·ЕФЪУІЦКІЈБ§№ЬДЪЎЈ
(5)ҪУНЁөзФҙЈ¬Ҫ«өзС№ЦёКҫЕМөчөҪ35 VЈ¬өзВҜЛҝәЬҝмұдәмЈ¬ІўТэ·ўЧуұЯ»мәПОп·ўЙъ·ҙУҰЎЈ№ШұХөзФҙЎЈ
(6)Ҫ«·ҙУҰәуөД»мәПОпАдИҙәујУИлПЎБтЛбЦРЈ¬И»әуИЎЙПІгЗеТәөОјУБтЗиЛбјШИЬТәСйЦӨІъОпЦРМъФӘЛШөД»ҜәПјЫЎЈ
ЈЁЛјҝјМҪҫҝЈ©
(1)ІҪЦи(3)ЦРИұЙЩөДКөСйІЩЧчКЗКІГҙЈҝ____ЎЈ
(2)№ШұХөзФҙәуЈ¬·ҙУҰИФјМРшҪшРРөДФӯТтКЗКІГҙЈҝ_____________ЎЈ
(3)Ҫ«КўУРNaOHИЬТәөДЖҝЦРAЎўBөј№ЬО»ЦГ·ҙҪУКЗ·сҝЙТФЈҝОӘКІГҙЈҝ______________ЎЈ
(4)ДіН¬С§ИПОӘЈ¬ИфFe·ЫУлS·Ы·ҙУҰІъОпЦРМъФӘЛШөД»ҜәПјЫКЗЈ«2јЫЈ¬ФтЙПКцІҪЦи(6)ЦРөДИЬТәІ»ұдәмЈ¬ДгИПОӘЛыөДЛө·ЁХэИ·ВрЈҝ__________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝјЧҙјКЗТ»ЦЦҝЙФЩЙъДЬФҙЈ¬ҫЯУР№г·әөДҝӘ·ўәНУҰУГЗ°ҫ°ЎЈ№ӨТөЙПТ»°гІЙУГПВБРБҪЦЦ·ҙУҰәПіЙјЧҙјЎЈ
·ҙУҰўсЈәCO(g)+2H2(g) ![]() CH3OH(g)Ј¬ЎчH1
CH3OH(g)Ј¬ЎчH1
·ҙУҰўтЈәC02(g)+3H2(g) ![]() CH30H(g)+ H2O(g)Ј¬ЎчH2
CH30H(g)+ H2O(g)Ј¬ЎчH2
ПВұнЛщБРКэҫЭКЗ·ҙУҰIФЪІ»Н¬ОВ¶ИПВөД»ҜС§ЖҪәвіЈКэ(K)Јә
ОВ¶И | 250Ўж | 300Ўж | 350Ўж |
K | 2.O | 0.27 | 0.012 |
ЈЁ1Ј©УЙұнЦРКэҫЭЕР¶ПЎчH1_____0(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°=Ўұ)·ҙУҰЈ¬C02(g)+H2(g)![]() CO(g)+H20(g) ЎчH3=____(УГЎчH1әНЎчH2ұнКҫ)ЎЈ
CO(g)+H20(g) ЎчH3=____(УГЎчH1әНЎчH2ұнКҫ)ЎЈ
ЈЁ2Ј©ИфИЭЖчИЭ»эІ»ұдЈ¬ПВБРҙлК©ҝЙМбёЯ·ҙУҰўсЦРCOЧӘ»ҜВКөДКЗ_________(СЎЧЦДё)ЎЈ
aЈ®ідИлCOЈ¬К№МеПөЧЬС№ЗҝФцҙу
bЈ®Ҫ«CH3OH(g)ҙУМеПөЦР·ЦАл
eЈ®ідИлHeЈ¬К№МеПөЧЬС№ЗҝФцҙу
dЈ®К№УГёЯР§ҙЯ»ҜјБ
ЈЁ3Ј©Рҙіц·ҙУҰўтөД»ҜС§ЖҪәвіЈКэұнҙпКҪЈәK=_________Ј»ұЈіЦәгОВәгИЭөДМхјюПВҪ«·ҙУҰўтөДЖҪәвМеПөёчОпЦКЕЁ¶ИҫщФцјУТ»ұ¶Ј¬Фт»ҜС§ЖҪәв_________(МоЎ°ХэПтЎұЎўЎ°ДжПтЎұ»тЎ°І»Ўұ)ТЖ¶ҜЈ¬ЖҪәвіЈКэK____(МоЎ°ұдҙуЎұЎўЎ°ұдРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҫЫхЈСЗ°·КЗТ»Аа·ЗіЈУРЗ°ҫ°өДҝЙҪөҪвДӨІДБПЈ¬ЖдЦРТ»ЦЦДӨІДБПQөДәПіЙВ·ПЯИзПВЎЈ
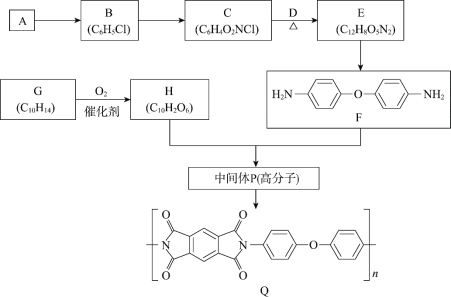
ТСЦӘЈәiЈ®![]() +
+![]()
![]()
![]() +
+![]()
iiЈ®![]() +NaOH
+NaOH![]()
![]() +
+![]()
(1)AКЗ·јПгМюЈ¬A![]() BөД»ҜС§·ҪіМКҪКЗ________ЎЈ
BөД»ҜС§·ҪіМКҪКЗ________ЎЈ
(2)BЧӘ»ҜОӘCөДКФјБәНМхјюКЗ________ЎЈ
(3)CЦРЛщә¬өД№ЩДЬНЕөДГыіЖКЗ________ЎЈ
(4)DҝЙУЙCУлKOHИЬТә№ІИИАҙЦЖұёЈ¬CУлD·ҙУҰЙъіЙEөД»ҜС§·ҪіМКҪКЗ________ЎЈ
(5)E![]() FөД·ҙУҰАаРНКЗ________ЎЈ
FөД·ҙУҰАаРНКЗ________ЎЈ
(6)GУлA»ҘОӘН¬ПөОпЈ¬әЛҙЕ№ІХсЗвЖЧУР2Чй·еЈ¬G![]() HөД»ҜС§·ҪіМКҪКЗ________ЎЈ
HөД»ҜС§·ҪіМКҪКЗ________ЎЈ
(7)HУлFЙъіЙЦРјдМеPөДФӯЧУАыУГВКОӘ100%Ј¬PөДҪб№№јтКҪКЗ________(РҙТ»ЦЦ)ЎЈ
(8)·ПЖъөДДӨІДБПQУГNaOHИЬТәҙҰАнҪөҪвәуҝЙ»ШКХөГөҪFәН_______(МоҪб№№јтКҪ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРКэҫЭ»тКВКөЛщіКПЦөД№жВЙІ»ДЬУГФӘЛШЦЬЖЪВЙҪвКНөДКЗ
A. B.
B.
C.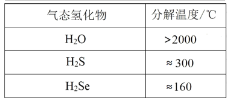 D.
D.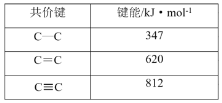
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіОВ¶ИПВЈ¬ФЪТ»ёц2LөДГЬұХИЭЖчЦРЈ¬јУИл4molAәН 2molBҪшРРИзПВ·ҙУҰЈә3A(g)Ј«2B(g)![]() 4C(s)Ј«2D(g)ЎЈ·ҙУҰТ»¶ОКұјдәуҙпөҪЖҪәвЈ¬ІвөГЙъіЙ1.6molCЈ¬ФтПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
4C(s)Ј«2D(g)ЎЈ·ҙУҰТ»¶ОКұјдәуҙпөҪЖҪәвЈ¬ІвөГЙъіЙ1.6molCЈ¬ФтПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A.ёГ·ҙУҰөД»ҜС§ЖҪәвіЈКэұнҙпКҪКЗ K=![]()
B.ҙЛКұЈ¬BөДЖҪәвЧӘ»ҜВККЗ40%
C.ФцҙуёГМеПөөДС№ЗҝЈ¬ЖҪәвПтУТТЖ¶ҜЈ¬»ҜС§ЖҪәвіЈКэФцҙу
D.ФцјУ BЈ¬ЖҪәвПтУТТЖ¶ҜЈ¬BөДЖҪәвЧӘ»ҜВКФцҙу
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪКўУР1L0.1mol/LCuSO4ИЬТәөДҙуЙХұӯЦРЈ¬УГРҝЎўНӯЧчөзј«Ј¬УГөјПЯБ¬ҪУРОіЙФӯөзіШЈ¬өұөзј«РҝПыәД3.25gКұЈ¬КФНкіЙЈә
ЈЁ1Ј©Рҙіцөзј«·ҙУҰКҪЈәёәј«__________________Ј»Хэј«____________ЎЈ
ЈЁ2Ј©өзј«ЙПОціцНӯөДЦКБҝЎЈ__________________
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘ ЎЈКТОВПВУГ
ЎЈКТОВПВУГ![]() өД
өД![]() өО¶Ё
өО¶Ё![]() ДіТ»ФӘЛб
ДіТ»ФӘЛб![]() өДҪб№ыИзНјЛщКҫЈ¬ПВБРЛө·ЁЦРХэИ·өДКЗ
өДҪб№ыИзНјЛщКҫЈ¬ПВБРЛө·ЁЦРХэИ·өДКЗ

A. ![]() КфУЪИхЛб
КфУЪИхЛб
B. Хыёц№эіМЦРЈ¬![]() өгКұЛ®өДөзАліМ¶ИЧоҙу
өгКұЛ®өДөзАліМ¶ИЧоҙу
C. ![]() өг¶ФУҰТәЦР
өг¶ФУҰТәЦР![]()
D. ![]() өДКэБҝј¶ОӘ
өДКэБҝј¶ОӘ![]()
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com