
【题目】如图是第三周期主族元素(11~17号)某些性质变化趋势的柱形图,下列有关说法中正确的是( )
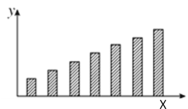
A. 若X轴为原子序数,y轴表示的可能是第一电离能
B. 若X轴为原子序数,y轴表示的可能是原子半径
C. 若X轴为最高正化合价,y轴表示的可能是电负性
D. 若X轴为族序数,y轴表示的可能是0.1mol/L最高价氧化物对应水化物溶液的pH
【答案】C
【解析】
A.对于第三周期11~17号元素,随着原子序数的增大,第一电离能呈现增大的趋势,但Mg和P特殊,其价电子分别为3s1和3s2sp3,s1和p3为半充满,因而稳定,第一电离能会大于相邻的两个原子的第一电离能,A错误;
B.同周期时,原子半径随原子序数增大而依次减小,与图显示的趋势矛盾,B错误;
C.对于第三周期,最高正化合价随原子序数增大而依次增大,而电负性在同周期时随原子序数增大而依次增大,因而X轴为最高正化合价,y轴表示的可能是电负性,C正确;
D.对于第三周期,主族序数随原子序数增大而依次增大,而最高价氧化物对应水化物碱性在同周期时随原子序数增大而依次减弱,即最高价氧化物对应水化物碱性在同周期时随主族序数依次减弱,例如NaOH的碱性强于Al(OH)3,等浓度时NaOH溶液pH大于Al(OH)3溶液,与图显示趋势相反,D错误。
故答案选C。


科目:高中化学 来源: 题型:
【题目】电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为__________________。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)__________c(CH3COO-)(填“>”、“<”或“=”)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________。
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】优良的有机溶剂对孟烷和耐热型特种高分子功能材料PMnMA的合成路线如下:

已知:①芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
![]() +RX
+RX![]()
![]() +HX(R是烃基,X为卤原子)
+HX(R是烃基,X为卤原子)
②0.01 molC质量为1.08 g,能与饱和溴水完全反应生成3.45 g白色沉淀,E不能使Br2的CCl4溶液褪色。
③G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1,G与Na2CO3溶液反应放出气体。
根据以上信息回答以下问题:
(1)化合物A的名称为______;C的结构简式为_______;C的名称为_______;
(2)下列说法正确的是_____(填选项字母)。
a.B可使酸性高锰酸钾溶液褪色
b.C不存在芳香族醛类同分异构体
c.D的酸性比E弱
d.F不能使溴水褪色
(3)①E与G反应生成H的化学方程式为__________;其反应类型为______。
②PMnMA的结构简式为_____,由H生成该有机物的反应类型为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂和形成的反应是( )
A.NH4Cl![]() NH3↑ +HCl↑
NH3↑ +HCl↑
B.2Na2O2+2CO2=2Na2CO3+O2
C.2NaOH+Cl2=NaCl+NaClO+H2O
D.CaC2+2H2O=Ca(OH)2 +C2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )
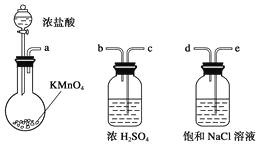
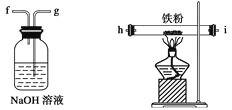
A.a b cdeefg–hB.aedcbhicbg
C.aed hicbgD.acb deh icbf
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请分析下图装置。

⑴Fe电极是_____(填“正”或“负”)极,其电极反应为________;
⑵Cu电极是_____电极,其电极反应为________________。
⑶若用浓硝酸做电解质溶液____做负极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。下列判断不正确的是( )
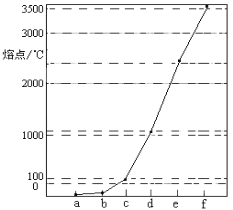
A. 图中对应的e、f单质晶体熔化时克服的是共价键
B. d单质对应元素的电子排布式:1s22s22p63s23p2
C. b元素形成的最高价含氧酸易与水分子之间形成氢键
D. 单质a、b、f对应的元素以原子个数比1∶1∶1形成的最简单分子中含2个σ键和2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双氧水是常见的氧化剂、消毒剂,一种制取双氧水的流程如下:
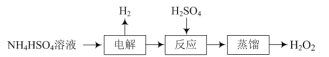
(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为______。
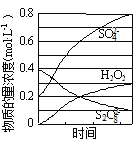
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为______。
(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO![]() 被还原成Mn2+,测定反应的离子方程式为______。
被还原成Mn2+,测定反应的离子方程式为______。
(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
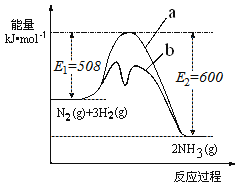
(1)根据如图提供的信息,写出该反应的热化学方程式____________________________,下图的曲线中________(填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_____________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n molN2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)500℃、50MPa时,在容积为1 L的容器中加入1 mol N2、3 mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为a。则K和a的关系是K=_______________。
(4)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 |
| 1 |
ⅱ | ______ |
| 10 |
ⅲ | 480 | ______ | 10 |
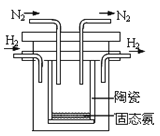
(5)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨。其实验装置如图。阴极的电极反应式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com