
【题目】(1)下图的虚线框中每一列、每一行相当于课本附录的元素周期表的每一族和每一周期,并已标出氢元素的位置,但它的列数和行数都多于元素周期表。请在虚线框中用实线画出周期表第一至第五周期的轮廓,并画出金属与非金属的分界线________。

(2)部分短周期主族元素的原子半径及主要化合价
元素 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 | 庚 | 辛 |
原子半径(nm) | 0.077 | 0.143 | 0.111 | 0.104 | 0.066 | 0.186 | 0.037 | 0.099 |
主要化合价 | +4,-4 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
①乙元素的原子结构示意图____________,丙在元素周期表中的位置___________,戊、庚、辛以原子个数比1∶1∶1形成的化合物的结构式______________。
②甲的单质与丁的最高价氧化物的水化物反应的化学方程式是___________,辛的单质与己的最高价氧化物的水化物反应的离子方程式是______________________________。
【答案】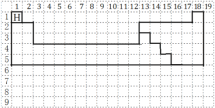
![]() 第2周期第IIA族H-O-ClC+2H2SO4(浓)
第2周期第IIA族H-O-ClC+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2OCl2+2OH-=Cl-+ClO-+H2O
CO2↑+2SO2↑+2H2OCl2+2OH-=Cl-+ClO-+H2O
【解析】
(1)周期表中第一周期2种元素,第二周期含8种元素,第三周期开始出现过渡元素,从第二周期开始,出现金属与非金属交界,用实线画出周期表第一至第五周期的轮廓,并画出金属与非金属的分界线如图为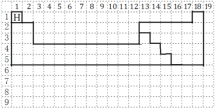 ;
;
(2)主族元素的最高化合价与其族序数相等,故己、庚为第ⅠA族,丁、戊为第ⅥA族,丁是S,戊是O,所以己是Na,庚是H;辛的最高价是+7价,最低价是-1价,则辛是Cl;甲有-4价和+4价,原子半径大于戊小于丁,则甲是C;根据乙、丙的最高价和原子半径可知乙是Al,丙是Be。则
①乙元素是Al,原子结构示意图为![]() ,丙是Be,在元素周期表中的位置为第2周期第IIA族,戊、庚、辛以原子个数比1∶1∶1形成的化合物是次氯酸,结构式为H-O-Cl。
,丙是Be,在元素周期表中的位置为第2周期第IIA族,戊、庚、辛以原子个数比1∶1∶1形成的化合物是次氯酸,结构式为H-O-Cl。
②甲的单质碳与丁的最高价氧化物的水化物浓硫酸反应的化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O,辛的单质氯气与己的最高价氧化物的水化物氢氧化钠反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O。
CO2↑+2SO2↑+2H2O,辛的单质氯气与己的最高价氧化物的水化物氢氧化钠反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】基于CaSO4为载氧体的天然气燃烧是一种新型绿色的燃烧方式,CaSO4作为氧和热量的有效载体,能够高效低能耗地实现CO2的分离和捕获其原理如下图所示:
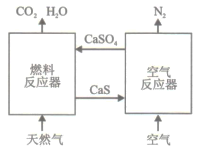
(1)已知在燃料反应器中发生如下反应:
i.4CaSO4(s)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反应器中主反应为_________(填“i”“ii”或“ⅲ”)。
②反应i和ii的平衡常数Kp与温度的关系如图1,则a_______0(填“ >”“ =“或“<” );720℃时反应ⅲ的平衡常数Kp=________。

③下列措施可提高反应ii中甲烷平衡转化率的是_______。
A.增加CaSO4固体的投入量 B.将水蒸气冷凝
C.降温 D.增大甲烷流量
(2)如图2所示,该燃料反应器最佳温度范围为850℃ -900℃之间,从化学反应原理的角度说明原因:_______。
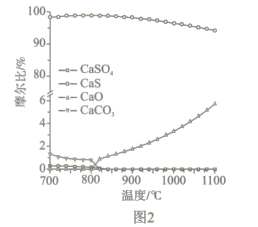
(3)空气反应器中发生的反应为
CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根据热化学原理推测该反应为__________反应。
②在天然气燃烧过程中,可循环利用的物质为________。
(4)该原理总反应的热化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于图示四个装置的叙述不正确的是


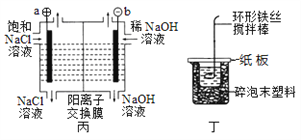
A. 装置甲是可以在铁钉上镀铜的装置
B. 装置乙若为电解精炼铜装置,则X电极为精铜
C. 装置丙的a端产生的气体能使湿润的淀粉碘化钾试纸变蓝
D. 装置丁可用于测定化学反应的反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是石化行业的重要基础原料。能发生如下一系列变化。下列说法不正确的是
![]()
A. 有机物I能发生氧化反应、取代反应和加成反应
B. 有机物II能使溴的四氯化碳溶液褪色
C. 有机物Ⅲ的同分异构体中,苯环上只有一个烃基的物质不只4种
D. 上图反应①属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能减小室内空气污染的是
A. 大量使用人造板材料家具 B. 涂刷墙壁用水性溶剂洗涤
C. 烹饪燃料用固体煤球代替天然气 D. 室内装修可用含氡胡花岗账等大理石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前36号元素A、B、C、D、E原子序数依次增大,A与B是同一周期紧邻元素,B与D同一主族,B元素氢化物的水溶液可用于玻璃的雕刻。C元素是同周期元素中第一电离能最小的元素,C与E的最外层电子数相同,E元素内层均排满电子。
(1)基态原子E的电子排布式为___________;依据电子排布周期表划分为5个区,该元素位于周期表的_________区。
(2)元素A、B、D电负性由大到小的顺序为___________。
(3)D2A分子中,中心原子的杂化方式为___________。分子键角大小关系,AB2分子_____D2A分子(填“大于”,“小于”或“等于”),原因_________________________。
(4)单质C经常用于储氢,储氢后形成晶体结构如图所示:
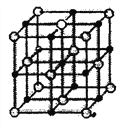
该晶体中与C离子近邻的氢离子有_______个。这些氢离子,构成的空间构型为_______。已知C离子与氢离子之间最近的核间距为a pm,则该晶体的密度为_____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
实验方案 |
|
|
|
|
目的 | A.比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | B.除去乙烯中的二氧化硫 | C.制银氨溶液 | D.证明碳酸酸性强于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温下,C(s)+H2O(g)![]() CO(g)+H2(g) 不能自发进行,则该反应的ΔH>0
CO(g)+H2(g) 不能自发进行,则该反应的ΔH>0
B. 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C. 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强
D. 常温下,在0.1 mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯和苯三种有机物的共同点是
A. 都由C和H两种元素组成
B. 都能使酸性KMnO4溶液褪色
C. 都能发生加成反应和取代反应
D. 在O2中完全燃烧都生成CO2和H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com