
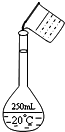
 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:| n |
| V |
| n |
| V |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
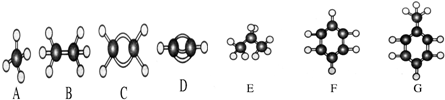
| 试剂 | 方法 | |
| 乙烷混有少量乙烯 | ||
| 溴苯混有少量溴单质 | ||
| 苯中混有少量苯酚 | ||
| 乙醇中混有少量水 | ||
| 硝酸钾中混有少量氯化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
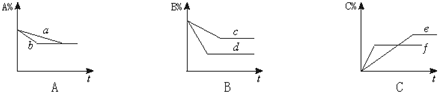
查看答案和解析>>
科目:高中化学 来源: 题型:
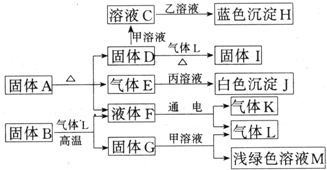
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 0.1mol?L-1的乙酸溶液中含有的氧原子数0.2NA |
| B、标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA |
| C、标准状况下,23g CH3CH2OH中含有的分子数目为0.5NA |
| D、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、被玻璃割伤手后,先取出伤口里的玻璃片,再用稀双氧水擦洗,然后敷药包扎 |
| B、苯酚沾在皮肤上应立即用酒精擦洗(提示:苯酚具有强烈腐蚀性,易溶于酒精) |
| C、温度计摔坏导致水银散落到地面上,应立即用水冲洗水银 |
| D、酒精灯碰倒洒出酒精着火,迅速用湿抹布扑盖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com