
【题目】某兴趣小组为探究Na2CO3溶液的性质,需要480mL 0.2molL-1的Na2CO3溶液。溶液的配制过程如图所示:

(1)指出配制过程中两处明显错误_______________.
(2)请分析下列情况对所配溶液浓度产生的影响:其中引起所配溶液浓度偏高的有__________(填序号,下同),偏低的有________,无影响的是________。
①用“左物右码”的方法称量(使用游码);②碳酸钠不纯,其中混有氯化钠;③容量瓶未经干燥使用;④称量碳酸钠时所用砝码生锈;⑤移液过程中有少量溶液溅出;
(3)向标准配制的0.2molL-1的Na2CO3溶液50mL中,逐滴加入0.2molL-1的Ba(OH)2溶液50mL。该过程中发生反应的离子方程式为_____;反应后所得溶液中溶质的物质的量浓度为_____molL-1(忽略溶液体积变化)。
【答案】称量的碳酸钠的质量应为10.6g,定容时视线应与刻度线、凹液面相切 ④ ②⑤ ①③ CO32+Ba2+=BaCO3↓ 0.2mol/L
【解析】
(1)由于实验室无480mL容量瓶,应选用500mL容量瓶,配制出50mL的溶液,据此计算所需的碳酸钠的质量;定容时应平视;
(2)根据c=![]() 并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(3)向标准配制的0.2molL-1的Na2CO3溶液50mL中,逐滴加入0.2molL-1的Ba(OH)2溶液50mL,两者物质的量相等,恰好完全反应生成BaCO3和NaOH,据此分析。
(1)由于实验室无480mL容量瓶,应选用500mL容量瓶,配制出50mL的溶液,故所需的碳酸钠的质量m=CVM=0.2mol/L×0.5L×106g/mol=10.6g,故所称量的碳酸钠的质量错误;定容时应平视刻度线,使凹液面与刻度线相切;
(2)①用“左物右码”的方法称量(使用游码)是正确的,故所配溶液的浓度无影响;
②碳酸钠不纯,其中混有氯化钠,则会导致碳酸钠的质量偏小,则浓度偏低;
③容量瓶未经干燥使用对浓度无影响;
④称量碳酸钠时所用砝码生锈,则砝码变重,导致称量出的药品的质量偏大,则溶液浓度偏高;
⑤移液过程中有少量溶液溅出,会导致溶质的损失,则浓度偏低;
(3)0.2molL-1的Na2CO3溶液50mL中,逐滴加入0.2molL-1的Ba(OH)2溶液50mL,两者物质的量相等,且均为0.01mol。混合后恰好完全反应生成BaCO3和NaOH:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH,离子方程式为:CO32-+Ba2+=BaCO3↓。由于Na2CO3和Ba(OH)2的物质的量均为0.01mol,则生成的NaOH的物质的量为0.02mol,由于溶液体积为100mL,故浓度为c=![]() =0.2mol/L。
=0.2mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)氨气是重要的化工原料,主要用作化肥、冷冻剂等。现向一固定容积的反应器中通入2molN2和6molH2在催化剂作用下加热至平衡状态,测得此时容器内压强比反应前减小了![]() ,列式计算H2的平衡转化率___。
,列式计算H2的平衡转化率___。
(2)燃料的燃烧将化学能转化成热能,提供了人类生存和发展所需要的能量和动力。现将标况下8.96L乙烷和乙烯的混合气体和足量氧气充分混合并点燃,燃烧产物经过浓硫酸充分吸收后增重16.2g,则混合气体中乙烷和乙烯的物质的量之比为多少___?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种元素①X、Y、Z的单质在常温下均为气体;②X单质可以在Z单质中燃烧,生成物为XZ,其中火焰为苍白色;③XZ极易溶于水,电离出X+和Z﹣,其水溶液可使蓝色石蕊试液变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体;⑤Z单质溶于X2Y中所得溶液具有漂白作用。
(1)推断元素符号X_____、Y_____、Z_____;
(2)化合物XZ的电子式为_____,X2Y属于_____(填离子化合物、共价化合物、共价分子);
(3)写出XZ(写化学式)的电离方程式_____;写出XZ(写化学式)与Ca(ClO)2反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:
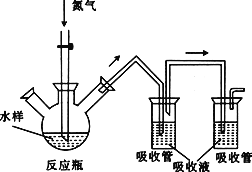
Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知:![]() )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。

(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的构型判断错误的是
A. 甲烷是正四面体结构,烷烃的碳原子呈直线形
B. 乙烯是平面结构,四个氢原子和二个碳原子共面
C. 苯分子中碳原子采用sp2杂化,得到平面正六边形结构
D. 氨气分子的空间构型为三角锥形,氮原子杂化方式为SP3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2是一种橙黄色的液体,遇水剧烈反应,并产生能使品红褪色的气体。下列说法错误的是

A. S2Cl2的分子中的两个S原子均是sp3杂化
B. S2Br2与S2Cl2结构相似,熔沸点:S2Br2 > S2Cl2
C. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O = SO2↑+3S↓+4HCl
D. S2Cl2分子中的S为+1价,是含有极性键和非极性键的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiNiO2是一种前景很好的锂离子电池正极材料。当温度高于850°C时,LiNiO2会分解。请按要求回答下列问题:
(1)LiNiO2中Ni的化合价为___________,工业上用Ni(OH)2与LiOH的混合物在空气流中加热到700~800°C制得 LiNiO2,该反应的化学方程式为___________,加热温度不宜过高的原因是_________,工业上也可用LiNO3代替上述工艺中的LiOH,存在的缺点可能是_______。
(2)以废旧二次电池为原料回收利用合成Ni(OH)2的工艺如下:

已知:酸浸后滤液中含有Ni2+、Al3+、Fe3+、Mn2+;
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,Ksp[Ni(OH)2]=1.6×10-14;
①滤渣Ⅱ为___________。
②“氧化除锰”是将锰元素最终转化为MnO2而除去,反应历程如下:
i.5S2O82-+2Mn2++8H2O=2MnO4-+10SO42-+16H+;
ii.______________________(用离子方程式表示)。
③转化操作后,还需经过过滤、洗涤、烘干得到产品。检验Ni(OH)2是否洗涤干净的实验操作是___________。
④调pH=5操作时,已知溶液中Ni2+浓度为2.0mol/L,则“滤渣II”中是否存在Ni(OH)2沉淀?___________(列式计算,并使用必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马兜铃酸是一种致癌物。如图为马兜铃酸的结构简式,R,R1,R2代表-H,-OH或-OCH3中的一种或几种,下列有关说法正确的是

A. 若R代表—OH,R1,R2代表—H,则对应有机物的分子式为C16H9NO7
B. 若R代表—H,R1,R2代表—OCH3,则对应有机物的结构中含有4种官能团
C. 若R,R1,R2均代表—H,则对应有机物能发生取代反应,氧化反应和水解反应
D. 若R,R1,R2中至少有1个代表—H,则对应的有机物最多有9种结构(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量变化示意图,下列说法正确的是
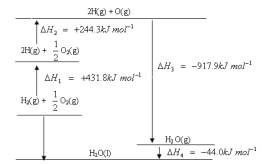
A. H2在O2中燃烧生成气态水的过程中吸收能量
B. 断开1mol H2O(g)所含的共价键共放出917.9kJ的能量
C. H2O(g)比H2O(l)更稳定
D. H2在O2中燃烧生成液态水的热化学方程式为:2H2(g) + O2(g) == 2H2O(l) ![]() H = -571.6 kJ·mol-1
H = -571.6 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com