
【题目】25℃时,用NaOH溶液滴定H2C2O4 溶液,溶液中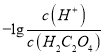 和-lgc(HC2O4-)或
和-lgc(HC2O4-)或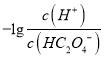 和-lgc(C2O42-)关系如图所示,下列说法正确的是
和-lgc(C2O42-)关系如图所示,下列说法正确的是
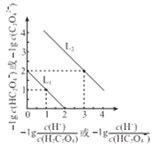
A. 曲线L1表示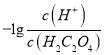 和-lgc(HC2O4-)的关系
和-lgc(HC2O4-)的关系
B. Ka2(H2C2O4)的数量级为10-2
C. NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 向0.1mol/LH2C2O4溶液中加入少量水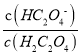 减小
减小
【答案】A
【解析】A. H2C2O4是二元弱酸,在溶液中发生两步电离:H2C2O4 ![]() HC2O4-+H+、HC2O4-
HC2O4-+H+、HC2O4-![]() C2O42-+H+,Ka1=
C2O42-+H+,Ka1=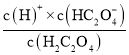 、Ka2=
、Ka2= ,-lgKa1=-lg
,-lgKa1=-lg =-[lg
=-[lg +lgc(HC2O4-)]、-lgKa2=-lg
+lgc(HC2O4-)]、-lgKa2=-lg =-[lg
=-[lg +lgc(C2O42-)],因Ka1>Ka2,则-lgKa1<-lgKa2,即-[lg
+lgc(C2O42-)],因Ka1>Ka2,则-lgKa1<-lgKa2,即-[lg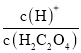 +lgc(HC2O4-)]<-[lg
+lgc(HC2O4-)]<-[lg +lgc(C2O42-)],所以曲线L1表示
+lgc(C2O42-)],所以曲线L1表示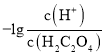 和-lgc(HC2O4-)的关系,故A正确;B. 曲线L2表示
和-lgc(HC2O4-)的关系,故A正确;B. 曲线L2表示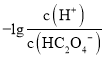 和-lgc(C2O42-)的关系,据图可知,-lgKa2=-lg
和-lgc(C2O42-)的关系,据图可知,-lgKa2=-lg =-[lg
=-[lg +lgc(C2O42-)]=2+3=5,则Ka2=10-5,Ka2(H2C2O4)的数量级为10-5,故B错误;C. 由上述分析可知,HC2O4-发生电离的平衡常数Ka2=10-5,HC2O4-发生水解反应的平衡常数Kh=
+lgc(C2O42-)]=2+3=5,则Ka2=10-5,Ka2(H2C2O4)的数量级为10-5,故B错误;C. 由上述分析可知,HC2O4-发生电离的平衡常数Ka2=10-5,HC2O4-发生水解反应的平衡常数Kh=![]() =
=![]() =10-12,Ka2>Kh,即HC2O4-的电离程度大于水解程度,所以在NaHC2O4溶液中c(Na+)>c(HC2O4-)> c(C2O42-) >c(HC2O4),故C错误;D. 由Ka1=
=10-12,Ka2>Kh,即HC2O4-的电离程度大于水解程度,所以在NaHC2O4溶液中c(Na+)>c(HC2O4-)> c(C2O42-) >c(HC2O4),故C错误;D. 由Ka1=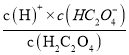 可得:
可得: 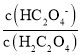 =
=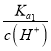 ,向0.1mol /LH2C2O4溶液中加入少量水,Ka1不变,c(H+)减小,则
,向0.1mol /LH2C2O4溶液中加入少量水,Ka1不变,c(H+)减小,则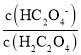 =
=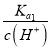 增大,故D错误;答案选A。
增大,故D错误;答案选A。


科目:高中化学 来源: 题型:
【题目】氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且使平衡混合物中NH3的体积分数一定增大的是______。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下向100m10.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
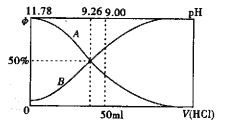
①表示NH3·H2O浓度变化的曲线是______(填“A”或“B")。
②NH3·H2O的电离常数为_______(已知1g1.8=0.26)
③当加入盐酸体积为50ml时,溶液中c(NH4+)-c(NH3·H2O)=____mol/L(用精确值表示)。
II.已知常温下,Ksp[Al(OH)3]=4.0×10-38,在AlCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:________________;若将所得悬浊液的pH调整为3,则溶液中Al3+浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.10m/L的弱碱BOH滴定10.00 ml a mol/L的盐酸,溶液的pH与所加BOH溶液体积(V)的关系如图所示。已知N点溶液中存在关系式:c(C1—)=c(B+)+c(BOH)。下列说法正确的是

A. M点溶液中存在c(H+)=c(OH—)+2c(BOH)+c(B+)
B. N、Q两点溶液中BOH电离平衡常数:N<Q
C. P点BOH过量,此时溶液中c(B+)>c(Cl—)
D. a<0.108
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究称癌症导致的死亡率呈逐年上升的趋势,目前是仅次于心血管疾病的第二大杀手。M是一种可用于治疗肿瘤的药物,其合成路线如下

已知:①芳香烃A的相对分子质量在86-96之间:F能使溴水褪色。
②J与 NaHCO3溶液反应放出CO2气体,核磁共振氢谱显示其有3个吸收峰。
③ ④M的结构简式为
④M的结构简式为
回答下列问题:
(1)A的化学名称为________________ , ④的反应类型是_____________.
(2)D分子中所含官能团的名称为_________________________。
(3)②的反应方程式为________________,⑤的反应方程式为__________________。
(4)N(C7H7NO2)是E在一定条件下的水解产物,符合下列条件的N的同分异构体有_____种。其中核磁共振氢谱有4个峰的结构简式为_________________。
①分子中苯环上直接连一NH2②能发生银镜反应
(5)4-甲氧基乙酰苯胺( )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )和乙酰氯( CH3 COCl)制备4-甲氧基乙酰苯胺的合成路线(无机试剂任选):_____________________________________________________________。
)和乙酰氯( CH3 COCl)制备4-甲氧基乙酰苯胺的合成路线(无机试剂任选):_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲探究CO还原CuO,设计如图所示装置(夹持装置略去)。下列说法正确的是
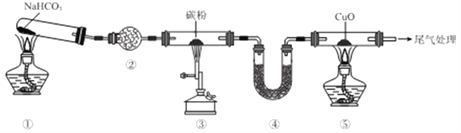
A. ②、④中均可盛装碱石灰
B. 加热的顺序为③、①、⑤
C. ①、③、⑤中均发生氧化还原反应
D. 可将尾气用导管通入到⑤的酒精灯处灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈CH3CN 等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯睛(C3H3N)和副产物丙烯醛(CH2=CHCHO)的热化学方程式如下:
① C3H6(g)+NH3(g)+O2(g)=C3H3N(g)+3H2O(g)△H=-515kJ/mol
② C3H6(g)+O2(g)=C3H4O(g)+H2O(g) △H=-353kJ/mol
有利于提高丙烯腈平衡产率的反应条件是______;提高丙烯腈反应选择性的关键因素是_____.
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是_____;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D. 反应活化能增大
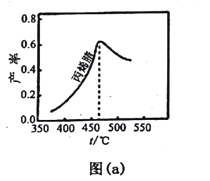
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为_________ ,理由是_______。进料氨、空气、丙烯的理论体积约为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________;
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________;
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ ![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ ![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________;
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应: ![]() (aq)+I2(aq)+2OH(aq)
(aq)+I2(aq)+2OH(aq)![]()
![]() (aq)+2I(aq)+ H2O(l)。溶液中c(
(aq)+2I(aq)+ H2O(l)。溶液中c(![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。

①下列不可判断反应达到平衡的是__________(填标号);
a.溶液的pH不再变化 b.v(I)=2v(![]() )
)
c.c(![]() )/c(
)/c(![]() )不再变化 d.c(I)=y mol·L1
)不再变化 d.c(I)=y mol·L1
②tm时,v逆_____ v正(填“大于”“小于”或“等于”);
③tn时v逆_____ tm时v逆(填“大于”“小于”或“等于”);
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________;
(5)H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图-1和题图-2所示:
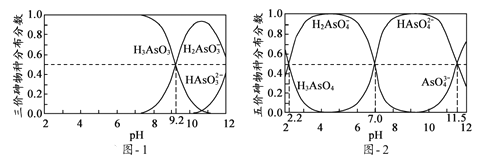
①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为____________;
②H3AsO4第一步电离方程式H3AsO4![]() H2AsO4-+H+的电离常数为Ka1,则pKa1=_________(p Ka1 = -lg Ka1);
H2AsO4-+H+的电离常数为Ka1,则pKa1=_________(p Ka1 = -lg Ka1);
(6)溶液的pH对吸附剂X表面所带电荷有影响,pH =7.1时,吸附剂X表面不带电荷;pH > 7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多。pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如题图-3所示:
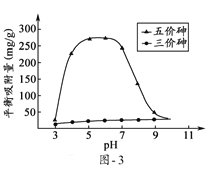
试问,提高吸附剂X对三价砷去除效果可采取的措施是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种物质,均含同一种元素,一定条件下其转化关系如下(部分产物已略去):
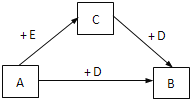
请回答:
(1)若A是短周期元素组成的金属单质,D是短周期中原子半径最大的主族元素形成的氢氧化物。
①组成A的元素在周期表中的位置是_________________。
②当A与D的溶液反应转移1.5 mol电子时,产生气体的体积(标准状况)为____L。
(2)若A是常见金属单质,B的溶液为黄色,D的组成元素的原子M层电子数比L层少1。
①下列关于C的说法正确的是_________(填字母)。
a. 其溶液为无色 b. 遇KSCN溶液变红色
c. 既有氧化性也有还原性 d. 其溶液可用于吸收氯气
②B与HI溶液反应可生成C、E和一种单质,该反应的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是
A. 0.6mol过氧化钠晶体中所含阴离子的数目为1.2NA
B. 电解精炼铜时,若阳极质量减少6.4g,则阴极得到电子数为0.2NA
C. 标准状况下,22.4LCHCl3中含有的C-Cl键数为3NA
D. 常温常压下,4.0gD2O中含有的中子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com