
分析 (1)在水溶液中或熔融状态下能导电的化合物为电解质;
(2)在水溶液中和熔融状态下均不能导电的化合物为非电解质;
(3)物质有自由移动的电子或离子则能导电.
解答 解:①NaCl晶体不能导电,是电解质;
②铝能导电,是单质,既不是电解质也不是非电解质;
③CaCO3固体不能导电,是电解质;
④酒精不能导电,是非电解质;
⑤NH3不能导电,是非电解质;
⑥熔化的KNO3能导电,是电解质;
⑦盐酸能导电,是混合物,故既不是电解质也不是非电解质.
(1)综上分析可知,是电解质的是①③⑥,故答案为:①③⑥;
(2)综上分析可知,是非电解质的是④⑤,故答案为:④⑤;
(3)综上分析可知,能导电的是②⑥⑦,故答案为:②⑥⑦.
点评 本题考查了电解质、非电解质和物质导电的判断,难度不大,应注意的是能导电的不一定是电解质,电解质不一定能导电.


科目:高中化学 来源: 题型:选择题
| A. | MnS的溶解度小于PbS、CuS、CdS等硫化物的溶解度 | |
| B. | 除杂试剂MnS也可用Na2S替代 | |
| C. | MnS与Cu2+反应的离子方程式是Cu2++S2-=CuS↓ | |
| D. | 整个过程涉及的反应类型有氧化还原反应和复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠加热可以分解,因为升高温度利于熵增的方向自发进行 | |
| B. | 在温度、压强一定的条件下,自发反应总是向△G=△H-T△S<0的方向进行 | |
| C. | 水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 | |
| D. | 混乱度减小的吸热反应一定不能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度,H2S浓度减小,表明该反应是放热反应 | |
| B. | 通入CO后,逆反应速率逐渐增大,直至再次平衡 | |
| C. | 反应前H2S物质的量为6mol | |
| D. | CO的平衡转化率为20% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积 ②>③>①>④ | B. | 密度 ②>③>④>① | ||
| C. | 质量 ②>③>④>① | D. | 氢原子个数 ①>③>④>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
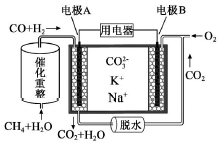
| A. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 反应CH4+H2O $\frac{\underline{催化剂}}{△}$ 3H2+CO,每消耗1molCH4转移12mol 电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量时,左盘高,右盘低 | |
| B. | 定溶时俯视容量瓶刻度线 | |
| C. | 原容量瓶洗净后未干燥 | |
| D. | 摇匀后见液面下降,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤⑦ | C. | ④⑧ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,推断溶液中含有NH4+ | |
| B. | 无色试液在焰色反应中呈黄色,推断试液是钠盐溶液,不含钾盐 | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,推断溶液中含有CO32- | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,推断溶液中含有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com