
����Ŀ��ʵ�����Ʊ�����������ʵ��װ����ͼ��ʾ��
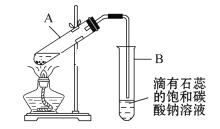
(1)A��Ũ�����������________��
(2)ʵ��ʱԤ���Թ�B�в����������У�___��___����2�㣩��
(3)�����Թ�B�з�����������������õķ�����_______(���������)����Ҫ�Բ�Ʒ�����������и��__����ܡ����ܡ����ü�ʯ�Ҹ��������______��
(4)д��ʵ�������Ҵ���������ȡ���������Ļ�ѧ����ʽ:_______��
(5)����A�м���4.6 g���Ҵ���9.0 g�����ᡢ����Ũ���ᣬ��������A����ַ�Ӧ�����Ʒ���д���������������5.28 g����ʵ��IJ�����________����ע������ָ����ij���������ʵ�ʲ��������۲����ı�ֵ��
���𰸡�����������ˮ��������ˮ������ƽ�������ƶ������ʸ��ߣ� ����״Һ������ �ϲ�ʯ���Ϊdz��ɫ ��Һ ���� �����������������ʯ�ҷ�����Ӧ CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O 60%
CH3COOCH2CH3 + H2O 60%
��������
ʵ������Ҫ����ˮ������Ҵ���Ũ������������·�Ӧ���������������ñ���̼������Һ��������������������Һ�õ���������������ʵ���������ۼ�������ɵ����������������ٸ���ʵ�ʲ���������ʡ�
��ʵ�����Ʊ�������������������Ҵ�Ũ������������·�Ӧ���÷�Ӧ�ǿ��淴Ӧ����ˮ������ƽ�������ƶ������A��Ũ������Ҫ�����Ǵ�������ˮ������ˮ������ƽ�������ƶ������ʸ��ߣ��ʴ�Ϊ������������ˮ��������ˮ������ƽ�������ƶ������ʸ��ߣ�
�����ɵ������������뵽B�У��������������ڱ���̼������Һ�����ϲ㣬��״Һ�壬��������δ��Ӧ��������Ҵ����뵽B�У������ʹ�ϲ�ʯ���dz��ɫ�����ʵ��ʱԤ���Թ�B�в����������У�����״Һ�����ɣ��ϲ�ʯ���Ϊdz��ɫ���ʴ�Ϊ������״Һ�����ɣ��ϲ�ʯ���Ϊdz��ɫ��
����������������̼������Һ����������Թ�B�з�����������������õķ����Ƿ�Һ����ʯ���������ƺ��������ƵĻ������������������ڼ���������Ҫˮ�⣬��˲����ü�ʯ�Ҹ�������������������������ʯ�ҷ�����Ӧ���ʴ�Ϊ����Һ�����ܣ������������������ʯ�ҷ�����Ӧ��
��ʵ�������Ҵ���������ȡ���������Ļ�ѧ����ʽCH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O���ʴ�Ϊ��CH3COOH + CH3CH2OH
CH3COOCH2CH3 + H2O���ʴ�Ϊ��CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O��
CH3COOCH2CH3 + H2O��
��
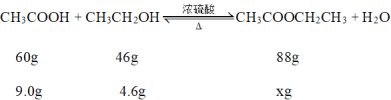
�������ݷ����ó����������ֻ�ܰ����Ҵ����м��㣬
![]()
���x = 8.8g
![]() ���ʴ�Ϊ60%��
���ʴ�Ϊ60%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ȷ��Ʊ�![]() ���������ܷ�ӦΪ
���������ܷ�ӦΪ![]() ����˵����ȷ����
����˵����ȷ����
A.![]() ��
��![]() ����������
����������
B.![]()
C.ÿת��3mol���ӣ���![]() ������
������
D.��������ֻ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȡ4.00g����ͭ�������������������50.0mL2.00mol��L-1���������ܽ⣬��������Һ�м���5.60g���ۣ���ַ�Ӧ�ù��������Ϊ3.04g������㣺
��1���������۳�ַ�Ӧ����Һ�����ʵ����ʵ���_________________��
��2����������������ͭ������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵���
ѡ�� | �� | �� | �� | ʵ����� |
|
A | Ũ���� | KMnO4 | NaOH | ����ȡ���ռ�������������β�� | |
B | Ũ��ˮ | ��ʯ�� | ��̪ϡ��Һ | ����ȡ��������֤������ˮ��Һ�ʼ��� | |
C | ϡ���� | Na2SO3 | Ba(NO3)2��Һ | SO2������Ա��ξ������ɰ�ɫ���� | |
D | ϡ���� | Na2CO3 | Na2SiO3��Һ | �ǽ����ԣ�S>C>Si |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�NCl3��һ�ֻ�ɫ��״Һ�壬���Ʊ�����ˮ������ClO2��ԭ�ϣ����Բ�����ͼ��ʾװ���Ʊ�NCl3������˵����ȷ����( )

A.ÿ����1 mol NCl3����������4 mol H�������ӽ���Ĥ���Ҳ������Ǩ��
B.����ʪ���KI��������ֽ��������M
C.ʯī���ĵ缫��ӦʽΪNH4+��3Cl����6e��===NCl3��4H��
D.�������У����ӵ���������Ϊ��Դ������������ʯī������Դ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ���̿��Ʊ�1,4-�����������Իش�
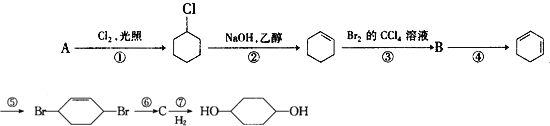
(1)��Ӧ�١��ڡ��۷ֱ�����___��____��___��(�Ӧ����)
(2)������![]() �����������ŵ�����Ϊ_______��________��
�����������ŵ�����Ϊ_______��________��
(3)д�����л�����Ľṹ��ʽ��A_________��C________��
(4)��Ӧ�����õ��Լ�������Ϊ_________________��
(5)д�����з�Ӧ�Ļ�ѧ����ʽ����Ӧ��_____________����Ӧ��_______________��
(6)��д����CH3CH2BrΪԭ���Ʊ�HOCH2CH2OH�ĺϳ�·������ͼ[���Լ�����,�ϳ�·������ͼʾ��������]��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ����( )
A.��״���£�11.2 L H2O �к��е���ԭ����Ϊ0.5NA
B.5.6 g�����������ᷴӦת�Ƶĵ�����Ϊ0.3NA
C.16 g O2��16 g O3���е���ԭ����Ŀ���
D.���³�ѹ�£�11.2 L��������ԭ����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��õζ�����ȡһ�������Ũ��ˮ������ƿ�У���NaOH��Һ�Ժ㶨�ٶ����ζ���Ũ��ˮ�����ݲⶨ������Ƴ�ClO����ClO3�������ӵ����ʵ���Ũ��c��ʱ��t�Ĺ�ϵ�������¡�����˵����ȷ����( )
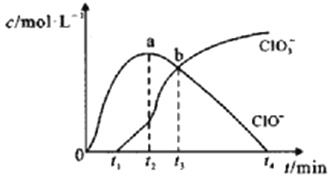
A.NaOH��Һ��Ũ��ˮ����ʹ��ͬ�ֵζ���ʢװ
B.a����Һ�д������¹�ϵ��c(Na+) + c(H+) = c(ClO��)+ c(OH��)+ c(ClO3��)
C.b����Һ�и�����Ũ�ȣ�c(Na+) > c(Cl��) > c(ClO��) = c(ClO3��)
D.t2~t4��ClO�������ʵ����½���ԭ�������ClO�������绯��2ClO��= Cl��+ ClO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե��з�̪��Һ��������Һ����������ɫ�������
A. ������Һ���� B. CH3COONa��Һ����
C. ��ˮ�м�������NH4Cl���� D. С�մ���Һ�м�������NaCl����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com