
【题目】(1)①某温度下,等物质的量的碘和环戊烯(![]() )在刚性容器内发生反应:
)在刚性容器内发生反应:![]() (g)+I2(g)===
(g)+I2(g)===![]() (g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数Kp=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
(g)+2HI(g),起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数Kp=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
②环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是________(填标号)。

A.T1>T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L-1
(2) 298 K时,将20 mL 3x mol·L-1Na3AsO3、20 mL 3x mol·L-1 I2和20 mL NaOH溶液混合,发生反应:AsO33- (aq)+I2(aq)+2OH-(aq)![]() AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。

下列可判断反应达到平衡状态的是________(填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO33-)
c.  不再变化
不再变化
d.c(I-)=y mol·L-1
(3)已知反应2HI(g) ![]() H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。
H2(g)+I2(g),ΔH>0,由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。

【答案】40% 3.56×104 BD CD a、c A、E
【解析】
(1)运用“三段式”法计算平衡时各反应物的物质的量,根据气体物质的量之比等于压强之比,计算转化率及平衡常数;(2)根据平衡状态的本质和特征分析解答;(3)根据平衡状态的建立及外界条件对平衡移动的影响分析解答。
(1)①设碘和环戊烯(![]() )的初始物质的量都为nmol,转化的物质的量为xmol,
)的初始物质的量都为nmol,转化的物质的量为xmol,
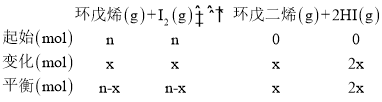
刚性容器内气体的压强与物质的量成正比,则:![]() =1+20%,解得:x=0.4n,平衡时环戊烯的转化率为:
=1+20%,解得:x=0.4n,平衡时环戊烯的转化率为:![]() ;
;
平衡时混合气体的压强为:105Pa×(1+20%)=1.2×105Pa,混合气体总物质的量为:(n-0.4n+n-0.4n+0.4n+0.4n×2)mol=2.4nmol,平衡时各组分所占压强分别为p(![]() )=p(I2)=
)=p(I2)=![]() ,p(
,p(![]() )=
)=![]() ,
,
p(HI)=![]() ,该反应的平衡常数Kp=
,该反应的平衡常数Kp= ;
;
A.通入惰性气体,各组分浓度不变,平衡不移动,则环戊烯的转化率不变,故A错误;
B.该反应为吸热反应,提高温度平衡向着正向移动,环戊烯的转化率增大,故B正确;
C.增加环戊烯浓度,环戊烯的转化率减小,故C错误;
D.增加碘浓度,反应物浓度增大,平衡向着正向移动,环戊烯的转化率增大,故D正确;
故答案为:40%;3.56×104;BD;
②A. 温度越高反应速率越快,根据图示可知,在温度T2(虚线)的反应速率较大,则T1<T2,故A错误;
B. 温度:a<c,浓度a>c,无法比较a、c点反应速率,故B错误;
C. a到b的过程为正反应速率逐渐减小,且b点v(正)>v(逆),则a点的正反应速率大于b点的逆反应速率,故C正确;
D. b点时环戊二烯的浓度变化为:1.5mol/L-0.6mol/L=0.9mol/L,环戊二烯的二聚体的浓度为环戊二烯浓度变化的1/2,则b点时二聚体的浓度为0.9mol/L×1/2=0.45molL-1,故D正确;故答案为:CD;
(2)a. 溶液pH不变时,则c(OH)也保持不变,反应达到平衡状态,故a正确;
b. 同一个化学反应,速率之比等于化学计量数之比,无论是否达到平衡,都存在v(I-)=2v(AsO33-),故b错误;
c. 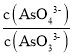 不再变化,可说明各物质的浓度不再变化,反应达到平衡状态,故c正确;
不再变化,可说明各物质的浓度不再变化,反应达到平衡状态,故c正确;
d. 由图可知,当c(AsO43)=ymolL1时,浓度不再发生变化,则达到平衡状态,由方程式可知此时c(I)=2ymolL1,故d错误;故答案为:ac;
(3)对于2HI(g)H2(g)+I2(g),反应建立平衡时:升高温度,正、逆反应速率均加快,因此排除C点,正反应为吸热反应,升高温度,平衡向吸热反应方向移动,因此平衡正向移动,再次平衡时HI的物质的量分数减小,因此排除B点,故选A点;对于H2(g)+I2(g)2HI(g),反应建立平衡时:升高温度,正、逆反应速率均加快,升高温度,平衡向吸热反应方向移动,因此平衡逆向移动,再次平衡时H2的物质的量分数增大,故选E点;因此反应重新达到平衡,v正~x(HI)对应的点为A,v逆~x(H2)对应的点为E,故答案为:A、E。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】25 ℃,c(HCN)+c(CN-)=0.1 mol·L-1的一组HCN和NaCN的混合溶液,溶液中 c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是( )
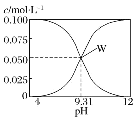
A.将 0.1 mol·L-1 的 HCN 溶液和 0.1 mol·L-1NaCN溶液等体积混合(忽略溶液体积变化):c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+)
B.W 点表示溶液中:c(Na+)=c(HCN)+c(CN-)
C.pH=8的溶液中:c(Na+)+c(H+)+c(HCN)=0.1 mol·L-1+c(OH-)
D.将0.3 mol·L-1 HCN溶液和0.2 mol·L-1NaOH溶液等体积混合(忽略溶液体积变化):c(CN-)+3c(OH-)=c(HCN)+3c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有离子:K+、Na+、Fe2+、Fe3+、SO32-、SO42-,且溶液中各离子的物质的量相等,将此溶液分为两份,一份加高锰酸钾溶液,现象为紫色褪去,另一份加氯化钡溶液,产生了难溶于水的沉淀。下列说法正确的是( )
A.若溶液中含有硫酸根,则可能含有K+
B.若溶液中含有亚硫酸根,则一定含有K+
C.溶液中可能含有Fe3+
D.溶液中一定含有Fe2+和SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
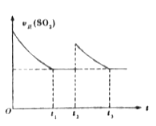
A. t1时平衡常数K1小于t3时平衡常数K2
B. t1时平衡混合气的M1 >t3时平衡混合气的M2
C. t2时刻改变的条件可能是:升温或缩小容器体积
D. t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 molL﹣1s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL0.50mol·L﹣1盐酸与50mL0.55molL﹣1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中的热量可计算中和热。回答下列问题:

(1)实验中改用60mL0.50mol·L﹣1盐酸跟50mL0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量___(填“相等”或“不相等”),所求中和热___(填“相等”或“不相等”),简述理由:___。
(2)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___;用50mL0.50mol·L﹣1CH3COOH溶液(已知CH3COOH电离时吸热)进行上述实验,测得的中和热的数值会___。(均填“偏大”、“偏小”或“无影响”)
(3)平行地做一次这样的实验需要测定___次温度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如下图所示。下列分析不正确的是

A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点,两溶液中含有相同物质的量的OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
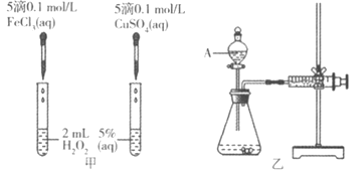
(1)定性如图甲可通过观察________________现象,定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是________________
(2)定量如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为________________,实验中需要测量的数是________________
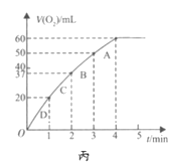
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。A、B、C、D各点反应速率由快到慢的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为实现下列实验目的,下表提供的主要仪器以及所用试剂均合理的是( )
选项 | 实验目的 | 主要仪器 | 试剂 |
A | 配制480mL | 胶头滴管、烧杯、玻璃棒、托盘天平、480mL容量瓶 | NaOH固体、蒸馏水 |
B | 分离 | 分液漏斗、烧杯 | 乙醇 |
C | 鉴别 | 试管、胶头滴管 | 澄清石灰水 |
D | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com