
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
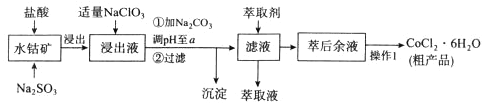
已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
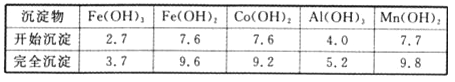
③CoCI2.6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式: 。
(2)写出NaClO3发生反应的主要离子方程式: ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式: 。
(3)惰性电极电解CoCl2溶液的阳极电极反应式为 。
(4)“操作1”中包含3个基本实验操作,它们依次是 、 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是 。
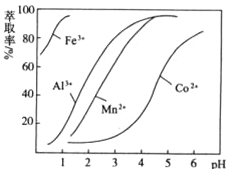
(5)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是 ,其使用的最佳pH范围是 。
A.2.0~2.5 | B.3.0~3.5 |
C.4.0~4.5 | D.5.0~5.5 |
(6)力测定粗产品中CoCl2·H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 。(答一条即可)
【答案】(1)Co2O3+SO32-+4H+=2Co2++SO42-+2H2O。(2)ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
(3) 2Cl--2e-=Cl2↑(4)蒸发浓缩,冷却结晶;降低烘干温度,防止产品分解。
(5)除去锰离子 B(6)粗产品含有可溶性氯化物或晶体失去了部分结晶水
【解析】试题分析:(1)向水钴矿加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有氢离子,钴离子,亚铁离子,锰离子和铝离子等,所以氧化钴和亚硫酸钠在酸性条件下发生氧化还原反应,根据电荷守恒和得失电子守恒,反应的离子方程式为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O。(2)氯酸钠的作用是将亚铁离子氧化成铁离子,其反应的离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O..(3)电解氯化钴溶液时阳极是氯离子失去电子生成氯气,电极反应为:2Cl--2e-=Cl2↑(4)利用从溶液中制取固体的方法制取氯化钴固体,其操作为蒸发浓缩,冷却结晶,过滤。根据题意知道氯化钴晶体常温下稳定无毒,加热到110~120℃,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的氯化钴晶体需减压烘干。(5)根据流程图分析,此时溶液中存在锰离子和钴离子,由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液pH在3.0-3.5之间,可使锰离子完全沉淀,丙防止钴离子转化为氢氧化钴沉淀。(6)根据氯化钴晶体的组成分析,造成产品中氯化钴晶体的质量分数大于100%的原因可能是含有杂质,导致氯离子含量大或结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大。


科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中由于哑铃形的C22-存在,使晶胞沿一个方向拉长。下列关于CaC2晶体的说法中正确的是( )

A.1 个 Ca2+周围距离最近且等距离的 C22-数目为 6
B.该晶体中的阴离子与F2是等电子体
C.6.4 g CaC2晶体中含阴离子0.1 mol
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列流程中有机物均为芳香族化合物。H为一种酯,其合成路线如下:

已知以下信息:
① 有机物B能发生银镜反应,D的相对分子质量比C大4,E的苯环上的一溴代物有两种。
②![]()
③![]()
请回答下列问题:
(1)A的结构简式____________ ,C→D的反应类型为_____________;B中含氧官能团名称为__________ ,F中不含氧的官能团的名称为___________ ; H的结构简式为___________;
(2)E→F与F→G的顺序不能颠倒,理由是___________;
(3)F→G ①的化学方程式为___________;
(4)G还可以通过缩聚反应制得高分子材料,试写出其结构简式___________;
(5)A的同分异构体很多,其中能使FeCl3溶液显紫色有___________种,写出一种核磁共振氢谱有4组峰的分子的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】促进生态文明,保护生态环境,是实现“中国梦”的重要组成部分。
(1)天然水中杂质较多,常需加入明矾、漂白粉等物质处理后才能饮用。加入明矾的作用是________;漂白粉能杀菌消毒是因为漂白粉使蛋白质发生________。
(2)处理废水中重金属铊(TI),需在废水中加入NaClO,作________(填“氧化剂”或“还原剂”),将TI+转变为TI3+;再加入氨水,将TI3+转变为难溶物TI(OH)3,写出生成TI(OH)3,的离子方程式:________。该方法处理后的废水中因含有大量的________元素(填写元素名称),直接排放易导致水体富营养化。
(3)聚乙烯塑料常用于食品包装,随便丢弃会造成白色污染。聚乙烯的结构简式是________,聚乙烯塑料属于________(填“热固性”或“热塑性”)塑料。
(4)空气污染指数是根据空气中________、二氧化氮和可吸入颗粒等污染物的浓度计算出来的数值。大气污染的危害是多方面的,如形成酸雨,除雨是指pH小于________的降水。
(5)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2,其物质转化如图所示。写出其中氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式:________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知a为ⅡA族元素,b为ⅢA族元素,它们的原子序数分别为m和n,且a、b为同一周期元素,下列关系错误的是 ( )
A. n=m+1 B. n=m+11 C. n=m+25 D. n=m+10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛的化合物如TiO2、Ti(NO3)4、TiCl4、 Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式____________。
(2)TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4-中B原子的杂化类型为____________;
(3)在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子化学式为_________________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(绿色),两者配位数_____(填“相同”或“不同”),绿色晶体中配体是______。

(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为____________。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为![]() g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[2CuCO3·Cu(OH)2]可用于制造烟火等。在较低温度下,将Cu(NO3)2饱和溶液倒入一定浓度的Na2CO3溶液中,即有碱式碳酸铜生成,同时有CO2逸出。
(1)Cu基态核外电子排布式为________。
(2)向Cu(NO3)2溶液中加入过量的氨水可生成[Cu(NH3)4]2+、1 mol[Cu(NH3)4]2+中含有σ键的数目为________。
(3)与CO2互为等电子体的一种微粒为________ (填化学式)。 NO3-的空间构型为________(文字描述)。
(4)烟火燃放过程中会产生SO2、NO等有毒气体,N、O、S 原子的第一电离能由大到小的顺序是________。
(5)Cu的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是________。
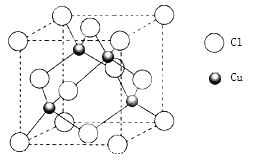
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中化合物做还原剂的是
A. Br2+2NaI= 2NaBr+ I2 B. Zn+ H2SO4= ZnSO4+H2↑
C. 3C+CaO![]() CaC2+CO↑ D. 2Al+ Fe2O3
CaC2+CO↑ D. 2Al+ Fe2O3![]() 2Fe+ Al2O3
2Fe+ Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写化学方程式:
(1)一种单质还原一种化合物_____________________________________
(2)一种单质氧化另一种单质_________________________________________
(3)一种非金属单质还原一种氧化物________________________________________
(4)同一物质中一种元素氧化另一种元素______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com