
【题目】实验室用密度为1.84 gcm﹣3、溶质的质量分数为98 %的硫酸,配制250 mL物质的量浓度为0.46 molL﹣1的硫酸。
(1)需要量取该浓硫酸的体积为_______mL。
(2)实验需要以下步骤:
①定容 ②量取 ③摇匀 ④洗涤 ⑤转移 ⑥冷却 ⑦计算 ⑧装瓶 ⑨稀释
进行顺序为_______。
(3)下列操作使所配溶液的物质的量浓度偏高的是________。
A.往容量瓶中转移溶液时有少量液体溅出
B.未洗涤稀释浓H2SO4的小烧杯
C.定容时俯视刻度线
D.洗净容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
【答案】6.3 ⑦②⑨⑥⑤④①③⑧ C
【解析】
(1)根据n=cV计算。
(2)根据配制一定物质量浓度的溶液的步骤分析;
(3)根据c=![]() 进行判断。
进行判断。
(1)浓硫酸的浓度为![]() ,配制250mL物质的量浓度为0.46molL-1的硫酸需要硫酸的物质的量为:0.46mol·L-1×0.25L=0.115mol,需要浓硫酸的体积为:
,配制250mL物质的量浓度为0.46molL-1的硫酸需要硫酸的物质的量为:0.46mol·L-1×0.25L=0.115mol,需要浓硫酸的体积为:![]() =0.00625L=6.25mL,所以需要选用10mL量筒,但是10mL量筒只能精确到小数点后一位,故需要量取该浓硫酸的体积为6.3mL;
=0.00625L=6.25mL,所以需要选用10mL量筒,但是10mL量筒只能精确到小数点后一位,故需要量取该浓硫酸的体积为6.3mL;
(2)配制一定物质量浓度的溶液的正确步骤是:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶;故进行顺序为⑦②⑨⑥⑤④①③⑧;
(3)A. 往容量瓶中转移溶液时有少量液体溅出,会导致部分溶质损失,使所配溶液的物质的量浓度偏低,故A错误;
B. 未洗涤稀释浓H2SO4的小烧杯,会导致部分溶质损失,使所配溶液的物质的量浓度偏低,故B错误;
C. 定容时俯视刻度线,会导致定容时溶液体积偏小,使所配溶液的物质的量浓度偏高,故C正确;
D. 洗净容量瓶未干燥即用来配制溶液,对实验结果没有影响,故D错误;
E. 定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,会导致定容时溶液体积偏大,使所配溶液的物质的量浓度偏低,故E错误;
正确答案是C。


科目:高中化学 来源: 题型:
【题目】漂白粉主要成分可用下式表示:
Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为
A、7.5 B、8.0 C、9.5 D、11.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构和性质的说法错误的是
A. 分子式为C5H10O2且能与 NaHCO3反应放出气体的结构共有4种
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 苯甲酸(![]() )分子中所有原子可能位于同一平面
)分子中所有原子可能位于同一平面
D. 1mol盐酸美西律( )最多可与3 mol H2发生加成
)最多可与3 mol H2发生加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧1g乙炔(C2H2)生成二氧化碳和液态水,放出热量50kJ, 则这一反应的热化学反应方程式为( )
A. 2C2H2(g)+ 5O2(g) ═4CO2(g)+ 2H2O(l) ΔH= +50kJ/mol
B. C2H2(g)+ 5/2O2(g)═2CO2(g)+ H2O(l) ΔH= +1300kJ/mol
C. 2C2H2+ 5O2═4CO2+ 2H2O ΔH=-2600kJ
D. 2C2H2(g)+ 5O2(g)═4CO2(g)+ 2H2O(l) ΔH=-2600kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H < -57.3kJmol-1
BaSO4(s)+H2O(l) △H < -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O3比O2稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应,都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如下图所示,则比较下列大小关系:
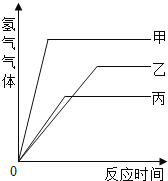
(1)三种金属的活动性由强到弱的顺序为:________________________。
(2)三种金属反应时消耗硫酸的质量由少到多的顺序为:_____________。
(3)三种金属的相对原子质量由大到小的顺序为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,充入1molN2和3molH2,并在一定温度和压强下,使其发生反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH= -92.4 kJ·mol-1。回答下列问题:
2NH3(g) ΔH= -92.4 kJ·mol-1。回答下列问题:
(1)若保持容器容积不变,再向其中充入1molN2,反应速率会________(填“加快”“减慢”或“不变”,下同),理由是____________。
(2)若保持容器容积不变,再向其中充入1molHe,反应速率会________,理由是________。
(3)若保持容器内气体压强不变,再向其中充入1molHe,反应速率会________,理由是___________。
(4)加入催化剂,反应速率会________,理由是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,美国食品药品监督管理局批准为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:
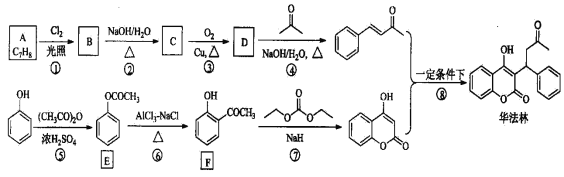
请回答下列问题:
(1)A的名称为_____________________,E中官能团名称为____________________。
(2)B的结构简式为___________________________。
(3)由C生成D的化学方程式为________________________________________。
(4)⑤的反应类型为____________,⑧的反应类型为_______________。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有__________种。a.能与FeCl3溶液发生显色反应; b.能发生银镜反应;其中核磁共振氢谱为五组峰的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义。
(1)用CO可以合成甲醇。已知:
CH3OH(g)+3/2O2(g)===CO2(g)+2H2O(l) ΔH=-764.5 kJ·mol-1
CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
则CO(g)+2H2(g) ![]() CH3OH(g) ΔH=______kJ·mol-1。
CH3OH(g) ΔH=______kJ·mol-1。
(2)下列措施中能够增大上述合成甲醇反应速率的是________(填写序号)。
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将CH3OH从反应混合物中分离出来
(3)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系
如右图所示。
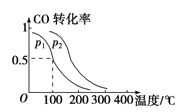
①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=________;
③在其他条件不变的情况下,再增加a mol CO和2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(4)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:_____________________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下。请写出开始时阳极反应的电极反应式:_________________。
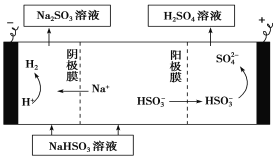
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com