
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
| 盐酸 分子式:HCl 相对分子质量:36.5,密度:1.19 g·cm-3 HCl的质量分数:36.5% |
(1)11.9 (2)BD (3)①16.8 ②a.B b.B (4)①25 ②C
解析试题分析:(1)根据c=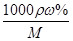 可知,该浓盐酸中HCl的物质的量浓度c=
可知,该浓盐酸中HCl的物质的量浓度c=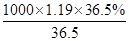 mol/L=11.9mol/L。
mol/L=11.9mol/L。
(2)溶液是均一、稳定的混合物,所以取用任意体积的该盐酸溶液时,A、根据n=cV可知,溶液中HCl的物质的量与溶液的体积有关系,A不正确;B、溶液的浓度是不变的,总是11.9mol/L,B正确;C、溶液中Cl-的数目与氯化氢的物质的量有关系,因此与溶液的体积有关系,C不正确;D、溶液的密度是溶液的性质,与溶液的体积无关系,D正确,答案选BD。
(3)①根据稀释过程中溶质的质量不变可知,配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸需要该浓盐酸的体积=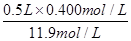 =0.0168L=16.8ml。
=0.0168L=16.8ml。
②根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。a.用量筒量取浓盐酸时俯视观察凹液面,则浓盐酸的偏小,因此所配溶液的浓度偏低,答案选B;b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,则溶液的体积增加,所以所配溶液的浓度偏低,答案选B。
(4)①0.4 g NaOH的物质的量=0.4g÷40g/mol=0.01mol,则根据方程式HCl+NaOH=NaCl+H2O可知,消耗氯化氢的物质的量是0.01mol,因此需要该盐酸的体积=0.01mol÷0.400mol/L=0.025L=25ml。
②A、浓盐酸挥发,浓度不足,则在氢氧化钠的物质的量不变的条件下,消耗盐酸溶液的体积偏大,A不正确;B、配制溶液时,未洗涤烧杯,则导致盐酸的浓度偏小,因此在氢氧化钠的物质的量不变的条件下,消耗盐酸溶液的体积偏大,B不正确;C、配制溶液时,俯视容量瓶刻度线,则容量瓶中溶液的体积偏小,因此在氢氧化钠的物质的量不变的条件下,消耗盐酸溶液的体积偏小,C正确;D、加水时超过刻度线,用胶头滴管吸出,则导致盐酸的浓度偏小,因此在氢氧化钠的物质的量不变的条件下,消耗盐酸溶液的体积偏大,D不正确,答案选C。
考点:考查物质的量浓度的有关计算、配制、误差分析以等


科目:高中化学 来源: 题型:填空题
WO3可用于制备电阻元件、电子射线屏等。其工业生产流程如下: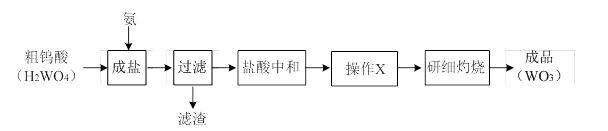
(1)操作X的目的是为了获得纯净的仲钨酸铵晶体,该操作包括:将用盐酸中和后的溶液 、冷却结晶、 、低温烘干。
(2)实际工业生产中,粗仲钨酸铵晶体(含少量NH4Cl晶体)可不经提纯就直接灼烧,其原因是 。
(3)已知:仲钨酸铵晶体[x(NH4)2O·yWO3·zH2O]受热分解的化学方程式如下:
x(NH4)2O·yWO3·zH2O→WO3 +NH3↑+H2O↑(未配平)。
某同学为测定仲钨酸铵晶体的组成,进行如下实验:
①准确称取16.21g样品,研细灼烧;
②将产生的气体通入装有碱石灰干燥管,充分吸收称得干燥管增重1.44g;
③称量冷却后的固体质量为13.92g。
通过计算确定此仲钨酸铵晶体的化学式(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室要配制1mol/L的稀硫酸250mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸 mL
(2)配制时,必须使用的仪器有 (填代号) 还缺少的仪器是 。
①烧杯 ②100 mL量筒 ③20 mL量筒 ④1000 mL容量瓶 ⑤250 mL容量瓶 ⑥托盘天平(带砝码) ⑦玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是 、 。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”)
①没有洗涤烧杯和玻璃棒。 。
②如果加水超过了刻度线,取出水使液面恰好到刻度线。 。
③容量瓶没有干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)37Cl—离子结构示意图 ,质量相等的两种物质SO2和SO3,所含氧原子个数之
为 ;
(2)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为 ,则含R 8.0g 的NaR的物质的量为 ;
(3)在标准状况下,4.8g甲烷(CH4)所占的体积为_________L,它与标准状况下________L硫化氢(H2S)含有相同数目的氢原子;
(4)在100g浓度为18 mol·L-1、密度为ρ(g·cm–3)的浓硫酸中加入一定量的水稀释成9mol·L-1的硫酸,则加入水的体积 100mL(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
用质量分数为98%,密度为1.84g·cm-3的浓硫酸配制l mol/L稀硫酸100mL,其操作有以下各步:
①用量筒量取 mL浓硫酸
②洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
③将稀释、冷却后的硫酸转入100 mL容量瓶中
④将浓硫酸倒入盛有水的烧杯中稀释、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)第①步操作中应用量筒量取 mL浓硫酸;应选择 mL量筒(填5、10或50)。
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是 。
(3)正确的操作顺序是(用序号填写) 。
(4)下列操作会使实际浓度偏高,偏低还是不变,请填写:
1).摇匀后,液面低于刻度线,没有再加水;
2).移液过程中,不小心溅出少量溶液;
3).定容时,如果俯视刻度线,配制的硫酸浓度将
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为________。
(3)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断B可能是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将2.3克钠投入到水(滴有酚酞)中,反应结束后,溶液是0.1升。则:
(1)反应过程中,可以发现钠浮在水面,说明钠的密度 (填“大于”“小于”“等
于”)水的密度,溶液最后显 色。
(2)化学反应方程式是 。
(3)求最后溶液的物质的量浓度是多少?(写出解题过程)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题: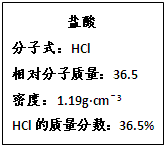
(1)该浓盐酸中HCl的物质的量浓度为___________。若用KMnO4。氧化上述HCl。其反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(2)1molKMnO4完全反应,反应后溶液的体积为2L,则所得产物中Cl-的物质的量浓度为____________。
(3)8molHCI完全反应,产生的Cl2在标准状况下的体积为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
写出下列物质的电子式,有结构式的请写出结构式
①氨气 、 ②氯化铵 、
③干冰 、 ④苛性钠 、
⑤冰 、 ⑥过氧化钠 、
⑦双氧水 、 ⑧HClO 、
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com