
����Ŀ��50 mL 0.5 mol��L��1��������50 mL 0.55 mol��L��1��NaOH ��Һ����ͼ��ʾ��װ��(�������ȼ�)�н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���ش��������⣺
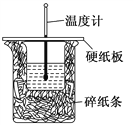
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��______________��
��2���ձ���������ֽ����������___________________��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ__________(����ƫ������ƫС������Ӱ����)��
��4��ʵ���и��� 60 mL 0.50 mol�� L��1������� 50 mL 0.55 mol�� L��1�� NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������________(��������������������)�������к���________(��������������������)��
��5��ʵ���и��� 50mL 0.50 mol�� L��1�Ĵ���� 50 mL 0.55 mol�� L��1�� NaOH��Һ���з�Ӧ��������ʵ����ȣ������к���________(��������������������)����������______________________________��
���𰸡� ���β�������� ����ʵ������е�������ʧ ƫС ����� ��� ����� ���������Ҫ��������
��������(1).�������ȼƵĹ����֪����װ��ȱ�ٵIJ��������ǻ��β�����������ʴ�Ϊ�����β����������
(2).�к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�������С�ձ�֮��������ֽ�����Լ���ʵ������е�������ʧ���ʴ�Ϊ������ʵ������е�������ʧ��
(3).���ձ����粻��Ӳֽ�壬����һ��������ɢʧ����õ��к�����ֵ����ƫС���ʴ�Ϊ��ƫС��
(4).��Ӧ�ų����������������Լ�������Ķ����й�������60mL0.50molL1������Һ��50mL0.55molL1NaOH��Һ���з�Ӧ��������ʵ�����������ˮ�������������ų�������Ҳ���࣬�����к���ָ����ǿ���ǿ�Ӧ����1molˮʱ�ų�����������������������������60mL0.50molL1�������������Һ����ʵ�飬����к�����ֵ��ȣ��ʴ�Ϊ������ȣ���ȣ�
(5).���������ᣬ�������Ϊ���ȹ��̣������ô������������Һ��Ӧ���ų�����������ƫ�٣���õ��к��ȵ���ֵ��ƫС���ʴ�Ϊ������ȣ����������Ҫ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��糧�ղ����ķ�ú�ҵ���Ҫ�ɷ�ΪSiO2��Al2O3��FeO��Fe2O3��MgO��TiO2�ȡ��о�С���������ۺϴ������������£�
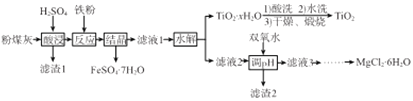
��֪���١������������Ҫ��TiOSO4��ʽ���ڣ�ǿ�����TiOSO4����Һ�н��ܵ���SO42-��һ��������
�������£�Ksp[Al(OH)3]=1.0��10-34��Ksp[Fe(OH)3]=4.0��10-38��Ksp[Mg(OH)2]=1.0��10-11
��ش��������⣺
(1)�������ʱTiO2������Ӧ�����ӷ���ʽΪ_______________��
(2)����Ӧ��ʱ�������۵�����Ϊ_______________��
(3)���ᾧ���������70�����ң��¶ȹ��ᵼ�µĺ��Ϊ_____________��
(4)��ˮ�⡱��Ӧ�����ӷ���ʽΪ______________������TiO2xH2O ����������ϴ��Ŀ��Ϊ____________��
(5)Ϊʹ����2������ȫ(��Һ������Ũ��С��10-5mol/L)���衰��pH����СΪ________��
(6)ʵ������MgCl2��Һ�Ʊ�MgCl26H2O������еIJ���Ϊ_____�����½ᾧ�����ˡ�ϴ�ӡ����
(7)FeSO47H2O��Ʒ���ȵIJⶨ��ȡa g��Ʒ����ˮ���bmL.��Һ�����ữ��cmol/LKMnO4����Һ�ζ����ﵽ�ζ��յ�ʱ���ı�Һ�����ΪdmL����Ʒ��FeSO47H2O����������Ϊ____ ���ô���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.��ϩ�Ľṹ��ʽ��CH2CH2
B.������Ҵ����������Ʒ�Ӧ�������壬������̼���Ʒ�Ӧ��������
C.C4H10��һ��ȡ���ﹲ��4��
D.��״���£�22.4L�ȷ��к���3molClԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ0.1mol/L NaOH��Һ450mL��0.5mol/L������Һ500mL��������������Һ����������ش��������⣺
��1����ͼ��ʾ��������������Һ�϶�����Ҫ����______________��(�����)������������Һ�����õ��IJ���������______________(����������)��

��2������NaOHʱ����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ��______0.1mol/L(����ڡ��������ڡ���С�ڡ�)��
��3�����ݼ����֪��������������Ϊ98%���ܶ�Ϊ1.84g/cm3��Ũ��������Ϊ_____________mL(����������һλС��)����ʵ����������������ȷ��������Ͳ��ȡŨ����ʱ���ӿ̶��ߣ������������ҺŨ��_____________0.5mol/L(����ڡ��������ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����ֱ�����Na��O��H�γɵĵ��ʣ�A��B��C����H��0��Na����Ԫ���е����ֻ�������ɵĻ�������ֵ����뻯����֮�ʴ�����ͼ��ʾ��ת��Цϵ��

��ش�
��1��д���������ʵĻ�ѧʽA________��B_________��C_______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��
�����ʼ�+������B_____________________________��
��������A+������B___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4molL��1��KOH��Һ100mL��ȡ��5mL����5mL��Һ��K+Ũ��Ϊ�� ��
A.4 molL��1
B.0.2molL��1
C.2 molL��1
D.0.4 molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ض�ʳƷ�Ƿ����Ӻ��������Ӽ������˶������λ�����г��õ��������������������(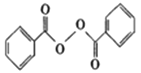 )Ҳ�����á�������һ���Ա�Ϊԭ�Ϻϳɹ����������������̣�
)Ҳ�����á�������һ���Ա�Ϊԭ�Ϻϳɹ����������������̣�
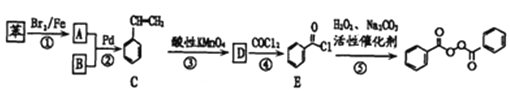
��֪��![]()
��ش��������⣺
��1����ҵ������B��Ҫ��Դ��_____������D��������_______��ÿ��C�����������____��ԭ�ӹ�ƽ�档
��2����Ϲ������������ṹ������������������������Ϊ������ԭ����________��
��3��д����Ӧ�ڵĻ�ѧ����ʽ________����Ӧ����Ϊ________��
��4��ij����FΪ��������������ͬ���칹�壬ͬʱ��������������F��ͬ���칹����______�֣���д�����������ֲ�ͬ��ѧ��������ԭ�ӵĽṹ��ʽ:____________��
�� ����������![]() ���ṹ��Ԫ.��������״�ṹ
���ṹ��Ԫ.��������״�ṹ
�� ��һ���������ܷ���������Ӧ
�� 1mol F��������4mol NaOH
��5����д���Ա���ϩΪԭ�ϣ��ϳ�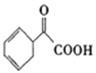 �����̣����Լ���ѡ��ע����Ӧ������____________
�����̣����Լ���ѡ��ע����Ӧ������____________
ʾ�����£�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼʾ����3��Բ�����ɵ�����ϵͼ������IΪ��Բ��II��III�ֱ�Ϊ��Բ֮�ڵ�СԲ������ѡ���з�����������ϵ����( )

A. I: DNA II: RNA III:����
B. I����ԭ���� II������ III������
C. I���̴� II�����̴� III��ά����D
D. I�������� II��ø III������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ����У�ǰ���ǵ���ʣ������Ƿǵ���ʵ�����ǣ� ��
A.NaCl��Cl2
B.NaHCO3������
C.Ba��OH��2��HCl
D.H2SO4������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com