
【题目】标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂
(1)2K2S + K2SO3 + 3H2SO4= 3K2SO4 + 3S↓+ 3H2O _______氧化剂_______
(2)2KMnO4 +5H2O2 + 3H2SO4 = K2SO4+2MnSO4+5O2↑ + 8H2O _______ 氧化剂_______
科目:高中化学 来源: 题型:
【题目】用18.4 mol·L-1的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒、②烧瓶、③烧杯、④胶头滴管、⑤量筒、⑥容量瓶、⑦托盘天平。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)________。
(2)经计算,需量取浓H2SO4 ________mL。现有①10 mL、②50 mL、③100 mL三种规格的量筒,你选用的量筒是________(写序号)。
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到______ mL的容量瓶中。
(4)在配制过程中,其他操作都准确,下列操作中能引起误差偏高的有________(填代号)。
①定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
②转移前,容量瓶中含有少量蒸馏水
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线
(5)在下图的配制过程示意图中,正确的是(填写序号)_______。
A.称量
B.溶解
C.转移
D.定容![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
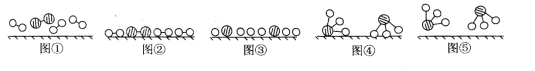
(1)图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______,_______。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g);ΔH=-1266.8kJ/mol,N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ/mol,氨催化氧化的热化学方程式为_________________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
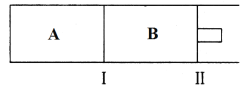
①当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为________________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将______________(填“正向”、“逆向”或“不”)移动。
②向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为_____________。
(4)以CO和O2为电极燃料,以熔融K2CO3为电解质组成燃料电池,请写出该电池的负极反应方程式_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)用作香料的原料,它可由A合成得到:
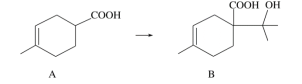
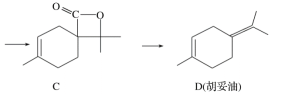
下列说法正确的是
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 有机物C的所有同分异构体中可能有芳香族化合物存在
D. 1 mol有机物A中含有6.02×1023个双键.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物F(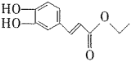 )在自身免疫性疾病的治疗中有着重要的应用,工业上以乙烯和芳香族化合物B为基本原料制备F的路线图如下:
)在自身免疫性疾病的治疗中有着重要的应用,工业上以乙烯和芳香族化合物B为基本原料制备F的路线图如下:
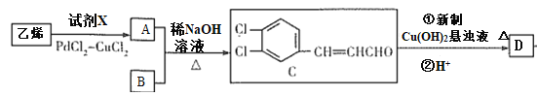
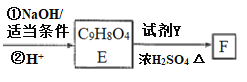
已知:RCHO+CH3CHO![]() RCH=CHCHO
RCH=CHCHO
(1)乙烯生成A的原子利用率为100%,则X是___________(填化学式),F中含氧官能团的名称为___________。
(2)E→F的反应类型为___________,B的结构简式为___________,若E的名称为咖啡酸,则F的名称是___________。
(3)写出D与NaOH溶液反应的化学方程式:_________________________________。
(4)E的同系物G比E多一个碳原子,G有多种同分异构体,符合下列条件的同分异构体有___________种
①能发生水解反应、银镜反应且1mol该物质最多可还原出4 mol Ag
②遇FeCl3溶液发生显色反应
③分子中没有甲基,且苯环上有2个取代基
(5)以乙烯为基本原料,设计合成路线合成2-丁烯酸,写出合成路线:______________________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高温下, Al与Fe2O3发生铝热反应后得到的固体混合物中主要含有Al2O3、Fe,还含有少量Fe2O3。从该样品中固体混合物分离出Al2O3,并回收Fe和Fe2O3的流程如下:

已知:NaAlO2 + CO2 + 2H2O = Al(OH)3↓ + NaHCO3
回答下列问题:
(1)固体①的成分是__________。溶液②的溶质是____________。
(2)加入过量NaOH溶液时,发生反应的离子方程式是__________。
(3)白色固体②与NaOH溶液反应的离子方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是___。
(2)反应①的化学方程式为___。
(3)反应③的离子方程式为___。
(4)反应⑧的化学方程式为___。
(5)反应⑥过程中的现象是____。
(6)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下下列溶液中的指定离子与100 mL 3.9 mol/L Ba(NO3)2溶液所含NO3-物质的量浓度相同的是
A.390 mL 0.1 mol/L MgCl2溶液中的Cl-
B.200 g 浓度为26%,密度为1.2g/mLNaOH溶液中的OH-
C.50 mL 7.8 mol/L Al2(SO4)3溶液中的SO42-
D.200 mL 3.9 mol/L CaCl2溶液中的Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业上使用![]() 溶液蚀刻铜箔制造印刷电路板。在该制备工艺中,为了实现资源再生,减少污染,某兴趣小组提出废液处理和资源回收的过程如下:
溶液蚀刻铜箔制造印刷电路板。在该制备工艺中,为了实现资源再生,减少污染,某兴趣小组提出废液处理和资源回收的过程如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液![]() ,同时鼓入足量的空气。
,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4×10-38,回答下列问题:
(1)![]() 蚀刻铜箔反应的离子方程式为______;过程Ⅰ加入铁屑的主要作用是______
蚀刻铜箔反应的离子方程式为______;过程Ⅰ加入铁屑的主要作用是______
(2)过程Ⅱ中鼓入足量的空气发生反应的化学方程式为______
(3)过程Ⅱ中调节溶液的![]() 为5,金属离子浓度为______。(列式计算)
为5,金属离子浓度为______。(列式计算)
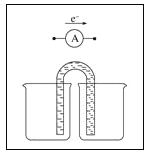
(4)另一兴趣小组将制造印刷电路板![]() 蚀刻铜箔的反应设计成一个原电池。请将方框中实验装置图补充完整,并作相应标注(标出电极材料、电解质溶液)。限选材料:
蚀刻铜箔的反应设计成一个原电池。请将方框中实验装置图补充完整,并作相应标注(标出电极材料、电解质溶液)。限选材料:![]() ,
,![]() ,
,![]() ,
,![]() :铜片,铁片,锌片,石墨和导线。
:铜片,铁片,锌片,石墨和导线。
(5)废旧印刷电路板经粉碎分离能得到非金属粉末和金属粉末,也可回收利用实现资源再生,减少污染。印刷电路板的金属粉末用![]()
![]() 和
和![]()
![]() 的混合溶液处理,溶出印刷电路板金属粉末中的铜。控制其他条件相同时,测得不同温下铜的平均溶解速率(见下表)。
的混合溶液处理,溶出印刷电路板金属粉末中的铜。控制其他条件相同时,测得不同温下铜的平均溶解速率(见下表)。
温度 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率 |
|
|
|
|
|
|
|
①当温度高于![]() 时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。
时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。
②在提纯后的![]() 溶液中加入一定量的
溶液中加入一定量的![]() 和
和![]() 溶液,加热,生成
溶液,加热,生成![]() 沉淀。制备
沉淀。制备![]() 的离子方程式是______。
的离子方程式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com