
【题目】能量之间可相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。
设计两种类型的原电池,探究其能量转化效率。限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
(1)完成原电池甲的装置示意图(如图所示),并做相应标注。要求:在同一烧杯中,电极与溶液含相同的金属元素。

(2)以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极 。
(3)甲乙两种原电池中可更有效地将化学能转化为电能的是 ,其原因是 。
【答案】(1)如图所示(合理即可)
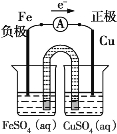
(2)逐渐溶解
(3)甲 甲使用了盐桥,避免负极金属直接与溶液中的铜离子反应而造成能量损失
【解析】(1)由题给材料,结合原电池的构成条件可知,组合的原电池可以为锌铜原电池、锌铁原电池、铁铜原电池。由题图所给电子移动方向可知,左边为负极(较活泼金属)、右边为正极(较不活泼金属),则组合的原电池如图所示。
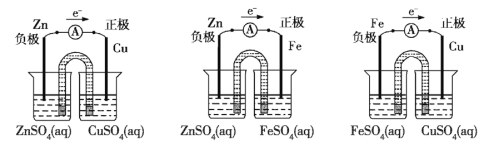
(2)由所给的电极材料可知,当铜片作电极时,铜片一定是正极,则负极是活泼的金属(如Zn或Fe,失去电子发生氧化反应),反应现象是电极逐渐溶解。
(3)甲电池使用了盐桥,避免负极金属直接与溶液中的铜离子反应而造成能量损失,能更有效地将化学能转化为电能。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组同学将氧化还原反应:2KMnO4+10FeSO4+8H2SO4![]() 2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计成原电池(如图),其中甲、乙两烧杯中各物质的物质的量浓度均为 1 mol·L1,盐桥中装有饱和K2SO4溶液。
2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计成原电池(如图),其中甲、乙两烧杯中各物质的物质的量浓度均为 1 mol·L1,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(1)发生氧化反应的烧杯是 (填“甲”或“乙”)。
(2)外电路的电流从 流向 (填“a”或“b”)。
(3)电池工作时,盐桥中的![]() 移向 (填“甲”或“乙”)烧杯。
移向 (填“甲”或“乙”)烧杯。
(4)甲烧杯中发生的电极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图所示:

甲 乙 丙

丁 戊
回答下列问题:
(1)根据原电池原理填写下表:
装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
甲 | |||
乙 | |||
丙 | |||
丁 | |||
戊 |
(2)电极类型除与电极材料的性质有关外,还与 有关。
(3)根据上述电池分析,负极材料是否一定参加电极反应? (填“是”、“否”或“不一定”),用上述电池说明: 。
(4)上述电池放电过程中,电解质溶液酸碱性的变化:甲 ,丙 ,戊 。(均填“酸性减弱”或“碱性减弱”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为________,W、D、E三种元素的简单离子的离子半径由大到小顺序为__________(用离子符号表示)。
(2)由A、B、W三种元素组成的18电子微粒的电子式为_______________。
(3)经测定A2W2为二元弱酸,其酸性比碳酸弱,写出其第一步电离的电离方程式_________________,实验室常用稀硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_____________________________________。
(4)元素D的单质在一定条件下与元素A的单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,该反应的化学方程式为____________。
(5)元素D的某化合物呈淡黄色,可与氯化亚铁溶液反应,生成红褐色沉淀,且无气体生成.则该反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同周期的IIA族与ⅢA族元素的原子序数一定相差1
B. 第三周期非金属元素含氧酸的酸性从左到右依次增强
C. 元素的非金属性越强,其气态氢化物水溶液的酸性越强
D. 镁、铝、铜、铁、钠五种金属元素中,铜和铁属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用胆矾配制0.2mol/L的CuSO4溶液,下列操作正确的是( )
A.取50g胆矾溶于1L水中
B.取50g胆矾溶于水配成1L溶液
C.取32g胆矾溶于水配成1L溶液
D.取无水硫酸铜32g溶于1L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的描述中,正确的是
A.金属钠在氯气中燃烧,有白雾生成
B.铜在氯气中燃烧,生成蓝色的氯化铜颗粒
C.钠投入硫酸铜溶液中,会产生蓝色沉淀
D.钠在空气中燃烧后得到白色粉末状固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com