
����Ŀ����ԭ�ᣨC16H18O9�����нϹ㷺�Ŀ����������������������ã��������ѡ�60%�Ҵ����ݶ��ٸ�Ҷ���õ���ȡҺ����һ�������ԭ��ֲ�Ʒ��һ�ֹ���������ͼ������˵��������ǣ� ��
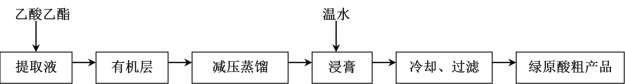
A.��ԭ������ˮ�е��ܽ��С����ˮ�е��ܽ��
B.�õ��л����ʵ�����Ϊ��ȡ��Һ
C.��ѹ�����Ŀ�ķ�ֹ�¶ȹ��ߣ���ԭ�����
D.��ԭ��ֲ�Ʒ����ͨ���ؽᾧ��һ���ᴿ
���𰸡�A
��������
��ԭ��������������������ȡҺ����������������Һ�õ��л��㣬��ѹ����õ���ԭ�ᣬ������ˮ���࣬����ȴ�����˵õ���ԭ��ֲ�Ʒ���Դ˽����⡣
A.�����м�����ˮ���࣬��ȴ�����˵õ���ԭ��ֲ�Ʒ����֪��ԭ����������ˮ��������ˮ�е��ܽ�ȴ�����ˮ�е��ܽ�ȣ���A����
B.��ԭ��Ϊ�л��ᣬ���������л��ܼ�������������������ԭ�ᱻ��ȡ���л����㣬�л�����ˮ�㻥�����ܵ�Һ��Ӧ���÷�Һ�����룬��B��ȷ��
C.��ԭ����п��������ã���ѹ����ɽ����¶ȣ������¶ȹ��ߵ�����ԭ����ʣ���C��ȷ��
D.����A�ķ�������ԭ��ֲ�Ʒ�����ؽᾧ�ķ�����һ���ᴿ����D��ȷ��
��ѡ��A��


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��������������ƽ�������ص�ʵ�顣
����֪��Na2S2O3+H2 SO4 Na2SO4+SO2��+S��+H2O��ijͬѧ̽��Ӱ�������������ϡ���ᷴӦ���ʵ�����ʱ�����������ϵ��ʵ�飺
ʵ����� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
�� | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
�� | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
�� | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
��1����ʵ��١��ڿ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬���V1=V2=____��V3=___��
��2����V4=10.0��V5=6.0����ʵ��١��ۿ�̽��_____�Է�Ӧ���ʵ�Ӱ�졣
�����÷�Ӧ��I2+2Na2S2O3 Na2S4O6+2NaI�ɶ����ⶨ���������(Mr=158)�Ĵ��ȣ����ڳ�ȡwg��������ƹ�����Ʒ�����250mL����Һ��ȡ25.00mL������ƿ�У�����ָʾ������amol/L�ĵ�ˮ�ζ������ĵ�ˮb mL����
��3���ζ�ʱ������ˮע��___�����ʽ����ʽ�����ζ����У��ζ�Ӧѡ���ָʾ����____���ζ��յ������Ϊ________��
��4�����ڸõζ�ʵ����йز�������������ȷ����____��
a���ζ�ǰ��Ҫ�ö�Ӧװ�����Һ��ϴ��ƿ�͵ζ���
b���ζ������У���Һ�ε���ƿ�⣬��ʹ����õĽ��ƫ��
c���ζ���ʼʱ�ζ��ܼ��������ݣ��ζ�������������ʧ����ô��Ƚ�ƫС
d���ζ�ǰ���Ӷ������ζ�����ʱƽ�Ӷ�����������õĴ��Ƚ���ƫС
��5����Ʒ����������ƴ��ȵı���ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ����Ҫ��ҽҩ�м��壬��ṹʽ��ͼ��ʾ������Q��W��X��Y��ZΪԭ�Ӱ뾶���ε����Ķ�����Ԫ�أ�Q��X��Z������������ͬ���ڡ�����˵���������
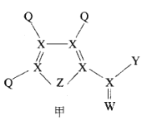
A.�ǽ����ԣ�X<Z<W
B.Q��W�γɻ�����ķе����Q��X�γɻ�����ķе�
C.��������г�Q�⣬����ԭ�Ӿ�����8�����ȶ��ṹ
D.0.1 molL-1 ����������Ӧˮ��������ԣ�Y> Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0. 100 0 mol��L-1 NaOH��Һ�ζ�20. 00 mL 0.100 0 mol��L-1 CH3COOH��Һ���õζ�������ͼ������˵����ȷ����(����)

A.�����ʾ��Һ�У�c(CH3COO-)+2c(OH-)=c(CH3COOH)+c(H+)
B.�����ʾ��Һ�У�c(Na+)=c(CH3COOH)+c(CH3COO-)
C.�ζ������п��ܳ��֣�c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.�����ʾ��Һ�У�c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���������[Co(NH3)6]Cl3�dzȻ�ɫ�������Ǻϳ�����һЩ����������ԭ�ϡ����ú��ܷ���(������Fe��Al������)��ȡ[Co(NH3)6]Cl3�Ĺ���������ͼ���ش��������⣺
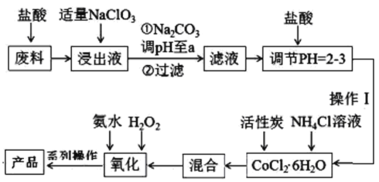
��֪����������Һ���к���Co2����Fe2����Fe3����Al3+��
��Ksp��Co(OH)2��=6��10-15��Ksp��Co(OH)3��=1.6��10-44
(1)��������NaClO3����������___��������Ӧ�����ӷ���ʽΪ___��
(2)����Na2CO3��pH��a�����������ֳ������ֱ�Ϊ___(�ѧʽ)��
(3)������IJ������___��___����ѹ���ˡ�
(4)������������������Ӧ�ȼ���___(������ˮ������H2O2��)����ˮԡ������50��60�棬�¶Ȳ��ܹ��ߣ�ԭ����___��д�������������跢����Ӧ�����ӷ���ʽ��___��������̿�����������ù�������г�[Co(NH3)6]Cl3����д������Ȼ�һ���就����[Co(NH3)5Cl]Cl2�����Ȼ��就һˮ����[Co(NH3)5H2O]Cl3���壬�������˴�����___�ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϫ��̸���мǣ��ݸ����龻�������鴦���Դƻ�Ϳ֮�����й��Ŵ����ƻƣ�As2S3�����������Ĵ��֣���ṹ��ͼ��ʾ������˵������ȷ���ǣ� ��
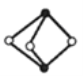
A.As��Sԭ�ӵ��ӻ���ʽ��Ϊsp3
B.AsH3�ķе��NH3�ĵ�
C.��Asͬ�����һ�̬ԭ�Ӻ���δ�ɶԵ�����Ŀ��ͬ��Ԫ��ֻ��V
D.��֪As2F2�����и�ԭ�Ӿ�����8���ӽṹ�������������������ĸ�����Ϊ3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ�ȥ��ʯ����(��CaO)����Һ�е�S2-������ȡʯ��(CaSO42H2O)�ij���������ͼ��
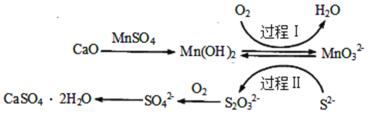
����˵������ȷ����( )
A.��������������������õ�������Mn(OH)2
B.�����£�56gCaO����ˮ���1L��Һ����Һ��Ca2+����ĿΪ6.02��1023��
C.��10L����Һ�е�S2-ת��ΪSO![]() (S2-Ũ��Ϊ320mg��L-1)�������Ϲ���Ҫ0.2mol��O2
(S2-Ũ��Ϊ320mg��L-1)�������Ϲ���Ҫ0.2mol��O2
D.�������У���Ӧ�����ӷ���ʽΪ4MnO![]() +2S2-+9H2O=S2O
+2S2-+9H2O=S2O![]() +4Mn(OH)2��+10OH-
+4Mn(OH)2��+10OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼�IJ�����������ʵ������������ŵ���Ҫ;��֮һ��
(1)Ŀǰ��ҵ��ʹ�õIJ�̼���� NH3 ��(NH4)2CO3�������� CO2 �ɷ������¿��淴Ӧ��
2NH3(l)��H2O(l)��CO2(g) ![]() (NH4)2CO3(aq) K1
(NH4)2CO3(aq) K1
NH3(l)��H2O(l)��CO2(g) ![]() NH4HCO3(aq) K2
NH4HCO3(aq) K2
(NH4)2CO3(aq)��H2O(l)��CO2(g) ![]() 2NH4HCO3(aq) K3
2NH4HCO3(aq) K3
�� K3��________(�ú� K1��K2 �Ĵ���ʽ��ʾ)��
(2)���� CO2 �Ʊ���ϩ���ҹ���Դ�����һ����Ҫս�Է��������£�
����һ��
CO2 ������ϳ���ϩ���䷴ӦΪ��2CO2(g)��6H2(g) ![]() C2H4(g)��4H2O(g) ��H��a kJ��mol��1��ʼʱ�� n(CO2)��n(H2)��1��3��Ͷ�ϱȳ���20 L�ĺ����ܱ������У���ͬ�¶���ƽ��ʱH2��H2O�����ʵ�����ͼ����ʾ��
C2H4(g)��4H2O(g) ��H��a kJ��mol��1��ʼʱ�� n(CO2)��n(H2)��1��3��Ͷ�ϱȳ���20 L�ĺ����ܱ������У���ͬ�¶���ƽ��ʱH2��H2O�����ʵ�����ͼ����ʾ��

��a______0(ѡ����>������<��)��
������˵����ȷ����______(����ĸ���)��
A ��ʹ�ô������ɽ��ͷ�Ӧ��ܣ��ӿ췴Ӧ����
B ��������������ʱ�������������ݻ����� v����С��v������
C ����������ڻ�������ܶȲ���ʱ��ı�ʱ��˵����Ӧ�Ѵ�ƽ��
��393 K�£�H2��ƽ��ת����Ϊ________(������λ��Ч����)��
��393 K�£��÷�Ӧ�ﵽƽ������������а� n(CO2)��n(H2)��1��3 Ͷ�� CO2 �� H2 ����n(H2)/n(C2H4)��____(�������������������������С��)��
��������
�ö��Ե缫���ǿ���ԵĶ�����̼ˮ��Һ�ɵõ���ϩ����ԭ����ͼ����ʾ��
��b�缫�ϵĵ缫��ӦʽΪ_______��
��װ����ʹ�õ���__________(����������������)���ӽ���Ĥ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���仯�����ڹ�ũҵ�������ճ��������й㷺��Ӧ�ã������о�������Ҫ���塣
�ش��������⣺
��1�����û���̿��___���ÿ�ȥ��ˮ�е��������ʡ�
��2��̿�ڿ��Ի�����ӵõ����(O*)��������Կ��ٽ�SO2����ΪSO3���������е������仯��ͼ��ʾ��
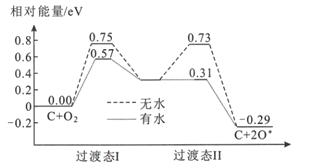
���������ˮʱ�Ļ�ܽ�����___eV����������γɹ����У�̿����___���á�
��3����֪��CO(g)+2H2(g)![]() CH3OH(g) H�����ⶨ��ͬ�¶��¸÷�Ӧ��Ũ��ƽ�ⳣ�����£�
CH3OH(g) H�����ⶨ��ͬ�¶��¸÷�Ӧ��Ũ��ƽ�ⳣ�����£�

�ٸ÷�Ӧ����H___0(����>������<")��250��ʱ��ijʱ�̲�÷�Ӧ��ϵ��c(CO)=0.4mol��L-1��c(H2)=0.4mol��L-1��c(CH3OH)=0.8mol��L-1�����ʱv��__v��(����>������=������<��)��.
��ij�¶��£���2L���������У�����0.8molCO��1.6molH2��ѹǿΪp��tmin��ﵽƽ�⣬���ѹǿΪ![]() P����v(H2)=____mol��L-1��min-1��ƽ��ʱ��Kp=____��
P����v(H2)=____mol��L-1��min-1��ƽ��ʱ��Kp=____��
��4��������Ա����˼���ȼ�ϵ�ص�ⱥ��ʳ��ˮװ����ͼ��ʾ����صĵ�����Dz�����Y2O3��ZrO2�Ĺ��壬���ڸ����´���O2-��
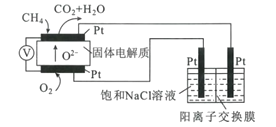
�ٸõ�ع���ʱ������Ӧ����ʽΪ____��
���øõ�ص��100mL����ʳ��ˮ������������������������ֱ�ΪV1L��V2L(��״��)����V1>V2������������Һ��c(OH-)=____mol��L-1(���������ܽ����Һ����仯)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com