
【题目】绿矾是含有一定结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
Ⅰ.为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置进行实验。
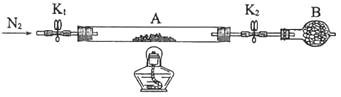
(1)仪器B的名称是______。
(2)将下列实验操作步骤正确排序______(填标号);重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量A
f.持续通氮气,冷却至室温
(3)根据实验记录,计算绿矾化学式中结晶水数目x=______(列式表示)。
Ⅱ.已知某些硫酸盐受热易分解为相应的氧化物,为探究硫酸亚铁的分解产物,将实验Ⅰ中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红棕色粉末。
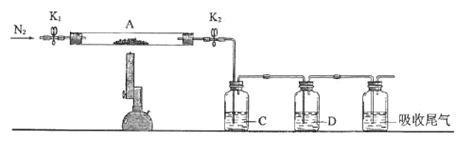
(4)C中盛放BaCl2溶液,并在实验中观察到有白色沉淀生成,其作用为:______。
(5)D中盛放的溶液为______(填标号)。
a.品红 b.NaOH c.Ba(NO3)2 e.浓H2SO4
(6)写出硫酸亚铁高温分解反应的化学方程式______。
【答案】球形干燥管 dabfce ![]() 检验FeSO4分解是否会生成SO3 a 2FeSO4
检验FeSO4分解是否会生成SO3 a 2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
【解析】
Ⅰ.(1)由仪器的图形可知B为干燥管,故答案为:干燥管;
(2)实验时,为避免亚铁被氧化,应先通入氮气,排出生成的水,冷却后注意关闭开关,冷却至室温再称量固体质量的变化,则正确的顺序为dabfce,故答案为:dabfce;
(3)直至A恒重,记为m3 g,应为FeSO4和装置的质量,则m(FeSO4)=(m3-m1),m(H2O)=(m2-m3),则n(H2O)=![]() 、n(FeSO4)=
、n(FeSO4)=![]() ,结晶水的数目等于
,结晶水的数目等于![]() =
=![]() ,故答案为:
,故答案为:![]() ;
;
Ⅱ.实验后反应管中残留固体为红色粉末,说明生成Fe2O3,则反应中Fe元素化合价升高,S元素化合价应降低,则一定生成SO2,可知硫酸亚铁高温分解可生成Fe2O3、SO3、SO2,C为氯化钡,用于检验SO3,可观察到产生白色沉淀,D为品红,可用于检验SO2,品红褪色。
(4)C中盛放BaCl2溶液,并在实验中观察到有白色沉淀生成,其作用为:检验FeSO4分解是否会生成SO3。
故答案为:检验FeSO4分解是否会生成SO3;
(5)D中盛放的溶液为品红,故选:a。
(6)硫酸亚铁高温分解可生成Fe2O3、SO3、SO2,反应的化学方程式2FeSO4![]() Fe2O3+SO2↑+SO3↑。故答案为:2FeSO4
Fe2O3+SO2↑+SO3↑。故答案为:2FeSO4![]() Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。


科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去) 如下所示:
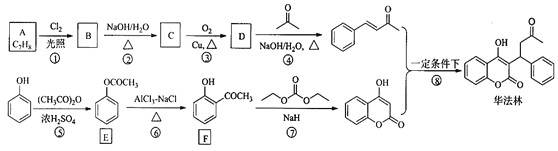
回答下列问题:
(1)A 的名称为________,E 中官能团名称为________。
(2)B 的结构简式为________。
(3)由 C 生成 D 的化学方程式为___________
(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F 的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与 FeCl3 溶液发生显色反应 b.含有-CHO
其中核磁共振氢谱为五组峰的结构简式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在TiCl3的饱溶液中通入HCl至饱和,再加入乙醚生成绿色晶体,如果不加入乙醚,直接通入HCl得到的是紫色晶体,已知两种晶体分子式均为TiCl3·6H2O,配位数都是6的配合物,分别取0.01mol两种晶体在水溶液中用过量AgNO3处理,绿色晶体得到的白色沉淀质量为紫色晶体得到沉淀质量的![]() ,则下列有关说法不正确的是( )
,则下列有关说法不正确的是( )
A.该绿色晶体配体是氯离子和水,它们物质的量之比为1:5
B.紫色晶体配合物的化学式为[Ti(H2O)6]Cl3
C.上述两种晶体的分子式相同,但结构不同,所以性质不同
D.0.01mol紫色晶体在水溶液中与过量AgNO3作用最多可得到2.78g沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | Na2S溶液滴入AgCl浊液中 | 热铜丝插入稀硝酸中 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 沉淀由白色逐渐变为黑色 | 产生无色气体,随后变为红棕色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.过渡金属元素性质研究在无机化学中所占的比重越来越大。
(1)铜元素在周期表的位置是______。
(2)比较NH3和[Cu(NH3)2]2+中H-N-H键角的大小:NH3______[Cu(NH3)2]2+(填“>”或“<”),并说明理由______。
(3)铜金合金是一种储氢材料,晶胞参数anm,面心立方堆积,铜原子在晶胞的面心位置,金原子在晶胞的顶点位置。已知阿伏加德罗常数的数值为NA,铜、金的摩尔质量分别为M(Cu)、M(Au),该晶体的密度为______g/cm3;氢原子可以进入到铜原子和金原子构成的四面体的空隙中,该材料储满氢后的化学式为______。
(4)研究发现,钒元素的某种配合物可增强胰岛素降糖作用,它是电中性分子,结构如图1,在图中画出由钒离子形成的配合物中的配位键______。
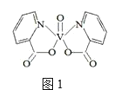
Ⅱ.氮元素可以形成多种化合物。
(5)NO3-的立体构型的名称是______,NO3-的一种等电子体为______。
(6)硫酸和硝酸都是常见的强酸,但性质差异明显:硫酸是粘稠的油状液体,沸点338℃;硝酸是无色液体,沸点仅为122℃,试从氢键的角度解释原因:______。
(7)图2表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的四个顶点(见图3),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是______(填标号)。
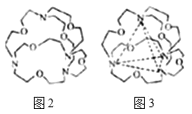
a.CF4 b.CH4 c.NH4+ d.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为①4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )
8Na2CrO4+2Fe2O3+8CO2,②2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O,下列说法正确的是 ( )
A. 反应①和②均为氧化还原反应
B. 反应①的氧化剂是O2,还原剂是FeO·Cr2O3
C. 高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D. 反应①中每生成1 mol Na2CrO4时转移电子3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
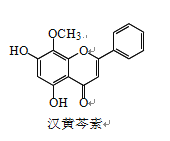
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氯水成分的实验,请回答以下问题:
(1)将足量氯气溶于水制成的饱和氯水呈_______色,说明氯水中含有_______分子。
(2)向氯水中滴加稀硝酸酸化的硝酸银溶液产生的现象是_______,说明氯水中还存在的粒子是_______。
(3)向氯水中加入少量Na2CO3溶液,发现有气泡产生,说明氯水中含有_______;将新制氯水滴加到蓝色石蕊试纸上产生的现象是_______,说明新制氯水中还存在的粒子是_______;由于_______见光易分解,因此氯水需保存在棕色试剂瓶中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入少量水,搅拌均匀,然后加入浓硫酸,快速搅拌,生成疏松多孔的黑色物质。
(1)  (2)
(2)  (3)
(3)  (4)
(4)  (5)
(5) 
请回答下列问题:
①根据上述实验步骤(1)-(5)中,蔗糖与浓硫酸反应的实验现象,浓硫酸表现出的化学性质有____________ (填字母)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
②反应中生成的黑色物质继续与浓硫酸作用,产生两种气体,其中一种气体 X 有刺激性气味,另一种气体 Y 无色无味,写出反应的化学方程式_____________。
③为了在混合气体中检验出 X、Y 这两种气体,提供下列试剂:(试剂可多次使用,不考虑尾气处理)
A.品红溶液 B.澄清石灰水 C.酸性高锰酸钾溶液 D.氢氧化钠溶液
气体通过的顺序依次是:____________→____________→____________→____________ (填字母)。证明有气体 Y 存在的实验现象为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com