
【题目】铬鞣剂[Cr(OH)SO4]可用于提高皮革的耐曲折强度。一种以铬渣(含Cr2O3及少量Fe2O3、CaO、Al2O3、SiO2等杂质)为原料制备Cr(OH)SO4的工艺流程如图:
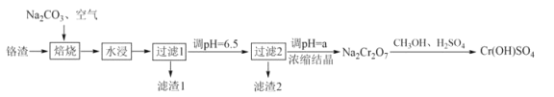
回答下列问题:
(1)“焙烧”时,Cr2O3转化为Na2CrO4的化学方程式为__。
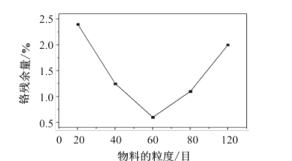
(2)“水浸”过程中,物料的粒度(颗粒大小)对铬残余量的影响如图所示,则最佳反应条件为__。
(3)“滤渣1”中有一种成分为铁铝酸四钙(Ca4Fe2Al2O10),是制造水泥的原料之一,用氧化物的形式表示其化学式__。
(4)“滤渣2”主要成分为Al(OH)3和__(填化学式),“过滤2”后,将溶液pH调至a,a__6.5(填“小于”或“大于”),目的是__(用离子方程式表示)。
(5)已知CH3OH在酸性条件下可被氧化生成CO2,写出Na2Cr2O7与CH3OH反应生成Cr(OH)SO4的化学方程式__。
(6)某厂用m1kg的铬渣(含Cr2O340%)制备Cr(OH)SO4,最终得到产品m2kg,则产率为__。
【答案】2Cr2O3+ 4Na2CO3+3O2![]() 4Na2CrO4 +4CO2 物质的粒度为60目时 4CaO·Fe2O3·Al2O3 H2SiO3 小于 2CrO42-+2H+
4Na2CrO4 +4CO2 物质的粒度为60目时 4CaO·Fe2O3·Al2O3 H2SiO3 小于 2CrO42-+2H+![]() Cr2O72-+H2O Na2Cr2O7+CH3OH+3H2SO4=2Cr(OH)SO4+CO2+ Na2SO4+4H2O
Cr2O72-+H2O Na2Cr2O7+CH3OH+3H2SO4=2Cr(OH)SO4+CO2+ Na2SO4+4H2O ![]()
【解析】
以铬渣(含Cr2O3及少量Fe2O3、CaO、Al2O3、SiO2等杂质)为原料制备Cr(OH)SO4,先加入碳酸钠、通入空气进行焙烧,再经过水浸、过滤除去固体杂质Fe2O3,调pH除去杂质氢氧化铝和氢氧化铁,最后通过氧化还原反应生成目标产物Cr(OH)SO4。
(1)“焙烧”时,Cr2O3转化为Na2CrO4,Cr元素的化合价升高,反应为氧化还原反应,还需氧化剂O2,根据电子守恒配平方程式为2Cr2O3+ 4Na2CO3+3O2![]() 4Na2CrO4 +4CO2。
4Na2CrO4 +4CO2。
(2)根据图示可知,当物质的粒度为60目时,铬的残余量最少,故最佳反应条件为物质的粒度为60目时。
(3)铁铝酸四钙(Ca4Fe2Al2O10),用氧化物的形式表示其化学式为4CaO·Fe2O3·Al2O3。
(4)步骤过滤1后溶液中存在偏铝酸钠和硅酸钠等杂质,调节pH使其转化为沉淀Al(OH)3和H2SiO3,故滤渣2主要成分为Al(OH)3和H2SiO3 。“过滤2”后,将溶液pH调至a,是为将2CrO42-转化为Cr2O72-,酸性条件下可以实现转化,故a小于6.5实现2CrO42-+2H+![]() Cr2O72-+H2O的转化。
Cr2O72-+H2O的转化。
(5)根据条件CH3OH在酸性条件下可被氧化生成CO2, Na2Cr2O7与CH3OH反应生成Cr(OH)SO4为氧化还原反应,其中碳元素、铬元素的化合价发生改变,根据电子守恒得化学反应方程式为Na2Cr2O7+CH3OH+3H2SO4=2Cr(OH)SO4+CO2+ Na2SO4+4H2O。
(6)最终得到产品Cr(OH)SO4m2kg,其中铬元素的含量为![]() kg,原料中铬元素的含量为
kg,原料中铬元素的含量为![]() ,则产率为
,则产率为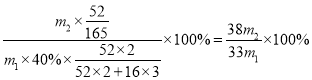 。
。


科目:高中化学 来源: 题型:
【题目】在一恒容的密闭容器中充入0.1mol/LCO2、0.1mol/LCH4,在一定条件下发生反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强的关系如图,下列有关说法不正确的是( )
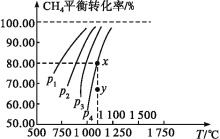
A.上述反应的ΔH>0
B.压强:p4>p3>p2>p1
C.1100℃时该反应平衡常数约为1.64
D.压强为p4时,在y点:v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.增大压强使平衡向生成Z的方向移动,平衡常数增大
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.反应达到平衡时,X的转化率为50%
D.增大X的浓度,Y的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A(C4H10O)是一种有机溶剂,且A只有一种一氯取代物B,在一定条件下A可以发生如下变化:
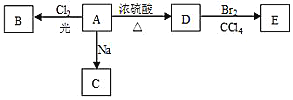
(1)A分子中的官能团名称是___,A的结构简式是___;
(2)写出下列化学方程式:
A→B:___;A→D:___;
(3)A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。F的结构简式是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
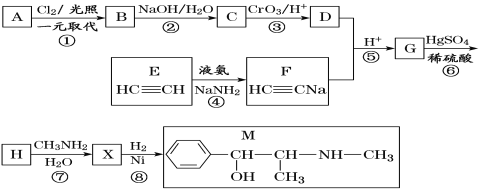
已知:I.R—CH2OH![]() RCHO
RCHO
II.R1-CHO+R-C≡CNa![]()
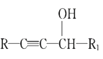
IV.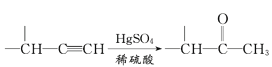
V.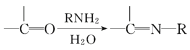
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
(1)混合气体的密度是_________。
(2)混合气体的平均摩尔质量是_________。
(3)CO2和CO的体积之比是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固定容积为2 L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图1表示T ℃时容器中各物质的量随时间变化的关系,图2表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图1表示T ℃时容器中各物质的量随时间变化的关系,图2表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
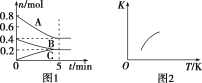
A.该反应可表示为2A(g)+B(g)![]() C(g) ΔH<0
C(g) ΔH<0
B.T ℃时该反应的平衡常数K=6.25
C.当容器中气体密度不再变化时,该反应达到平衡状态
D.T ℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是
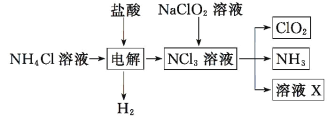
A.X 中大量存在的阴离子有 Cl-和 OH-B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构。下列说法不正确的是
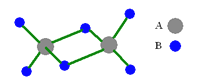
A.该化合物的化学式是Al2Cl6
B.该化合物在固态时所形成的晶体是分子晶体
C.该化合物是离子化合物,在熔融状态下能导电
D.该化合物中存在共价键,且不含有非极性共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com