
【题目】常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是:
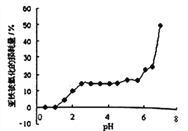
A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++O2+10H2O![]() 4Fe(OH)3+8H+平衡逆向移动
4Fe(OH)3+8H+平衡逆向移动
B. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH)2更易被氧化
D. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列判断正确的是( )
A. 2 g H2含有的氢原子数目为NA
B. 1 L 1molL﹣1KOH溶液中含有的钾离子数目为NA
C. 1 mol Zn完全变为Zn2+失去的电子数目为NA
D. 常温常压下,22.4 LO2含有的分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究(NH4)2 SO4 和 NH4HSO4混合物样品组成,称取四份该样品分别逐滴加入相同 浓度的 NaOH 溶液 40.0 mL,加热并完全反应,产生 NH3的体积(已折算成标准状况,
不考虑NH3在水中的溶解)如下表:
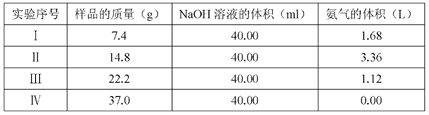
(1)样品中(NH4)2 SO4和NH4HSO4的物质的量之比为_____________。
(2)NaOH 溶液的物质的量浓度为_________________________(精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基烯酸酯在碱性条件下能快速聚合为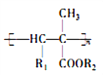 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
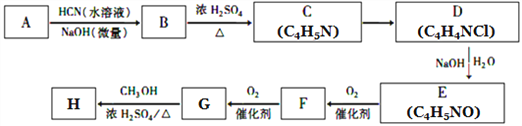
已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;
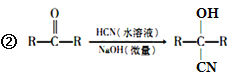
回答下列问题:
(1)A的化学名称为____________。
(2)C的结构简式为________________,F中的含氧官能团名称是________________。
(3)由E生成F的反应类型为_____________,由G生成H的反应类型为_____________。
(4)由G生成H的化学方程式为________________________________。
(5)写出A的能够发生银镜反应的同分异构体的结构简式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列如图所示是实验中常见的几种仪器:
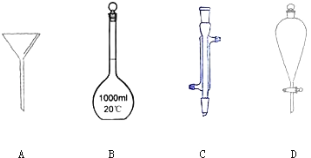
写出各字母代号所代表的仪器的名称 A : _____, B : _____, C : _____,D :__。
Ⅱ. 实验 室要配制 500 mL 0.2 mo l/ L NaOH 溶液 ,请 回 答 下列 问题:
(1)用托盘天平称取氢氧化钠,其质量为 _____g .
(2) 下列 主要操作步骤的正确顺序是 _____(填序号).
① 称取一定质量的氢氧化钠,放入烧杯 中 ,用适量蒸馏水溶解;
② 加水至液面离容量瓶颈刻度线下 1 -2 厘 米 时 , 改 用 胶 头 滴 管 滴 加 蒸 馏 水 至 凹 液 面 与 刻度线相切;
③ 待冷却至室温后,将溶液转移到 5 0 0 mL 容 量 瓶 中 ;
④ 盖好瓶塞,反复上下颠倒,摇匀;
⑤ 用少量的蒸馏水洗涤烧杯内壁和玻璃棒 2 ~ 3 次,洗涤液转移到容量瓶 中轻摇容量 瓶,使混合均匀 .
(3) 实验误差分析
① 如果 实验 过程 中 缺少步骤 ⑤ ,会使配制出的 N a O H 溶液浓度 _____(填 “偏高 ”或“偏低 ”或 “不变 ”,下同 )
②最终定容时 俯 视观察液面 会使配制出的 NaOH 溶液浓度 _____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着4个不同的原子或原子团,则这种碳原子称为“手性碳原子”。凡有一个手性碳原子的物质一定具有光学活性,物质![]() 有光学活性,发生下列反应后生成的产物有光学活性的是( )
有光学活性,发生下列反应后生成的产物有光学活性的是( )
A. 与NaOH水溶液共热 B. 与银氨溶液作用
C. 与乙酸发生酯化反应 D. 在催化剂存在下与H2作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是( )
A.SO2、H2S、O2
B.CO、H2、Cl2
C.NO、H2、O2
D.HCl、CO、NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,1体积水中能溶解500体积的HCl气体。若向水中通入标准状况下的44.8 L HCl气体配成1 L溶液,假设气体完全溶解,所得溶液中含HCl的物质的量浓度为____________,若得溶液密度为1.0g/cm3,则溶液中含HCl质量分数为________;从该溶液中取出10 mL浓盐酸溶解于水配制成250 mL溶液,配制后的稀溶液中含HCl物质的量浓度为________。在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有________________;配制过程中,造成浓度偏低的操作可能有________________(选填下列操作的序号)。
A.容量瓶用蒸馏水洗后未加干燥
B.量筒用蒸馏水洗后未干燥
C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量瓶中加水到刻度
D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线
E.定容时,俯视液面加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com