
【题目】标准状况下,1体积水中能溶解500体积的HCl气体。若向水中通入标准状况下的44.8 L HCl气体配成1 L溶液,假设气体完全溶解,所得溶液中含HCl的物质的量浓度为____________,若得溶液密度为1.0g/cm3,则溶液中含HCl质量分数为________;从该溶液中取出10 mL浓盐酸溶解于水配制成250 mL溶液,配制后的稀溶液中含HCl物质的量浓度为________。在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有________________;配制过程中,造成浓度偏低的操作可能有________________(选填下列操作的序号)。
A.容量瓶用蒸馏水洗后未加干燥
B.量筒用蒸馏水洗后未干燥
C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量瓶中加水到刻度
D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线
E.定容时,俯视液面加水至刻度线
【答案】2.0 mol/L7.3%0.08 mol/L250mL容量瓶(或容量瓶)BCD
【解析】
准状况下的44.8L HCl气体的物质的量=![]() =2mol,溶于水配成1L溶液,所得溶液中含HCl的物质的量浓度为:
=2mol,溶于水配成1L溶液,所得溶液中含HCl的物质的量浓度为:![]() =2mol/L;溶液的质量分数=
=2mol/L;溶液的质量分数=![]() ×100%=
×100%=![]() ×100%=7.3%;从该溶液中取出10mL浓盐酸溶解于水配置成250mL溶液,设配制后的稀溶液中含HCl物质的量浓度为C,依据溶液稀释前后所含溶质的物质的量不变得:C×250mL=2×10mL,解得C=0.08mol/L;容量瓶带有瓶塞,使用前应检验是否漏水;A.容量瓶用蒸馏水洗后未干燥,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故A不选;B.量筒用蒸馏水洗后未干燥,导致量取的氯化氢的物质的量偏小,溶液浓度偏低,故B选;C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量瓶中加水到刻度,导致溶质的物质的量偏小,溶液浓度偏小,故C选;D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线,导致溶质的物质的量偏小,溶液浓度偏小,故D选;E.定容时,俯视液面加水至刻度线,导致溶液体积偏小,溶液浓度偏大,故E不选;故选BCD;故答案为:2mol/L;7.3%;0.08mol/L;250mL容量瓶;BCD。
×100%=7.3%;从该溶液中取出10mL浓盐酸溶解于水配置成250mL溶液,设配制后的稀溶液中含HCl物质的量浓度为C,依据溶液稀释前后所含溶质的物质的量不变得:C×250mL=2×10mL,解得C=0.08mol/L;容量瓶带有瓶塞,使用前应检验是否漏水;A.容量瓶用蒸馏水洗后未干燥,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故A不选;B.量筒用蒸馏水洗后未干燥,导致量取的氯化氢的物质的量偏小,溶液浓度偏低,故B选;C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量瓶中加水到刻度,导致溶质的物质的量偏小,溶液浓度偏小,故C选;D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线,导致溶质的物质的量偏小,溶液浓度偏小,故D选;E.定容时,俯视液面加水至刻度线,导致溶液体积偏小,溶液浓度偏大,故E不选;故选BCD;故答案为:2mol/L;7.3%;0.08mol/L;250mL容量瓶;BCD。


科目:高中化学 来源: 题型:
【题目】体积为V mL,密度为d g/mL的溶液,含有相对分子质量为M的溶质m g,其物质的量浓度为c mol/L,质量分数为w%,下列表达式正确的是( )
A. c=(w×1000×d)/M B. m=V×d×w
C. w%=(c×M)/(1000×d)% D. c=(1000×m)/(V×M)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是:
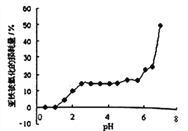
A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++O2+10H2O![]() 4Fe(OH)3+8H+平衡逆向移动
4Fe(OH)3+8H+平衡逆向移动
B. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH)2更易被氧化
D. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家发现了新的氢粒子,这种粒子是由3个氢原子核(只含质子)和2个电子构成的,这对解释宇宙演化提供了新的参考.对于这种氢粒子,下列说法错误的是( )
A.它的组成可以用H3+表示
B.它比普通氢分子多一个氢原子核
C.它一定含3个中子
D.可以推测它的化学性质与H2不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸异戊酯G(![]() )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下:
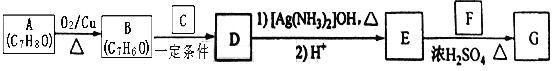
已知以下信息:
①![]() ;
;
②C为甲醛的同系物,相同条件下其蒸气与氢气的密度比为22。
回答下列问题:
(1)A的化学名称为_________________ 。
(2)B和C反应生成D的化学方程式为___________________________________ 。
(3)F中含有官能团的名称为____________ 。
(4)E和F反应生成G的化学方程式为__________________,反应类型为_________ 。
(5)F的同分异构体中不能与金属钠反应生成氢气的共有________ 种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为3:1的为____________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g。
求:(1)此混合气体中CO和CO2的物质的量各为多少?___________________
(2)混合气体缓慢通过足量的澄清石灰水后,剩余的气体是什么?其质量为多少?其所含电子数为多少?________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B. NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-![]() NH3↑+SO32-+2H2O
NH3↑+SO32-+2H2O
C. 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH-
D. 向FeO中加入稀硫酸:2FeO + 8H+ + SO42- =2Fe3+ + SO2 ↑+ 4H2O
【答案】B
【解析】
Fe(OH)3具有氧化性、I—具有还原性,二者反应生成I2和Fe2+;NaOH溶液电离出的OH-,既与NH4+反应,又与HSO3-反应;酸性条件下溶液中不存在OH-;向FeO中加入稀硫酸,发生复分解反应。
Fe(OH)3具有氧化性、I-具有还原性,二者反应生成I2和Fe2+,离子方程式为2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,A错误;NH4HSO3溶液与足量的NaOH溶液混合加热,足量的NaOH溶液电离出的OH-,既与NH4+反应,又与HSO3-反应,方程式符合客观事实,化学式书写正确,电荷和原子都守恒,B正确;酸性条件下KIO3溶液与KI溶液发生反应生成I2,正确的离子方程式为:IO3-+5I-+6H+=3I2+3H2O,C错误;向FeO中加入稀硫酸, FeO与稀硫酸反应生成硫酸亚铁和水,D错误。本题选B。
【点睛】
题考查了离子方程式的书写,明确物质的性质、离子方程式书写规则即可解答,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等。
【题型】单选题
【结束】
19
【题目】为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了四种不同的方法,其中不可行的是
A. 分别配成1mol/L的溶液,各取1mL滴加1滴酚酞试液,比较颜色深浅
B. 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊
C. 分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀
D. 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色(必要时可透过蓝色钴玻璃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是 。
第1组 | 第2组 | 第3组 |
S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2 -76.1℃,SO3 16.8℃;沸点:SO2 -10℃,SO3 45℃)

①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是 。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL 2.5mol/L NaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生反应的化学方程式是 。
【答案】(1)H2SO3 (2)①2SO2+O2![]() 2SO3
2SO3
②使SO3凝结成固体与SO2分离 5SO2+2H2O+2MnO4—=5SO42—+2Mn2++4H+
③3SO2+4NaOH=Na2SO3+2NaHSO3+H2O
【解析】
(1)观察第三组可知,第二组中X物质应该属于硫呈+4价的含氧酸,即亚硫酸
(2)①SO2在V2O5的催化作用下可被氧化为SO3
②由所给数据可知SO3在冰水中呈固态,所以II装置是通过冷凝将混合气体分离
SO2可将酸性KMnO4中的锰元素还原,且有酸生成(溶液pH降低),故反应方程式为:5SO2+ 2H2O + 2MnO4-="=" 5SO42-+ 2Mn2++ 4H+
③SO2与NaOH溶液反应与两者的物质的量比有关:
SO2+ 2NaOH = Na2SO3+ H2O SO2+ NaOH =NaHSO3
现两者的物质的量比为4:7,直接由总方程式根据元素守恒来配平即可
【题型】实验题
【结束】
29
【题目】如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。
![]()
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
1 | 10 mLFeO4溶液 | 10 mLNH3 | 生成白色沉淀,后变色 |
2 | 20 mLH2S | 12mLSO2 | |
3 | 30 mLNO2 | 10 mLH2O(l) | 剩有无色气体,活塞自动向内压缩 |
4 | 15 mLCl2 | 40 mLNH3 |
试回答下列问题:
(1)实验1中,沉淀最终变为_____色,写出沉淀变色的化学方程式_________________________。
(2)实验2甲针筒内的现象是:有_____________生成,活塞______移动(填向外、向内、不)。
反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________溶液中。
(3)实验3中,甲中最后剩余的无色气体是_______,写出NO2与H2O反应的化学方程式_______。
(4)实验4中,已知:Cl2 + NH3 → N2+ HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为____________,最后针筒中剩余气体的体积约为_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g)'ΔH=-92.4 kJ·mol-1,NH3在平衡混合气中的体积分数(φ)与温度(T)、压强(p)的关系如图所示。下列判断正确的是( )
2NH3(g)'ΔH=-92.4 kJ·mol-1,NH3在平衡混合气中的体积分数(φ)与温度(T)、压强(p)的关系如图所示。下列判断正确的是( )
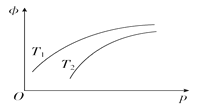
A. T1大于T2
B. 升高温度,该反应的化学平衡常数增大
C. 当n(N2)∶n(H2)∶n(NH3)=1∶3∶2时,反应一定达到平衡状态
D. 其他条件不变,缩小体积增大压强,可提高单位时间内NH3的产量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com