
【题目】环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
氢化反应:![]() (l)+H2(g)
(l)+H2(g)![]()
![]() (环戊烯)(l) H=-100.5 kJ/mol
(环戊烯)(l) H=-100.5 kJ/mol
副反应:![]() (l)+H2(g)
(l)+H2(g)![]()
![]() (环戊烷)(l) H=-109.4 kJ/mol
(环戊烷)(l) H=-109.4 kJ/mol
解聚反应: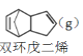
![]() 2
2![]() (g) H>0
(g) H>0
回答下列问题:
(1)反应![]() (l)+2H2(g)
(l)+2H2(g)![]()
![]() (l)的△H=_________ kJ/mol。
(l)的△H=_________ kJ/mol。
(2)一定条件下,将环戊二烯溶于有机溶剂进行氢化反应(不考虑二聚反应),反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如图所示:
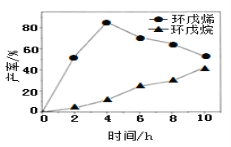
①0~4 h氢化反应速率比副反应快的可能原因是___________________。
②最佳的反应时间为_________h。若需迅速减慢甚至停止反应,可采取的措施有__________________(写一条即可)。
③一段时间后,环戊烯产率快速下降的原因可能是_____________________。
(3)解聚反应在刚性容器中进行(不考虑氢化反应和副反应)。
①其他条件不变,有利于提高双环戊二烯平衡转化率的是________(填标号)。
A.增大双环戊二烯的用量 B.使用催化剂 C.及时分离产物 D.适当提高温度
②实际生产中常通入水蒸气以降低双环戊二烯的温度(水蒸气不参与反应)。某温度下,通入总压为300 kPa的双环戊二烯和水蒸气,达到平衡后总压为500 kPa,双环戊二烯的转化率为80%,则 p(H2O)=________kPa,平衡常数Kp=__________kPa (Kp为以分压表示的平衡常数)。
【答案】-209.9 氢化反应的活化能小或反应物的浓度大 4 排出氢气或急剧降温 副反应增加 CD 50 3200
【解析】
(1)根据盖斯定律,将已知的热化学方程式叠加,可得待求反应的反应热;
(2)①活化能越小、反应物浓度越大,该反应越易正向移动;
②环戊烯的产率越大、环戊烷的产率越小越好;若需迅速减慢甚至停止反应,可以通过减少反应物浓度或降低温度实现;
③副反应能降低环己烯的产率;
(3)①该反应的正反应是一个反应前后气体体积增大的吸热反应,减小压强、升高温度都使平衡正向移动,有利于提高双环戊二烯平衡转化率;
②设加入的双环戊二烯的物质的量为x mol、水的物质的量为y mol,双环戊二烯的转化率为80%,则剩余双环戊二烯的物质的量为0.2x mol、生成环戊二烯的物质的量为1.6x mol,恒温恒容条件下,气体的压强之比等于物质的量之比,计算反应开始时双环戊二烯与水的物质的量的比,及平衡时各种气体的物质的量,计算出各种气体的平衡分压,代入平衡常数表达式然后计算可得其数值。
(1)①![]() (l)+H2(g)
(l)+H2(g)![]()
![]() (环戊烯)(l) H=-100.5 kJ/mol;
(环戊烯)(l) H=-100.5 kJ/mol;
②![]() (l)+H2(g)
(l)+H2(g)![]()
![]() (环戊烷)(l) H=-109.4 kJ/mol,
(环戊烷)(l) H=-109.4 kJ/mol,
由于反应热与反应途径无关,将方程式①+②整理可得:![]() (l)+2H2(g)
(l)+2H2(g)![]()
![]() (l)的△H=-209.9 kJ/mol;
(l)的△H=-209.9 kJ/mol;
(2)①活化能越小、反应物浓度越大,该反应越易正向移动,0~4 h氢化反应速率比副反应快的可能原因是氢化反应的活化能小或反应物的浓度大;
②环戊烯的产率越大、环戊烷的产率越小越好,根据图知4 h时环戊烯产率最大;若需迅速减慢甚至停止反应,可以通过减少反应物浓度或降低温度实现,所以排出氢气或急剧降温都能迅速减慢甚至停止反应;
③副反应能降低环己烯的产率,所以一段时间后,环戊烯产率快速下降的原因可能是副反应增加;
(3)①A. 增大双环戊二烯的用量,反应物浓度增大,化学平衡正向移动,但其转化率降低,A不符合题意;
B. 使用催化剂只改变化学反应速率不影响平衡移动,双环戊二烯的转化率不变,B不符合题意;
C. 及时分离产物,减小了生成物的浓度,化学平衡正向移动,提高双环戊二烯转化率,C符合题意;
D. 适当提高温度,化学平衡向吸热的正反应方向移动,双环戊二烯转化率升高,D符合题意;
故合理选项是CD;
②设加入的双环戊二烯的物质的量为x mol、水的物质的量为y mol,由于达到平衡时双环戊二烯的转化率为80%,则剩余双环戊二烯的物质的量为0.2x mol、生成环戊二烯的物质的量为1.6x mol。在恒温恒容条件下,气体的压强之比等于物质的量之比,所以(x+y)mol:(0.2x+1.6x+y)mol=300kPa:500kPa=3:5,解得x:y=5:1,则平衡时H2O的分压p(H2O)=![]() =50 kPa;p(双环戊二烯)=
=50 kPa;p(双环戊二烯)=![]() =50 kPa;p(环戊二烯)=
=50 kPa;p(环戊二烯)=![]() =400 kPa,则该反应的化学平衡常数用平衡分压表示Kp=
=400 kPa,则该反应的化学平衡常数用平衡分压表示Kp=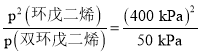 =3200 kPa。
=3200 kPa。


科目:高中化学 来源: 题型:
【题目】完成下列填空
① 2—溴丙烷的消去反应(化学方程式)
② 1,2-二溴乙烷的水解(化学方程式)
③检验溴乙烷中溴元素滴加试剂顺序(填化学式)
④二氢香豆素(![]() )常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(![]() )需要用到的试剂有:NaOH溶液、 。
)需要用到的试剂有:NaOH溶液、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。

有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果不能作为相应定律或原理的证据是
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 | |
实 验 方 案 |
|
|
|
|
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡, 试管中出现浑浊 | 测得ΔH为ΔH1、ΔH2的和 | H2与O2的体积比约为2︰1 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Ni、Pt在周期表中同族,该族元素的化合物在科学研究和实际生产中有许多重要用途。
(1)①Fe在元素周期表中的位置为________。
②已知FeO晶体晶胞结构如NaCl型,Fe2+的价层电子排布式为________,阴离子的配位数为_______。
③K3[Fe(CN)5NO]的组成元素中,属于第二周期元素的电负性由小到大的顺序是_______。
④把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),该反应的化学方程式为________。
(2)铂可与不同的配体形成多种配合物。分子式为[Pt(NH3)2Cl4]的配合物的配体是______;该配合物有两种不同的结构,其中呈橙黄色的物质的结构比较不稳定,在水中的溶解度大;呈亮黄色的物质的结构较稳定,在水中的溶解度小,下图图1所示的物质中呈亮黄色的是______(填“A”或“B”),理由是________。

(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如上图图2所示。储氢原理为:镧镍合金吸咐H2,H2解离为H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱心和上下底面的面心,则形成的储氢化合物的化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钼在工业和国防建设中有重要的作用。钼(Mo)的常见化合价为+6、+5、+4。由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4·2H2O),部分流程如图1所示:
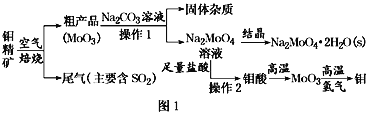
已知:钼酸微溶于水,可溶于液碱和氨水。
回答下列问题:
(1)焙烧钼精矿时发生的化学方程式为_____________________________。
(2)钼精矿焙烧时排放的尾气对环境的主要危害是___________________,请提出一种实验室除去该尾气的方法____________________________________。
(3)操作2的名称为________。由钼酸得到MoO3所用到的硅酸盐材料仪器的名称是________。
(4)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分数(φ)。
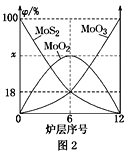
①x=________。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量分别为________、________。
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO42-)=0.80mol·L1,c(SO42-)=0.04 mol·L1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-。当BaMoO4开始沉淀时,SO42-的去除率是________。[Ksp(BaSO4)=1.1×1010、Ksp(BaMoO4)=4.0×108,溶液体积变化可忽略不计]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如下图所示。
下列有关麦考酚酸说法正确的是( )
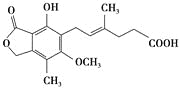
A.在一定条件下可与氢气发生加成反应,最多消耗氢气5 mol
B.不能与FeCl3溶液发生显色反应
C.在一定条件下可发生氧化、还原、取代、消去反应
D.1 mol麦考酚酸最多能与3 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①:2C(s)+O2(g)═2CO(q)△H=﹣221.0kJ/mol②2H2(q)+O2(q)═2H2O(g)△H=﹣483.6kJ/mol,则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
A.262.6kJ/mol B.﹣131.3kJ/mol C.﹣352.3kJ/mol D.+131.3kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com