
【题目】4molA和4molB在2L的密闭容器中发生如下反应:2A(g)+B(g)=2C(g)+D(g)。前15s,A的平均反应速率为0.12mol·(L·s)1,则15s时,容器中B的物质的量为( )
A.2.2molB.3.2molC.1.8molD.2.8mol
科目:高中化学 来源: 题型:
【题目】甲胺(![]() )的性质与氨气相似,将pOH相同、体积均为
)的性质与氨气相似,将pOH相同、体积均为![]() 的CH3NH2H2O和
的CH3NH2H2O和![]() 两种溶液分别加水稀释至体积为V,pOH随
两种溶液分别加水稀释至体积为V,pOH随![]() 的变化关系如图所示,下列叙述错误的是( )
的变化关系如图所示,下列叙述错误的是( )
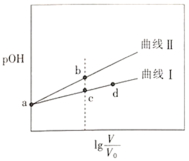
已知:常温下,![]() ,pOH=-lgc(OH-)。
,pOH=-lgc(OH-)。
A.稀释相同倍数时,CH3NH2H2O的浓度比![]() 的浓度大
的浓度大
B.溶液中水的电离程度:b点大于c点
C.由c点到d点,溶液中![]() 保持不变
保持不变
D.常温下,某盐酸的![]() ,a点时CH3NH2H2O的
,a点时CH3NH2H2O的![]() ,当
,当![]() 时,取等体积的两溶液混合,充分反应后:n(Cl-)>n(CH3NH3+)>n(H+)>n(OH-)
时,取等体积的两溶液混合,充分反应后:n(Cl-)>n(CH3NH3+)>n(H+)>n(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10 mL浓度均为3 mol·L-1的HNO3与H2SO4的混合溶液中加入1.92 g铜,充分反应后,设溶液体积仍为10 mL。求:
(1)产生的气体在标准状况下的体积是多少升?__________
(2)反应后溶液中各溶质的离子浓度是多少?_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为N2H4+O2===N2+2H2O。下列说法正确的是
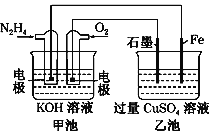
A. 乙池中Fe电极上发生氧化反应
B. 乙池中石墨电极上发生的反应可写为4OH--4e-===2H2O+O2↑
C. 甲池溶液pH增大,乙池溶液pH减小
D. 甲池中每消耗0.1 mol N2H4乙池电极上则会析出6.4 g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.20℃时,饱和KCl溶液的密度为1.174 g·cm-3,质量分数为![]() ×100%,此溶液中KCl的物质的量浓度为4.0 mol·L-1
×100%,此溶液中KCl的物质的量浓度为4.0 mol·L-1
B.100g浓度为c mol·L-1的氨水中加入一定量的水稀释成0.5cmol·L-1,则加入水的体积大于100ml(已知氨水的浓度越大,其密度越小)
C.将标准状况下的aLHCl气体溶于1000mL水中,得到的盐酸溶液密度为bg/mL,则该盐酸溶液的物质的量浓度为![]() mol/L
mol/L
D.V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中SO42—的物质的量浓度为![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X(g)+3Y(g)![]() 2W(g)+M(g) △H=-akJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1molX(g)与3molY(g),下列说法正确的是( )
2W(g)+M(g) △H=-akJ·mol-1(a>0)一定温度下,在体积恒定的密闭容器中,加入1molX(g)与3molY(g),下列说法正确的是( )
A.充分反应后,放出热量为akJ
B.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1∶2
C.当体系的压强不再改变时,表明该反应已达平衡
D.若增大Y的浓度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下CO2和H2S发生如下反应:CO2(g) +H2S(g)COS(g) +H2O(g)。有关实验数据如下:
实验 | 温度 | 物质的起始物质的量/(mol) | 平衡时COS物质的量/(mol) | |
n(CO2) | n(H2S) | n(COS) | ||
I | 337℃ | 0.10 | 0.40 | 0.01 |
II | 347℃ | 0.10 | 0.40 | 0.015 |
下列说法不正确的是
A.该反应为吸热反应
B.实验I达平衡后COS的物质的量分数为5%
C.实验I温度下,反应的平衡常数为![]()
D.平衡后向II中再充入0.10 mol CO2和0.40 mol H2S,相同温度下再达平衡时n(COS)=0.03mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Na2CO3与稀盐酸反应分两步进行:![]() +H+==
+H+==![]() ,
,![]() +H+= CO2↑+H2O。向10.00 mL 0.1000 mol·L-1Na2CO3溶液中滴加0.1000 mol·L-1盐酸,溶液pH随盐酸体积的变化如图。
+H+= CO2↑+H2O。向10.00 mL 0.1000 mol·L-1Na2CO3溶液中滴加0.1000 mol·L-1盐酸,溶液pH随盐酸体积的变化如图。
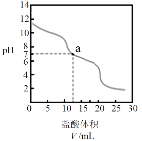
下列说法不正确的是
A.V = 5.00mL时,溶液中c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.V =10.00mL时,溶液中c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)+c(Cl-)
)+c(H2CO3)+c(Cl-)
C.a点的溶液中:n(![]() )+n(
)+n(![]() ) = 0.001 mol
) = 0.001 mol
D.V = 20.00mL时,溶液pH<7,是因为H2CO3 ![]()
![]() + H+
+ H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是
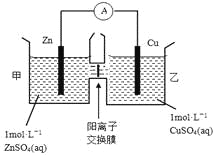
A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com