
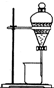
 某同学为了验证海带中含有碘元素并提取碘单质,拟进行如下实验,请回答相关问题.
某同学为了验证海带中含有碘元素并提取碘单质,拟进行如下实验,请回答相关问题.

科目:高中化学 来源: 题型:
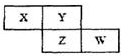 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、Cl-、NO3- |
| B、Mg2+、Ca2+、SO42-、OH- |
| C、Fe2+、Fe3+、H+、NO3- |
| D、Ba2+、Fe3+、Cl-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 120℃ | 300℃ | 480℃ | |
| 化学式 | KxFey(C2O4)Z | KxFeyO(C2O4)Z-1 | KxFeyO2(C2O4)Z-2 |
| 质量 | 4.370g | 3.650g | 2.930g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com