
周期表中有些元素有“对角线相似”现象,如Li、Mg;Be、Al;B、Si等两两性质相似。若用已潮解的LiCl加热蒸干并强热至熔融,再用惰性电极电解,结果得到金属锂和一种无色无味的气体。下列说法正确的是
A.LiOH易溶于水 B.电解前LiCl在加热时已发生水解
C.无色气体为电解生成的H2 D.Li和水反应要比Na和水剧烈
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
不能比较氮和氧非金属性相对强弱的是
| A.氨气在氧气中燃烧生成氮气 | B.沸点:H2O>NH3 |
| C.NO中N为+2价,氧为-2价 | D.热稳定性:H2O>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于第IVA族元素的说法中,正确的是
| A.原子半径:14Si>32Ge |
| B.稳定性:CH4<SiH4 |
| C.酸性:H2CO3>H2SiO3 |
| D.碱性:32Ge(OH)4>50Sn(OH)4>82Pb(OH)4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知第三周期元素M,其原子最外层达到饱和时所需的电子数小于次外层与最内层电子数之差,且等于最内层电子数的正整数倍。下列关于元素M的说法一定错误的是
| A.M元素存在同素异形体 |
| B.M元素为非金属元素 |
| C.M的最高价氧化物对应的水化物都是强酸 |
| D.常温下,能稳定存在的M的氧化物都是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质性质的变化规律中与共价键键能大小有关的是
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
| A.仅③ | B.①③ | C.②④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
| A.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
| B.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小 |
| C.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱 |
| D.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表是元素周期表的一部分,有关说法不正确的是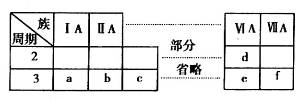
| A.元素e的氧化物对应的水化物均为强酸 |
B.a、b、d、e四种元素的离子半径: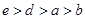 |
| C.b、f两种元素形成的化合物为离子化合物 |
| D.a、c、e的最高价氧化物对应的水化物之间能够相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图是元素周期表的一部分,下列关系正确的是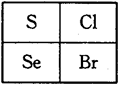
| A.还原性:Se2->S2->Cl- |
| B.热稳定性:HCl>H2Se>HBr |
| C.原子半径:Se>Cl>S |
| D.酸性:HBrO4>HClO>H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有一合金由X、Y、Z、W四种金属组成,①若将合金放入盐酸中只有Z、Y能溶解;②若将合金于潮湿空气中,表面只出现Z的化合物;③若将该合金作阳极,用X盐溶液作电解质溶液,通电时四种金属都以离子形式进入溶液中,在阴极上只析出X。这四种金属活动性顺序是
| A.Y>Z>W>X | B.Z>Y>W>X |
| C.W>Z>Y>X | D.X>Y>Z>W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com