
【题目】(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为________ (阿伏加德罗常数用NA表示),放出的热量为________kJ。
(2)已知:C3H8(g) == CH4(g)+HC≡CH(g)+H2(g) ΔH1=+156.6 kJ·mol-1
CH3CH=CH2(g) == CH4(g)+HC≡CH(g) ΔH2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g) === CH3CH=CH2(g)+H2(g)的ΔH=______kJ·mol-1。
(3)甲烷在高温下与水蒸气反应的方程式为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。部分物质的燃烧热数据如下表:已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式: _______________________________。
CO(g)+3H2(g)。部分物质的燃烧热数据如下表:已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式: _______________________________。
物质 | 燃烧热(kJ·mol-1) |
H2(g) | -285.8 |
CO(g) | -283.0 |
CH4(g) | -890.3 |
【答案】 1.6 NA 173.4 +124.2 CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.1 kJ·mol-1
【解析】(1)已知①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJmol-1,②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1 160kJmol-1,
利用盖斯定律![]() (①+②)可得:③CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g),△H=-
(①+②)可得:③CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g),△H=-![]() kJmol-1=-867kJmol-1,标况下4.48L甲烷的物质的量为:n(CH4)=
kJmol-1=-867kJmol-1,标况下4.48L甲烷的物质的量为:n(CH4)=![]() =0.2mol,甲烷中碳元素的化合价为-4价,反应产物二氧化碳中C元素化合价为+4价,化合价变化为8,即完全反应1mol甲烷转移了8mol(8NA)电子,则反应0.2mol甲烷转移的电子总数为:0.2mol×8NA=1.6NA;根据热化学方程式③可知,完全反应0.2mol甲烷放热的热量为:867kJmol-1×0.2mol=173.4kJ;
=0.2mol,甲烷中碳元素的化合价为-4价,反应产物二氧化碳中C元素化合价为+4价,化合价变化为8,即完全反应1mol甲烷转移了8mol(8NA)电子,则反应0.2mol甲烷转移的电子总数为:0.2mol×8NA=1.6NA;根据热化学方程式③可知,完全反应0.2mol甲烷放热的热量为:867kJmol-1×0.2mol=173.4kJ;
(2)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJmol-1
②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJmol-1
依据盖斯定律①-②得到C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol;
(3)已知:①H2(g)+![]() O2(g)=H2O(l)△H=-285.8kJmol-1;②CO(g)+
O2(g)=H2O(l)△H=-285.8kJmol-1;②CO(g)+![]() O2(g)=CO2(g) )△H=-283.0kJmol-1;③CH4(g)+2O2(g)=CO2(g)+2H2O(l))△H=-890.3kJmol-1,④H2O(g)=H2O(l)△H=-44.0kJmol-1,利用盖斯定律将④+③-②-3×①可得:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=(-44.0kJmol-1)+(-890.3kJmol-1)-(-283.0kJmol-1)-3×(-285.8kJmol-1)=+206.1kJmol-1,
O2(g)=CO2(g) )△H=-283.0kJmol-1;③CH4(g)+2O2(g)=CO2(g)+2H2O(l))△H=-890.3kJmol-1,④H2O(g)=H2O(l)△H=-44.0kJmol-1,利用盖斯定律将④+③-②-3×①可得:CH4(g)+H2O(g)=CO(g)+3H2(g) △H=(-44.0kJmol-1)+(-890.3kJmol-1)-(-283.0kJmol-1)-3×(-285.8kJmol-1)=+206.1kJmol-1,


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】立方烷(C8H8)外观为有光泽的晶体。其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氯代物1种、二氯代物有3种、三氯代物也有3种
C. 立方烷是棱晶烷(![]() )的同系物,也是环辛四烯的同分异构体
)的同系物,也是环辛四烯的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5molCH4的质量是_______________g,在标准状况下的体积为_______________L;含有约______________个氢原子。
(2)将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述错误的是 ( )


A. 已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);ΔH= - 483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B. 常温下0.2 mol·L-1 HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(A-)> c(Na+)>c(H+)>c(OH-)
C. 常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐减小,且HX的还原性逐渐减弱
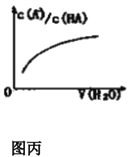
D. 图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,![]() 的变化情况
的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:

有关物质的物理性质见下表。
物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10 mL环己醇的A中,在55 ~ 60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的![]() ,反应剧烈将导致体系温度迅速上升,副反应增多。
,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为____________________________________________;
②蒸馏不能分离环己酮和水的原因是__________________________________________。
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加人无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是________________________________________________;
②B中水层用乙醚萃取的目的是______________________________________________;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__________,操作d中,加入NaC1固体的作用是_____________________________。
(4)恢复至室温时,分离得到纯产品体积为6 mL,则环已酮的产率为____________。(计算结果精确到0.1%)
查看答案和解析>>
科目:高中化学 来源: 题型:
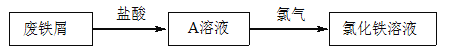
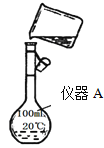
【题目】某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液。实验操作过程如下:
根据要求回答问题:
(1)用浓盐酸配制250mL 0.2molL-1稀盐酸,图中有两处错误分别是_____________,______________。
(2)废铁屑用盐酸处理后,还含有不溶性杂质,为获取澄清的A溶液,进行物质分离的操作名称是___________。
(3)若FeCl2溶液中混有少量的FeCl3溶液,现要加入一种试剂除去FeCl3,请写出除杂的离子方程式______________________。
(4)配制250mL 0.2molL-1稀盐酸时,下列操作会造成结果偏高的是(_______)
A.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
B.转移溶液前溶液未冷却至室温
C.未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶的刻度线
E.容量瓶洗涤干净后,瓶内壁有少量水滴。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)
2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)

回答下列问题:
(1)该实验中A部分的装置是______(填标号)。

(2)装置B中产生的现象为______。
(3)请设计实验验证装置C中的Na2SO3已被氧化______。
(4)写出D装置中发生反应的离子方程式______。
(5)该实验存在明显的缺陷,请你提出改进的方法______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物,如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下:
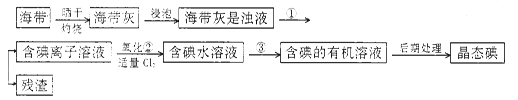
(1)指出提取碘的过程中有关的实验操作名称:①____________________;③______________。
若实验②中采用酸性条件下加入双氧水,则有关反应的离子方程式_________________________________。
(2)提取碘的过程中,可供选择的有关试剂是___________。
A.甲苯,酒精B.四氯化碳,苯C.汽油,乙酸D.汽油,甘油
(3)含碘的有机溶液后期处理得到晶态碘需要进行的操作为___________;
最后,晶态碘在___________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中可用如图装置来制取干燥的氨气。

(1)写出A处发生反应的化学方程式_____________________________________。
(2)U形管B中所放的药品是__________________。
(3)实验室制取下列气体时,与实验室制取氨气的气体发生装置相同的是______________(填字母)。
A. 氢气 B.氧气C.氯气 D.二氧化碳
(4)试管C的管口处要放置一小团棉花,放置棉花的作用是___________________________。
(5)资料显示:“氨气可在纯氧中点燃,反应生成氮气和水”。为验证此事实,某同学设计了一个实验方案,装置见D。请写出该反应的化学方程式__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com