
【题目】某氧原子的质最为ag,12C原子的质量为bg,且NA表示阿伏加德罗常数,下列说法中正确的是( )
A.该氧原子的摩尔质量为 ![]() g/mol
g/mol
B.1 mol 该氧原子质量为幽a NAg
C.xg 该氧原子所含的电子数为 ![]()
D.yg 该氧原子的中子数一定为 ![]()
【答案】B
【解析】解:A.某一原子的相对原子质量是指:以一个碳﹣12原子质量的 ![]() 作为标准,该原子的质量跟一个碳﹣12原子质量的1/12的比值,故该氧原子的相对原子质量为
作为标准,该原子的质量跟一个碳﹣12原子质量的1/12的比值,故该氧原子的相对原子质量为 ![]() ,即该氧原子的摩尔质量为
,即该氧原子的摩尔质量为 ![]() g/mol,故A错误;
g/mol,故A错误;
B.氧原子的质量为ag,NA个氧原子的质量为aNAg,故B正确;
C.一个该氧原子的质量是a,xg该氧原子个数为X/ag.1个氧原子所含的中子数是8个,则xg该氧原子所含的电子数为 ![]() ,故C错误;
,故C错误;
D.氧原子有多种,中子数不一定是8,故D错误.
故选:B.
A.某一原子的相对原子质量是指:以一个碳﹣12原子质量的 ![]() 作为标准,该原子的质量跟一个碳﹣12原子质量的1/12的比值;
作为标准,该原子的质量跟一个碳﹣12原子质量的1/12的比值;
B.NA个氧原子的质量就是1mol该原子质量;
C.氧原子的质子数为8,1个氧原子所含的电子数是8个;
D.氧原子的中子数不一定为8.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铅蓄电池的总反应式为:PbO2+Pb+2H2SO4 ![]() 2PbSO4+2H2O据此判断下列叙述正确的是( )
2PbSO4+2H2O据此判断下列叙述正确的是( )
A.放电时,H2SO4浓度增加
B.放电时,负极的电极反应式为:Pb+SO42﹣﹣2e﹣═PbSO4
C.在充电时,电池中每转移1 mol电子,理论上生成2 mol硫酸
D.在充电时,阴极发生的反应是PbSO4﹣2e﹣+2H2O═PbO2+SO42﹣+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关海水综合利用的说法正确的是( )
A.电解饱和食盐水可制得金属钠B.海水提溴涉及到氧化还原反应
C.海带提碘只涉及物理变化D.海水提镁不涉及复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是
A. 将FeCl3溶液滴入蒸馏水中即可
B. 将FeCl3溶液滴入热水中,得到棕黄色液体即可
C. 将FeCl3溶液滴入沸水中,并继续煮沸,得到红褐色液体即可
D. 将FeCl3溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的Cu分别被足量的浓硝酸和稀硝酸氧化成硝酸铜,硝酸还原产物分别为NO2和NO两种气体,若不考虑其他反应,则在同温同压下NO2和NO的体积比为()
A. 3:1 B. 1:3 C. 1:1 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: 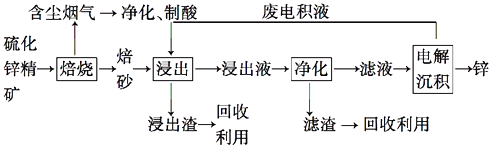
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生主要反应的离子方程式为 .
(6)我国古代曾采用“火法”工艺冶炼锌,明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷淀,毁罐取出,…,即倭铅也.”该炼锌工艺过程主要反应的化学方程式为 . (注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com