
����Ŀ���������ʹ��������㾫����Ҫԭ�ϣ��ϳ�·����ͼ��ʾ��
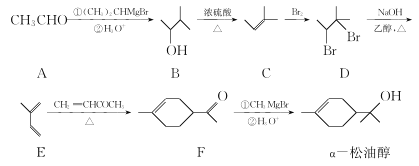
��1���������ʹ������������ŵ�����Ϊ______________��
��2��C��D�ķ�Ӧ����Ϊ______________ ��
��3��E��F�ķ�Ӧ���и�����X(��F��Ϊͬ���칹�壩���ɣ�д��X�Ľṹ��ʽ��______________��
��4���������ʹ���һ��ͬ���칹��ͬʱ��������������д����ͬ���칹��Ľṹ��ʽ��______________��
�ٷ��������л�ѧ�������ͣ�
�ڷ����в�ͬ��ѧ��������ԭ����Ŀ��Ϊ1:4:4��
��5����֪��RBr![]() RMgBr(R��ʾ��������д�����������2�����Ϊ��ԭ���Ʊ�
RMgBr(R��ʾ��������д�����������2�����Ϊ��ԭ���Ʊ�![]() �ĺϳ�·������ͼ�����Լ����л��ܼ����ã��ϳ�·������ͼʾ����������ɣ���______________
�ĺϳ�·������ͼ�����Լ����л��ܼ����ã��ϳ�·������ͼʾ����������ɣ���______________
���𰸡�̼̼˫�����ǻ� �ӳɷ�Ӧ 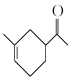
![]()
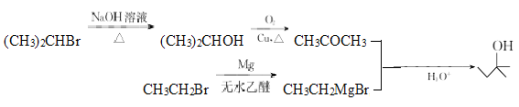
��������
��1�������������ʹ��Ľṹ��ʽ��д���������ƣ�
��2��C��D��![]() ��̼̼˫�����巴Ӧ����
��̼̼˫�����巴Ӧ����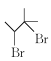 ��
��
��3��E��F�Ǽӳɷ�Ӧ������CH2=CHCOCH3�Ľṹ���ԳƷ���������X�Ľṹ��ʽ��
��4�����������ʹ��IJ����Ͷ���2�����������л�ѧ�������ͣ�˵������2������
�ڷ����в�ͬ��ѧ��������ԭ����Ŀ��Ϊ1:4:4��˵���ṹ�Գƣ�
��5��CH3CH2Br![]() CH3CH2MgBr��(CH3)2CHBr
CH3CH2MgBr��(CH3)2CHBr![]() (CH3)2CHOH��(CH3)2CHOH����ΪCH3COCH3��CH3COCH3��CH3CH2MgBr��Ӧ����
(CH3)2CHOH��(CH3)2CHOH����ΪCH3COCH3��CH3COCH3��CH3CH2MgBr��Ӧ����![]() ��
��
��1�������������ʹ��Ľṹ��ʽ��![]() �����й���������Ϊ̼̼˫�����ǻ���
�����й���������Ϊ̼̼˫�����ǻ���
��2��C��D��![]() ��̼̼˫�����巴Ӧ����
��̼̼˫�����巴Ӧ���� ����Ӧ�����Ǽӳɷ�Ӧ��
����Ӧ�����Ǽӳɷ�Ӧ��
��3��E��F��1,4�ӳɷ�Ӧ��CH2=CHCOCH3�Ľṹ���Գƣ��ӳɲ��������![]() ��
��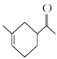 ������X�Ľṹ��ʽ��
������X�Ľṹ��ʽ�� ��
��
��4�����������ʹ��IJ����Ͷ���2�����������л�ѧ�������ͣ�˵������2�������ڷ����в�ͬ��ѧ��������ԭ����Ŀ��Ϊ1:4:4��˵���ṹ�Գƣ������������������ʹ���ͬ���칹����![]() ��
��
��5��CH3CH2Br![]() CH3CH2MgBr��(CH3)2CHBr
CH3CH2MgBr��(CH3)2CHBr![]() (CH3)2CHOH��(CH3)2CHOH����ΪCH3COCH3��CH3COCH3��CH3CH2MgBr��Ӧ����
(CH3)2CHOH��(CH3)2CHOH����ΪCH3COCH3��CH3COCH3��CH3CH2MgBr��Ӧ����![]() ���ϳ�·��Ϊ
���ϳ�·��Ϊ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ6NO2+8NH3=7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ������˵������ȷ����
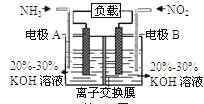
A.�������Ҳ�缫�������غ��������缫
B.A�缫�Ϸ���������Ӧ��BΪ����
C.�缫A����ӦʽΪ2NH3-6e-=N2+6H+
D.����2.24LNO2(��״��) ������ʱ��ת�Ƶ���Ϊ0.4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���������Mg(OH)2������ˮ��Һ�дﵽƽ��ʱ��Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq),ҪʹMg(OH)2�������ӣ�c(OH-)���ӣ��ɲ�ȡ�Ĵ�ʩ��
Mg2+(aq)+2OH-(aq),ҪʹMg(OH)2�������ӣ�c(OH-)���ӣ��ɲ�ȡ�Ĵ�ʩ��
A.��������ˮB.ͨ������HCl����
C.������NaOH����D.������MgSO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����Ͷ������( LiFePO4���)�ܷ�ӦʽΪLi1��xFePO4+LixC6![]() C6+LiFePO4���ڲ��ṹ��ͼ1��ʾ��ֻ��Li+ͨ���ۺ����Ĥ���Դ˵�ص��Na2SO4��Һ(�缫����Ϊʯī)�����Ƶ�NaOH��H2SO4����ԭ����ͼ2��ʾ������˵���������
C6+LiFePO4���ڲ��ṹ��ͼ1��ʾ��ֻ��Li+ͨ���ۺ����Ĥ���Դ˵�ص��Na2SO4��Һ(�缫����Ϊʯī)�����Ƶ�NaOH��H2SO4����ԭ����ͼ2��ʾ������˵���������

A. ��طŵ�ʱ��LixC6�ڸ�������������Ӧ
B. ��طŵ�ʱ��������ӦʽΪ Lil��xFePO4+xLi��+xe��= LiFePO4
C. ���ʱ��ͼ2��b�缫��ӦʽΪ2H2O��4e��=O2��+4H+
D. ���ʱ����ת��0.2mol���ӣ�A�ڲ������������1.6g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ԷϾ�п�̵�س���������ѡ���ĺ��̷���(MnO2��MnOOH��MnO������Fe��Pb�ȣ�Ϊԭ���Ʊ��ߴ�MnCl2��xH2O��ʵ���̵��������á��乤���������£�
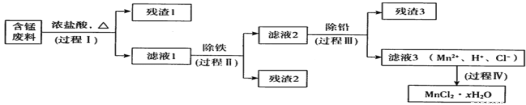
����a:Mn�Ľ������ǿ��Fe��Mn2+�����������±Ƚ��ȶ���pH����5.5ʱ�ױ�O2������
����b�������������������pH
Mn��OH��2 | Pb��OH��2 | Fe��OH��3 | |
��ʼ����ʱ | 8.1 | 6.5 | 1.9 |
��ȫ����ʱ | 10.1 | 8.5 | 3.2 |
ע���������ӵ���ʼŨ��Ϊ0.1 mol��L-l
(1)����I��Ŀ���ǽ����̡���������Һ1�к��е�������ΪMn2+��Fe3+��Pb2+��H+��
��MnO2��Ũ���ᷴӦ�����ӷ���ʽ��____________��
�ڼ�����Һ1��ֻ��Fe3+����Fe2+�IJ����������ǣ��ֱ�ȡ����������Һ1���Թ��У�һ��__________����һ�� ________________��
��Fe3+��Fe2+ת�����ɣ����ܷ����ķ�Ӧ�У�
a. 2Fe2++Cl2= 2Fe3++2Cl- b.4Fe2++O2+4H+=4Fe3++2H2O
c������ д��c�����ӷ���ʽ��____________________��
(2)���̢��Ŀ���dz��������������ַ�����
i����ˮ��������Һ1��ϡ�ͣ��ټ�����10%�İ�ˮ�����ˡ�
ii�����շ�������ҺlŨ���õ��Ĺ�����290�決�գ���ȴ��ȡ�������ˮ�ܽ⡢���ˣ���Һ�ټ������ữ������pH��
��֪�������з�������Ҫ��ӦΪ2FeCl3+3O2![]() 2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
�ٰ�ˮ������ʱ����ҺpHӦ������__________֮�䡣
�����ַ����Ƚϣ���ˮ��������ȱ����____________��
(3)���̢��Ŀ���dz�Ǧ��������Լ���____________��
(4)���̢����ù����е�x�IJⶨ���£�ȡm1g��Ʒ�����ڵ�����Χ�м�����ʧȥȫ���ᾧˮʱ��������������m2g����x=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ը�����(��Ҫ�ɷ�ΪFeO��Cr2O3������Al2O3��SiO2������)Ϊ��Ҫԭ����������ԭ�Ϻ췯��(��Ҫ�ɷ�Na2Cr2O7��2H2O)������Ҫ����������ͼ��
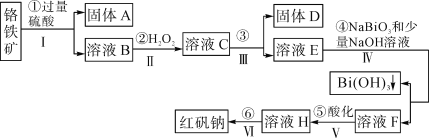
�������ϵ�֪��
��.�����£�NaBiO3������ˮ����ǿ�����ԣ��ڼ��������£��ܽ�Cr3+ת��ΪCrO42-��
��.
�������� | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
��ʼ������pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
������ȫ��pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
�ش��������⣺
��1����Ӧ֮ǰ�Ƚ���ʯ�����Ŀ����___��
��2������ۼӵ��Լ�Ϊ___��Ŀ���ǽ���ҺpHҪ����5ʹFe3+��Al3+����ȫת��ΪFe(OH)3��Al(OH)3��������ȥ��
��3��д����Ӧ�ܵ����ӷ�Ӧ����ʽ___��
��4�������ữ��ʹCrO42-ת��ΪCr2O72-��д���÷�Ӧ�����ӷ���___��
��5������ҺH��������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ����T�ú췯�ƴ־��壬���ƺ췯����Դ־�����Ҫ���õIJ�����___(���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ�м׳ص��ܷ�ӦʽΪ![]() ��
��
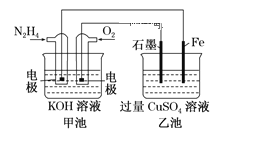
��1���׳��и����ϵĵ缫��ӦʽΪ_____________________��
��2���ҳ���ʯī�缫�ϵ缫��ӦʽΪ_________________________________��
��3��Ҫʹ�ҳػָ������ǰ��״̬��Ӧ����Һ�м��������� _______________��
A��CuO B��Cu(OH)2 C��CuCO3 D��CuSO4
��4�������ҳ��������缫�ijɵ�������Fe��Cu��ʵ����Fe�϶�Cu������������1.6gN2H4ʱ���ҳ��������缫������Ϊ_________________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Y���п������������ã�����X�Ƶá�
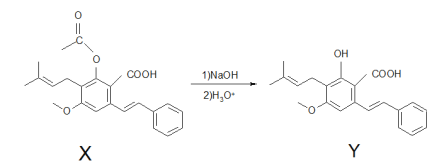
�����йػ�����X��Y��˵����ȷ����
A.X��NaOH��Һ�ܷ�Ӧ����Na2CO3��Һ�� NaHCO3��Һ������Ӧ
B.Y���Ҵ�����������Ӧ�ɵõ�X
C.X��Y������������KMnO4��Һ��Ӧ
D.������X��Y�ֱ�������Br2�ӳɵIJ������������̼ԭ����Ŀ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬѧ���Ѿ�ѧϰ��ͬλ�ء�ͬϵ�ͬ�������塢ͬ���칹�壬����������Щ�����������г��˼������ʣ��뽫���ʵĺ��������д���±��С�
��![]() ��
��![]()
��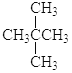 ��
��![]()
��CH4��CH3CH2CH3���ܽ��ʯ��ʯī����뭡����밣���16O��17O��18O�����Ҵ�(CH3CH2OH)�ͼ���(CH3OCH3)��������(O2)�����(O3)��
��� | ͬλ�� | ͬϵ�� | ͬ�������� | ͬ���칹�� |
��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com