
【题目】用铜锌合金制成的假金元宝欺骗人的事件屡有发生。下列不易区别其真伪的方法是( )
A.测定密度
B.放入硝酸中
C.放入盐酸中
D.观察外观
科目:高中化学 来源: 题型:
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大改变。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):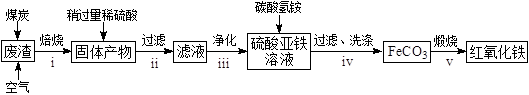
回答下列问题:
①在步骤i中产生的有毒气体可能有。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×1032 , 此时理论上将Al3+沉淀完全,则溶液的pH为。
③步骤iv中,生成FeCO3的离子方程式是。
(3)氯化铁溶液称为化学试剂中的“多面手”。向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生沉淀,写出该沉淀的化学式。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:
复分解反应ii的离子方程式是。
②如今基于普鲁士蓝合成原理可检测食品中是否含CN , 方案如下:![]()
若试纸变蓝则证明食品中含有CN , 请解释检测时试纸中FeSO4的作用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一容积为5L的恒容密闭容器中充入5molA与8molB,在一定条件下反应:2A(g)+3B(g)xC(g)+yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(Lmin),D的平衡浓度为0.3mol/L,又知v(B):v(C)=3:2,则下列说法中正确的是( )
A.x:y=3:1
B.v(A):v(C)=2:1
C.A的平衡浓度为0.4mol/L
D.A与B的平衡浓度之比为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/L NaOH 滴定 25.00mL 0.1000mol/L某一元酸HX,滴定过程中pH 变化曲线如图所示.下列说法正确的是( ) 
A.滴定前,酸中c(H+) 等于碱中c(OH﹣)
B.在A点,c(Na+)>c(X﹣)>c(HX)>c(H+)>c(OH﹣)
C.在B点,两者恰好完全反应
D.在C点,c(X﹣)+c(HX)=0.05 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将浓度为0.1 mol?L﹣1HF溶液加水不断稀释过程中,c(H+)和c(OH﹣)都会减小
B.25℃时,等体积、等pH的HCl、H2SO4、CH3COOH溶液分别与足量锌粉反应,H2SO4溶液产生的H2量最多
C.Na2CO3溶液存在水解平衡:CO ![]() +H2O?HCO
+H2O?HCO ![]() +OH﹣ , 加入NaOH固体会使平衡逆向移动,溶液pH减小
+OH﹣ , 加入NaOH固体会使平衡逆向移动,溶液pH减小
D.25℃时,pH均为8的CH3COONa和NaOH溶液中,由水电解产生的c(OH﹣)之比为100:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示的装置和以下实验步骤,可以制取少量的溴苯和溴乙烷.已知乙醇在一定条件下与氢溴酸反应可制备溴乙烷:
C2H5OH+HBr→C2H5Br+H2O
主要实验步骤如下:①连接好装置,检查装置的气密性;②向烧瓶中加入一定量的苯和液溴.向锥形瓶中加入乙醇和浓H2SO4的混合液至稍高于进气导管口处;③将A装置中的纯铁丝小心向下插入混合液中;④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min.
请填写下列空白:
(1)写出制取溴苯的化学方程式: .
(2)步骤③中观察到的现象是: .
(3)C装置中U形管内部用蒸馏水封住管底的作用是: .
(4)反应完毕后,U形管内的现象是: . 分离溴乙烷时所用的最主要仪器的名称是(只填一种) .
(5)实验结束,从烧瓶的混合物中分离出粗制黄色的溴苯,产生黄色的原因是其中含有(填化学式).欲得到无色的溴苯的方法是(填试剂和操作名称).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如下图所示。

(1)根据上图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的_____。
a.SO2 b.NOx c.VOCs d. NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式_______。

(3)SO2是气体污染物的主要成分之一。作为一种化学性质活泼的物质,它能发生多种反应,请按照下表提示,从不同角度梳理SO2不同类的化学性质,将化学方程式填在下表中。
SO2性质梳理 | 化学方程式 | |
物质类别 | 酸性氧化物 | ①SO2+H2O |
②SO2+CaO=CaSO3 | ||
③_______ | ||
S元素价态 | S为+4价 | ①_______ |
②SO2 +2H2S=3S+2H2O | ||
(4)科学家经过研究发现中国霾呈中性,其主要原因如下图所示:
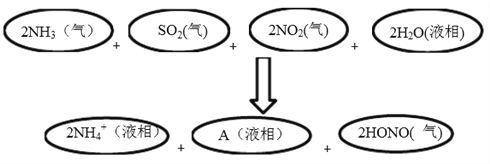
请判断A的化学式并说明判断理由:______________________。
(5)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
离子 | Na+ | SO42 | NO3 | H+ | Cl |
浓度/(mol·L1) | 5.5×103 | 8.5×104 | y | 2.0×104 | 3.4×103 |
①SO2和NaClO2溶液反应的离子方程式是_________________。
②表中y =______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离方法正确的是
A. 分离汽油和水可以用结晶的方法
B. 除去氯化钠溶液中的泥沙用分液的方法
C. 分离醋酸(沸点118℃)与乙酸乙酯(沸点77.1℃)用蒸馏的方法
D. 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾用过滤的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
(1)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4 =2ClO2↑+O2↑+2Na2SO4+2H2O
①方法一的离子方程式为____________________________________.
②方法二中被氧化的物质是___________,若反应中有0.1mol电子转移,则产生的ClO2气体在标准状况下的体积为___________L,在下面的化学方程式上用双线桥标出电子转移的方向和数目
2NaClO3+H2O2+H2SO4 =2ClO2↑+O2↑+2Na2SO4+2H2O___________
③某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3- 的浓度之比为1:1,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为____________;
(2)现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL 0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释、冷却 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
①应量取的浓硫酸体积是__________,实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有_________________;
②将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母)_________________________。
A. 用量筒量取浓硫酸时,仰视量筒的刻度
B. 容量瓶未干燥即用来配制溶液
C. 浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容
D. 往容量瓶转移时,有少量液体溅出
E. 烧杯未进行洗涤
F. 在容量瓶中定容时俯视容量瓶刻度线
G. 定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com