
����Ŀ����ҵ���ó�����Fe2O3��FeO��Ҳ����Al2O3��MnO2��CuO��SiO2�ȣ��Ʊ��̷�FeSO4��7H2O���������£�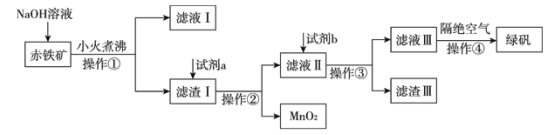
��1������������Һ����������з�����Ӧ�����ӷ���ʽΪ___________________________��
________________________________��
��2�����������м���������Լ�aΪ___________���������Լ�bͶ�뵽��Һ���������з�Ӧ�����ӷ���ʽΪ__________________________��________________________________��
___________________________________��
��3��ʵ�����в����٢ڢ۵�����Ϊ_________________________��
��4�������ܸ���������Ŀ����_______________________________________________��
���𰸡� Al2O3 +2OH-=2AlO2��+H2O SiO2+ 2OH-=SiO32-+ H2O ����(H2SO4) Fe��2Fe3+��3Fe2+ Fe��Cu2+��Cu��Fe2+ Fe��2H+��H2����Fe2+ ���� ��ֹ��Һ�е�Fe2+����������ΪFe3+
����������������������̿�֪����������������������Һ��ȡʱ���������Ͷ��������ܽ⣬���ˣ�������I�м���������ϡ���ᣬ���е������������������Լ�����ͭ�ܽ⣬���ˣ�����Һ�м������ۣ�����Һ�е�Fe3+��Cu2+��ԭ�����˵õ�����������Һ������Һ����Ũ�������½ᾧ�����ˡ�ϴ�ӡ�����õ��̷���
��1������������Һ����������з�����Ӧ�����ӷ���ʽΪAl2O3 +2OH-=2AlO2��+H2O��
SiO2+ 2OH-=SiO32-+ H2O��
��2�����������м���������Լ�aΪ����(H2SO4)���������Լ�b�����ۣ�Ͷ�뵽��Һ���������з�Ӧ�����ӷ���ʽΪFe��2Fe3+��3Fe2+��Fe��Cu2+��Cu��Fe2+��Fe��2H+��H2����Fe2+��
��3��ʵ�����в����٢ڢ۵�����Ϊ���ˡ�
��4�������ܸ���������Ŀ���Ƿ�ֹ��Һ�е�Fe2+����������ΪFe3+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�����������˵���д������
A. 1 mol H2���е�ԭ����Ϊ2NA
B. NA��ˮ�����к�����ԭ�ӵ����ʵ���Ϊ2 mol
C. 1 mol O2�к��еķ�����Ϊ2NA
D. 0.25 mol H2SO4����NA��Oԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A����;���Ľ�����B��C�����ֳ������嵥�ʣ�E��ҺΪ����ǿ�ᣬD��Һ�еμ�KSCN��Һ��Ѫ��ɫ�������ת����ϵ��ͼ��ʾ��
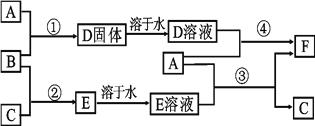
��ش�
��1��д��B���ʵĻ�ѧʽ��____��F�Ļ�ѧ���ƣ�____��
��2��д���ڢڲ�C��B��ȼ�յķ�Ӧ����____��
��3��д���ڢܲ���Ӧ�Ļ�ѧ��Ӧ����ʽ____��
��4��F��Һ�е���NaOH��Һ���ܲ�����ʵ��������____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�������建��ͨ��ʢ�������Լ����Լ�ƿA���Թ�B�����Թ�B�в��ܹ۲쵽�����������(����)
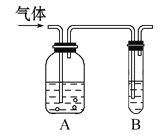
ѡ�� | ���� | A���Լ� | B���Լ� |
A | SO2��CO2 | ����KMnO4��Һ | ����ʯ��ˮ |
B | Cl2��HCl | ����NaCl��Һ | KI������Һ |
C | CO2��HCl | ����NaHCO3��Һ | NaAlO2��Һ |
D | NH3��CO2 | Ũ���� | ��̪��Һ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ�õ�����Ҫ����Դ��
��1����25�桢101kPa�£�16g�ļ״���CH3OH����ȫȼ������CO2��Һ̬ˮʱ�ų�352kJ�����������ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ
��2����ѧ��Ӧ�зų������ܣ��ʱ䣬��H���뷴Ӧ���������ļ��ܣ�E���йأ�
��֪��H2��g��+Cl2��g���T2HCl ��g����H=��185kJ/mol��
E��H��H��=436kJ/mol��E��Cl��Cl��=243kJ/mol��E��H��Cl��=
��3��2SO2��g��+O2��g��=2SO3��g����Ӧ���̵������仯��ͼ1��ʾ����֪1mol SO2��g������Ϊ1mol SO3�ġ�H=��99kJmol��1 �� ��ش��������⣺ 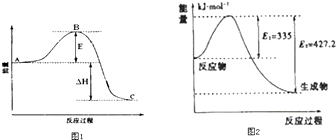
��ͼ�С�H=KJmol��1��
�ڸ÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�������ǽ��ͣ� ��
��4������ͼ2��N2��H2��Ӧ����2mol NH3�����������仯ʾ��ͼ�������ÿ����1mol NH3�ų�����Ϊ�� ��
������ʼʱ�������ڷ���1mol N2��3mol H2 �� ��ƽ���N2��ת����Ϊ20%����Ӧ�ų�������ΪQ1 kJ����Q1����ֵΪ������ͬ����������г���2mol N2��6mol H2 �� ��ƽ���ų�������ΪQ2 kJ����Q22Q1�����������������=����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������Ҫ�ò����������в�����������ͬ����( )
�ٹ��� ������ ���ܽ� ��������ƿת��Һ�� ��pH��ֽ��ʹ��
A. �ٺ͢� B. �ٺ͢� C. �ۺ͢� D. �ٺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ�Ļ�ѧ��ȤС����������ʵ��װ��̽��������������ʣ���֪Na2SO3��H2SO4(Ũ)===Na2SO4��SO2����H2O��E����װ������д̼�����ζ����ʹʪ��ĺ�ɫʯ����ֽ������
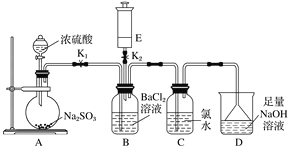
ʵ�鿪ʼʱ�ر�K2��K1���ӷ�Һ©��������ƿ�ڼ���Ũ���ᡣ
(1)B�������________________��
(2)д��C�з�Ӧ�Ļ�ѧ����ʽ��_______________________________________��
(3)D��������___________________________________________________��
��Ӧ�����ӷ���ʽΪ_______________________________________________��
(4)A�з�Ӧ��ɺر�K1����K2����E�е�����ע��B�У��۲쵽B��������________________________��
��Ӧ�����ӷ���ʽΪ_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[���ʽṹ������]
һ���ѧ�о��ɹ�������ͭ�������CuMn2O4�����ڳ����´����������е�һ����̼�ͼ�ȩ��HCHO����
��1����һ�����ʵ���Ũ�ȵ�Cu��NO3��2 ��Mn��NO3��2 ��Һ�м���Na2CO3 ��Һ�����ó������������գ����Ƶ�CuMn2O4 ��
��Mn2+��̬�ĵ����Ų�ʽ�ɱ�ʾΪ ��
��NO3���Ŀռ乹��������������������
��2����ͭ��������Ĵ��£�CO ������ΪCO2 �� HCHO ������ΪCO2 ��H2O��
�ٸ��ݵȵ�����ԭ����CO ���ӵĽṹʽΪ ��
��H2O ������O ԭ�ӹ�����ӻ�����Ϊ ��
��1mol CO2 �к��еĦҼ���ĿΪ ��
��3����CuSO4 ��Һ�м������NaOH ��Һ������[Cu ��OH��4]2�� �� �����ǿռ乹�ͣ�[Cu��OH��4]2���Ľṹ����ʾ��ͼ��ʾΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ת����ϵ���е�������δ�г��������У�DΪ�GΪ�ᣬ��������G ��Ũ��Һ�л�ۻ���F����Һ��ֻ��һ�����ʣ�
A��B��C��D��E����Q��R��X��T���ֶ�����Ԫ���е����ֻ�������ɣ���Q��R��X��Tԭ��������������X�������������ǵ��Ӳ�����3����R��X���ڣ�Q��Tͬ���壬QΪ�ǽ���Ԫ�أ�TΪ����Ԫ�أ���
��1��X�����ڱ��е�λ���� �� R��X��T��ԭ�Ӱ뾶��С�����˳��Ϊ����Ԫ�ط��ű�ʾ����
��2��A��G�����ʵ�����Ӧ�����ˮ��Һ���ԣ���ԭ�������ӷ���ʽ��ʾΪ��
��3��A��X2��Ӧ�Ļ�ѧ����ʽΪ��
��4��pH��Ϊ12��D��Һ��F��Һ�У�ˮ�������c��OH����֮��Ϊ��
��5��Ϊ����������ͨ����װ����β������װ�ã�ʹβ���е�E��CO��Ӧת��Ϊ���ֿ����ijɷ֣�����Ӧת��1 mol����ʱ�����ɵ������ڱ�״���µ������ΪL��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com