
【题目】将2.7g铝和4.6g钠同时加入足量的水中充分反应,将反应后的溶液稀释、定容为500mL。下列说法中正确的是( )
A. 反应中放出的气体在标准状况下的体积为2.24 L
B. 参加反应的水的质量与加入铝的质量相等
C. 所得溶液中钠离子和铝离子物质的量之比为2∶1
D. 所得溶液中阳离子和阴离子的物质的量之比为1∶1
【答案】D
【解析】
4.6 g钠的物质的量为![]() 0.2mol,2.7gAl的物质的量为
0.2mol,2.7gAl的物质的量为![]() 0.1mol;Na和水反应:
0.1mol;Na和水反应:
2 Na + 2H2O ═2 NaOH+ H2↑
0.2mol 0.2mol 0.2mol0.1mol
生成n(NaOH)=0.2mol,
NaOH和Al反应:
2 Al+ 2 NaOH+ 2H2O ═ 2 NaAlO2+ 3 H2↑
0.1mol0.1mol0.1mol 0.1mol0.15mol
NaOH过量,Al完全反应,反应后的溶质物为0.1molNaAlO2、0.1molNaOH。
A、因钠与水反应和铝与碱反应都放出气体,气体在标准状况下的体积为22.4L/mol×(0.1+0.15)mol=5.6L,故A错误;
B、因反应共消耗水0.3mol,质量为5.4g,Al的质量为2.7g,则参加反应的水的质量与加入铝的质量不相等,故B错误;
C、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,没有Al3+,故C错误;
D、因反应后溶液中含有0.1molNaAlO2、0.1molNaOH,阳离子和阴离子都为1价离子,阳离子和阴离子的物质的量之比为1:1,故D正确。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
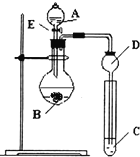
(1)图中D装置名称是______.
(2)N、C、Si的非金属性由强到弱的顺序是:______;从以下所给物质中选出甲同学设计的实验所用到物质:试剂A为______;试剂C为______(填序号).
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3溶液⑤SiO2
(3)①乙同学设计的实验所用到试剂A为______;试剂B为______;试剂C为______.(写名称)
②写出C中发生反应的化学方程式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰) Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知用甲醇制乙烯、丙烯等烯烃时,在温度为400 ℃时,发生的主反应为2CH3OH![]() C2H4+2H2O、3CH3OH
C2H4+2H2O、3CH3OH![]() C3H6+3H2O,副反应为2CH3OH
C3H6+3H2O,副反应为2CH3OH![]() CH3OCH3+H2O。乙烯和丙烯的选择性(转化的甲醇中生成乙烯和丙烯的百分比)及丙烯对乙烯的比值(Cat.1和Cat.2代表两种等量的催化剂)如图所示,下列说法不正确的是
CH3OCH3+H2O。乙烯和丙烯的选择性(转化的甲醇中生成乙烯和丙烯的百分比)及丙烯对乙烯的比值(Cat.1和Cat.2代表两种等量的催化剂)如图所示,下列说法不正确的是
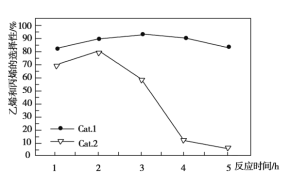
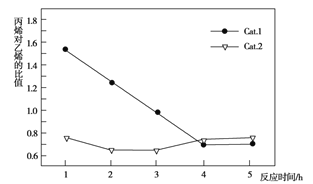
A. 使用Cat.2反应2小时后乙烯和丙烯的选择性下降
B. 使用Cat.1反应3小时后产生的烯烃主要是乙烯
C. 使用Cat.2反应3小时内产生的烯烃主要是丙烯
D. 使用Cat.1时乙烯和丙烯的选择性一直高于使用Cat.2时
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
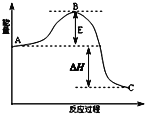
(1)图中A、C分别表示_____________、_____________.
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点_________(填“升高”,“降低”),△H_______(填“变大”,“变 小”或“不变”),理由是______________________.
(3)图中△H=________kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.0g镁在氧气中燃烧后增重0.64g, 但在空气中燃烧时增重不足0.64g,其原因可能是
A. 空气中镁燃烧肯定不完全 B. 空气中部分镁与CO2反应
C. 空气中镁部分与N2反应 D. 空气中镁部分与水蒸气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3—二异丙烯基苯![]() 是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
A.可以发生加成聚合反应B.不能使稀高锰酸钾溶液褪色
C.分子中所有原子共平面D.其苯环上的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。学习物质结构与性质,回答下列问题:
(1)太阳中的主要化学元素是氢和_______。
(2)氢负离子H-基态电子排布式为_______。
(3)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子H-的第一电离能为________。
(4)几种碱金属氢化物的部分性质如下表所示:
氢化物 | LiH | NaH | KH |
密度/g/cm3 | 0.78 | 1.43 | |
分解温度/℃ | 850 | 425 | 400 |
从化学结构的角度回答说明,分解温度LiH>NaH>KH___。
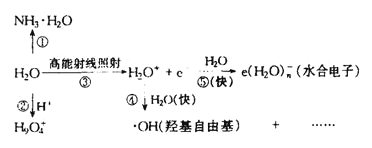
(5)水溶液中有H3O+、H5O2+、H9O4+等微粒的形式。H3O+中,中心原子的杂化类型是___,请画出H5O2+的结构式:______。当用高能射线照射液态水时,水分子便以一种新的方式电离,如图所示写出高能射线照射水的总反应的离子方程式_______。
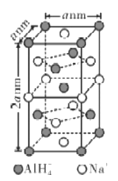
(6)氢化铝钠(NaAlH4)等复合氢化物是重要的有机还原剂。NaAlH4晶胞结构如图所示,NaAlH4晶体中,与Na+紧邻且等距的A1H4-有___个,设阿伏伽德罗常数为NA,则晶体的密度为___g·cm-3。
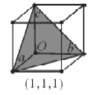
(7)在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面。如图则该立方晶胞体中(1,1,1)晶面共有___个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com