
【题目】化学反应伴随着能量的变化.下列过程中的能量变化不是由化学反应引起的是( )
A.天然气燃烧
B.中和反应
C.冰的融化
D.Ba(OH)28H2O晶体与NH4Cl晶体反应
科目:高中化学 来源: 题型:
【题目】某同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略)。请按要求回答下列问题:
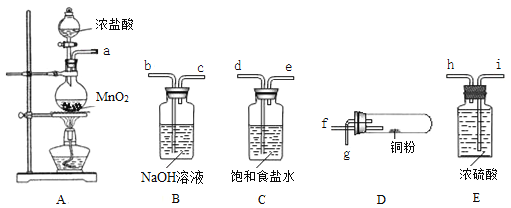
(1)装置A烧瓶中发生反应的化学方程式为_____________________________________。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→______________________。
(3)装置B中发生反应的离子方程式为________________________,装置C中饱和食盐水的作用是__________________________________。
(4)加热装置D时,铜粉发生反应的化学方程式为____________________________。
(5)比较下列两组实验,你认为下列说法正确的是_____(填序号)。
实验①:将足量的二氧化锰与含0.4molHCl的浓盐酸反应。
实验②:将8.7g二氧化锰与足量的浓盐酸反应。
A.①产生的氯气多 B.产生的氯气一样多
C.②产生的氯气多 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
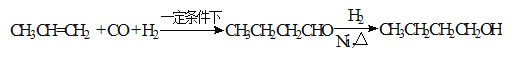
CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置(如下图)
CO↑+H2O,并设计出原料气的制备装置(如下图)
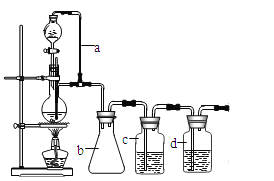
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氢气、丙烯。写出制备丙烯的化学方程式: 。
(2)若用以上装置制备干燥纯净的CO,装置中a的作用是 ,装置中b的作用是 ,c中盛装的试剂是 。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是 (填序号,试剂可重复使用)
①饱和Na2SO3溶液
②酸性KMnO4溶液
③石灰水
④无水CuSO4
⑤品红溶液
(4)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:
①R—CHO+NaHSO3(饱和)![]() RCH(OH)SO3Na↓;
RCH(OH)SO3Na↓;
②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:

试剂1为 ,操作2为 ,操作3为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
A. 足量锌与一定量浓H2SO4反应生成0.5mol气体,反应中转移的电子数为NA
B. 1L 0.1mol/L的CH3COOH溶液中含有H+的数目约为0.1 NA
C. 电解精炼铜(粗铜中含有锌、铁、银等杂质),电路中有2NA个电子通过时,阴极增重64g
D. 常温常压下,1.8 g甲基(-CD3)中含有的电子数为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应: KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O
(1)该反应中,氧化剂是________,氧化产物是________。
(3)当有1.5 mol I2生成时,有________mol还原剂被氧化。
(4)当有4 mol氧化剂参与反应时,转移电子数为________ 个。
II. 周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O = Cu2(OH)2CO3。
(1)该反应中的还原剂是_________,
(2)清除铜锈可以选择的试剂是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求做答
(1)甲烷(CH4)的摩尔质量为_________。
(2)0.5mol H2的质量为______,标准状况下该气体的体积为_________。
(3)5molCO2所含氧原子的数目为__________个。
(4)100mL0.25mol/L Na2SO4溶液中Na+的物质的量浓度是__________mol/L。
(5)有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl﹣)为1.6mol/L,则Al3+的物质的量浓度为______________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将1mLpH=2的一元酸HA溶液加水稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是

A. 加热HA溶液时,溶液酸性增强
B. lmol/LHA溶液与1mol/LNaOH溶液等体积混合,若所得溶液中c(Na+)>c(A-),则2<a<4
C. 某浓度的NaA溶液的pH=d,则其中由水电离出的c(OH-)=1014-d
D. HA溶液与NaOH溶液恰好完全反应时,一定有c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置图合理的是

A. 装置①可实现:Cu+2H2O![]() Cu(OH)2+H2↑
Cu(OH)2+H2↑
B. 装置②能构成锌铜原电池
C. 装置③可用于粗铜的电解精炼
D. 装置④可用于浓硫酸干燥氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com