
����Ŀ��t��ʱ����3molA��1molB����ͨ���ݻ�Ϊ2L���ܱ������У��ݻ����䣩���������·�Ӧ3A(g)+B(g) ![]() xC(g)��2minʱ��Ӧ����ƽ��״̬���¶Ȳ��䣩����ʱ������ʣ����0.8molB�������C��Ũ��Ϊ0.4mol��L��1������д���пհף�
xC(g)��2minʱ��Ӧ����ƽ��״̬���¶Ȳ��䣩����ʱ������ʣ����0.8molB�������C��Ũ��Ϊ0.4mol��L��1������д���пհף�
��1���ӷ�Ӧ��ʼ��ƽ��״̬������C��ƽ����Ӧ����Ϊ ��
��2��x= ��
��3������ԭƽ��������������ٳ���amolC����t��ʱ�ﵽ�µ�ƽ�⣬��ʱB�����ʵ���Ϊn(B)= mol��
��4�������¶Ⱥ�������䣬��ԭƽ�����������ߵ����ʵ��������µ�������ʹƽ�������ƶ����� ������ĸ����
A�������� B�����ӱ� C��������0.4mol D������С0.4mol
��5�����������Ӧ����ͬ�¶Ⱥ��ݻ��������н��У���ʼ����3molA��3molB���ﵽƽ��ʱA���������Ϊa%��������������ʱ�������������Ϊ��ʼ���ʣ�ƽ��ʱA�������������a%���� ������ĸ����
A��2molC B��1molA��3molB��4molC
C��1molB��4molC D��6molA��2molB
���𰸡�
��1��0.2 mol��L��1��min��1��
��2��4��
��3��0.8+0.2a��
��4��D��
��5��A��C��D
��������
�����������1������C��ƽ����Ӧ����v=![]() =
=![]() =0.2mol/��L��min�����ʴ�Ϊ��0.2mol/��L��min����
=0.2mol/��L��min�����ʴ�Ϊ��0.2mol/��L��min����
��2���μӷ�Ӧ��B�����ʵ���=��1-0.8��mol=0.2mol����B�ķ�Ӧ����=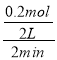 =0.05mol/L��C��ƽ����Ӧ����Ϊ0.2mol/��L��min����ͬһ���淴Ӧ��ͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�B��C�ļ�����֮�ȵ����䷴Ӧ����֮��=0.05mol/��L��min����0.2mol/��L��min��=1��4������x=4���ʴ�Ϊ��4��
=0.05mol/L��C��ƽ����Ӧ����Ϊ0.2mol/��L��min����ͬһ���淴Ӧ��ͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�B��C�ļ�����֮�ȵ����䷴Ӧ����֮��=0.05mol/��L��min����0.2mol/��L��min��=1��4������x=4���ʴ�Ϊ��4��
��3����һ��ƽ��ʱA�����ʵ���Ũ��=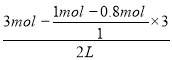 =1.2mol/L��B�����ʵ���Ũ��=
=1.2mol/L��B�����ʵ���Ũ��=![]() =0.4mol/L��C�����ʵ���Ũ��=0.4mol/L����ѧƽ�ⳣ��K=
=0.4mol/L��C�����ʵ���Ũ��=0.4mol/L����ѧƽ�ⳣ��K=![]() =
=![]() ��
��
��ƽ��ʱB�����ʵ���Ϊy��
3A��g�� + B��g�� ![]() 4C��g��
4C��g��
��ʼ 1.2 0.4 0.4
��Ӧ 3��0.4-![]() �� ��0.4-
�� ��0.4-![]() �� 4��0.4-
�� 4��0.4-![]() ��
��
ƽ��[1.2-3��0.4-![]() ��]
��] ![]() [0.4-4��0.4-
[0.4-4��0.4-![]() ��+
��+![]() ]��
]��
�¶Ȳ��䣬��ѧƽ�ⳣ�����䣬��ѧƽ�ⳣ��K= =
=![]() ��y=1.2-
��y=1.2-![]() ���ʴ�Ϊ��1.2-
���ʴ�Ϊ��1.2-![]() ��
��
��4�����Ũ���̴���ƽ�ⳣ������ƽ��������Ӧ�����ƶ���A��������ʱ����Ũ�Ⱦ���ԭ����һ�룬��Ũ����=![]() K=K������ƽ�ⲻ�ƶ����ʴ���B�����ӱ�ʱ����Ũ�Ⱦ���ԭ���Ķ�������Ũ����=
K=K������ƽ�ⲻ�ƶ����ʴ���B�����ӱ�ʱ����Ũ�Ⱦ���ԭ���Ķ�������Ũ����=![]() K=K������ƽ�ⲻ�ƶ����ʴ���C��������0.4mol����Ũ����=
K=K������ƽ�ⲻ�ƶ����ʴ���C��������0.4mol����Ũ����=![]() =��
=��![]() ��3����
��3����![]() ��3��ƽ�����淴Ӧ�����ƶ����ʴ���D��������0.4mol����Ũ����=
��3��ƽ�����淴Ӧ�����ƶ����ʴ���D��������0.4mol����Ũ����=![]() =��
=��![]() ��3����
��3����![]() ��3����ƽ��������Ӧ�����ƶ�������ȷ����ѡD��
��3����ƽ��������Ӧ�����ƶ�������ȷ����ѡD��
��5����Ӧ3A��g��+B��g��![]() 4C��g���У���������ڷ�Ӧǰ����ͬ����һ���¶��£��ں����ܱ������еõ�ƽ��״̬��ֻҪ��������ȫ��ת��ΪA��B��������n��A����n��B��=1��1�����ɵõ���ͬƽ��״̬����Ҫƽ���A�������������a%��˵��ƽ�������ƶ������ݵ�Чƽ�⣬�����ʶ�����ɷ���ʽһ�ߵ����ʣ�����n��A����n��B����1��1���ɡ�A��2molC��ȫת��Ϊ1.5molA��0.5molB���������ʵ���֮��Ϊ3��1��1��1����A��ȷ�� B��1molA��3molB��4molC��ȫת��ΪA��Bʱ��A�����ʵ���Ϊ4molA��4molB�����ߵ����ʵ���֮�ȵ���1��1����Чƽ�⣬��A���������Ϊa%����B����C��1mol B��4molC��C��ȫת��ΪA��Bʱ��A�����ʵ�����3mol��B�����ʵ���Ϊ2mol��A��B�����ʵ���֮��1.5��1����C��ȷ��D��6molA��2molB�����ߵ����ʵ���֮��Ϊ3��1��1������ƽ��ʱA�������������a%����D��ȷ����ѡACD��
4C��g���У���������ڷ�Ӧǰ����ͬ����һ���¶��£��ں����ܱ������еõ�ƽ��״̬��ֻҪ��������ȫ��ת��ΪA��B��������n��A����n��B��=1��1�����ɵõ���ͬƽ��״̬����Ҫƽ���A�������������a%��˵��ƽ�������ƶ������ݵ�Чƽ�⣬�����ʶ�����ɷ���ʽһ�ߵ����ʣ�����n��A����n��B����1��1���ɡ�A��2molC��ȫת��Ϊ1.5molA��0.5molB���������ʵ���֮��Ϊ3��1��1��1����A��ȷ�� B��1molA��3molB��4molC��ȫת��ΪA��Bʱ��A�����ʵ���Ϊ4molA��4molB�����ߵ����ʵ���֮�ȵ���1��1����Чƽ�⣬��A���������Ϊa%����B����C��1mol B��4molC��C��ȫת��ΪA��Bʱ��A�����ʵ�����3mol��B�����ʵ���Ϊ2mol��A��B�����ʵ���֮��1.5��1����C��ȷ��D��6molA��2molB�����ߵ����ʵ���֮��Ϊ3��1��1������ƽ��ʱA�������������a%����D��ȷ����ѡACD��


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ���״����ͽ�����࣬HNO3Ӧ����(����)
���ᡡ���⻯���������ܺ����ᡡ���ѻӷ����ᡡ��ǿ�������ᡡ��һԪ�ᡡ
�����
A���٢ڢۢܢݢޢߢ� B���٢ܢޢߢ�
C���٢� D���٢ܢݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ܱ�������W���У����������������淴Ӧ��
��A(g)+2B(g) ![]() 3C(g)+D(s) ��H1��0 ��xM(g)+N(g)
3C(g)+D(s) ��H1��0 ��xM(g)+N(g) ![]() 3Q(g) ��H2����Ӧ���и������뷴Ӧ���и����ʾ���������Ӧ����ij������ֻ���з�Ӧ����M��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�����ж�W�����н��еķ�Ӧ�ƶϺ�������
3Q(g) ��H2����Ӧ���и������뷴Ӧ���и����ʾ���������Ӧ����ij������ֻ���з�Ӧ����M��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�����ж�W�����н��еķ�Ӧ�ƶϺ�������
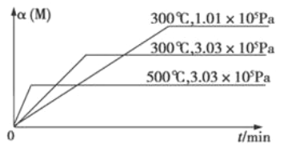
A����Ӧ��һ�����Է���Ӧ����Ӧ��һ���Ƿ��Է���Ӧ
B�����������¶ȱ��ֲ��䣬�� v��(B): v��(C)��2:3
C������ѹ�����£�����N����C�����ʵ�����С
D�������¶ȣ�������Ӧ��ƽ�ⳣ������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ϸ���Ļ������������ȷ����
A. �����ʷ����е�N��Ҫ�����ڰ�����
B. ��ԭ�����մ�л������������
C. ���ATP��DNA��RNA��Ԫ��������ȫ��ͬ
D. ֬�������к�H������࣬����Ҫ����Դ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na+Ũ��Ϊ0.5molL��1��ij������Һ�У������ܺ����±��е����������ӣ�
����֪H2SiO3Ϊ������ˮ�Ľ�״����������ʱ�ֽ�Ϊ������������
������ | K+ | Ag+ | Ca2+ | Ba2+ |
������ | NO3�� | CO32�� | SiO32�� | SO42�� |
��ȡ����Һ100mL��������ʵ��������������ڱ�״���²ⶨ����
����K] | ʵ������ | ʵ���� |
�� | �����Һ�м�������ϡ���� | ������ɫ��״�������ų���״����0.56L���� |
�� | �����ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ��������ù������� | ��������Ϊ2.4g |
�� | ��������Һ�еμ�BaCl2��Һ | ���������� |
��ش��������⣮
��1��ʵ������ȷ��һ�������ڵ������ǣ�
��2��ʵ������������������ӷ���ʽΪ��
��3��ͨ��ʵ�������������ͱ�Ҫ���㣬��д�±��������ӵ�Ũ�����ܼ�����ģ���д��������һ�������ڵ������0��������ȷ���Ƿ���ڵ��������������
������ | NO3�� | CO32�� | SiO32�� | SO42�� |
c/molL��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϩ��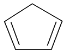 ����һ����Ҫ�Ļ���ԭ�ϣ��������Ի�����Ϊԭ���Ʊ������ϩ�ĺϳ�·�ߣ�
����һ����Ҫ�Ļ���ԭ�ϣ��������Ի�����Ϊԭ���Ʊ������ϩ�ĺϳ�·�ߣ�
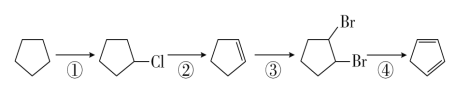
��1�����У���Ӧ�ٵķ�Ӧ������____________����Ӧ�ڵIJ���������__________��
��ҵ�Ͽ��ɻ����ϩ�Ʊ�����飨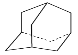 ����;�����£�
����;�����£�
��ش��������⣺
��2�������ϩ�����������________��ԭ�ӹ�ƽ�棻
��3�������ķ���ʽΪ__________��������еĶ��ȴ�����__________�֣�
��4��A�Ƕ��ۻ����ϩ��ͬ���칹�壬���ڷ��������䱽���ϵ�һ�ȴ���ֻ�ж��֣���ʹ������Ȼ�̼��Һ��ɫ������������Ϣ��A�����п��ܽṹ�������������칹���� �֣���д��������֧�����ļ���ͬ���칹��Ľṹ��ʽ��_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����У����ɺ��м��Խ��ķǼ��Է��ӵ��ǣ� ��
A. H2O B. Br2 C. CH4 D. HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��CH4���������ȼ�ϵ�أ�����ȼ�ϵ�صĹ���ԭ����ͼ��������ʾ��ԭ��ع���������OH����������_______________�������缫��ӦʽΪ��_____________������·��ת�Ƶ�����Ϊ0.8NA�������Һ��pH________������������������С����������������������Һ����ı仯�����Ҳ��OH�����ʵ����仯��Ϊ_________��
��2��CH4��H2O�ڸ������������ºʹ��������·�Ӧ��
CH4��g��+H2O��g��![]() CO��g��+3H2��g�� ��H=m kJ��mol��1
CO��g��+3H2��g�� ��H=m kJ��mol��1
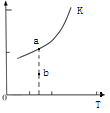
��Ӧ��ƽ�ⳣ������ʽK��______________��K�Ĵ�С���¶���T���Ĺ�ϵ����ͼ��������������ʾ����m__________0�����������������������������ı�ijһ������ʹ״̬��a�㵽��b�㣬�������¶Ȳ��䣬��Ӧ�ٴδﵽƽ��ʱ����CH4��ת����___________������������������С������������������ȷ����������Ӧ���ʱ�����H����_______________������������������С����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
2H2(g) + O2(g)��2H2O(l) ��H��-571.6 kJ/mol
C3H8(g) + 5O2(g)��3CO2(g) +4 H2O(g ) ��H��-2044.0 kJ/mol
(1)������ȼ������__________________��
(2)��֪��H2O(l)��H2O(g ) ��H����44.0 kJ/molд������(C3H8)ȼ�����ɶ�����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��_____________________��
(3)ʵ����H2��C3H8�Ļ�����干3mol����ȫȼ������Һ̬ˮʱ����2791.6 kJ��������������H2��C3H8���������________________��
(4)C3H8(g) + 5O2(g)��3CO2(g) +4 H2O(g ) ��H��-2044.0 kJ/mol����Ӧ��ת��10mol����ʱ��ȼ�յı���(C3H8)��������________ g�����ɵ�CO2�ڱ�״���µ������_________ L��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com