
ΓΨΧβΡΩΓΩΘ®IΘ©“―÷Σ‘Ύ448Γφ ±Θ§Ζ¥”ΠH2(g)ΘΪI2(g)![]() 2HI(g)ΒΡΤΫΚβ≥Θ ΐK1ΈΣ49Θ§‘ρΗΟΈ¬Ε»œ¬Ζ¥”Π
2HI(g)ΒΡΤΫΚβ≥Θ ΐK1ΈΣ49Θ§‘ρΗΟΈ¬Ε»œ¬Ζ¥”Π![]() H2(g)ΘΪ
H2(g)ΘΪ![]() I2(g)
I2(g)![]() HI(g)ΒΡΤΫΚβ≥Θ ΐK2ΈΣ____________ΓΘ
HI(g)ΒΡΤΫΚβ≥Θ ΐK2ΈΣ____________ΓΘ
Θ®IIΘ©‘Ύ“ΜΕ®ΧεΜΐΒΡΟή±’»ίΤς÷–Ϋχ––»γœ¬Μ·―ßΖ¥”ΠΘΚCO2(g)ΘΪH2(g)![]() CO(g)ΘΪH2O(g)Θ§ΤδΜ·―ßΤΫΚβ≥Θ ΐ(K)ΚΆΈ¬Ε»(t)ΒΡΙΊœΒ»γ±μΥυ ΨΘΚ
CO(g)ΘΪH2O(g)Θ§ΤδΜ·―ßΤΫΚβ≥Θ ΐ(K)ΚΆΈ¬Ε»(t)ΒΡΙΊœΒ»γ±μΥυ ΨΘΚ
t/Γφ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣKΘΫ________ΓΘ
Θ®2Θ©ΗΟΖ¥”ΠΈΣ________(ΧνΓΑΈϋ»»Γ±ΜρΓΑΖ≈»»Γ±)Ζ¥”ΠΓΘ
Θ®3Θ©Ρή≈–ΕœΗΟΖ¥”Π¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ“άΨί «________ΓΘ
A.»ίΤς÷–―Ι«Ω≤Μ±δ B.ΜλΚœΤχΧε÷–c(CO)≤Μ±δ
C.v’ΐ(H2)ΘΫvΡφ(H2O) D.c(CO2)ΘΫc(CO)
Θ®4Θ©Ρ≥Έ¬Ε»œ¬Θ§ΤΫΚβ≈®Ε»ΖϊΚœœ¬ ΫΘΚc(CO2)ΓΛc(H2)ΘΫc(CO)ΓΛc(H2O)Θ§ ‘≈–Εœ¥Υ ±ΒΡΈ¬Ε»ΈΣ________ΓφΓΘ
Θ®5Θ©‘Ύ800Γφ ±Θ§ΖΔ…ζ…œ ωΖ¥”ΠΘ§Ρ≥ ±ΩΧ≤βΒΟ»ίΤςΡΎΗςΈο÷ ΒΡ≈®Ε»Ζ÷±πΈΣc(CO2)ΈΣ2molΓΛLΘ≠1Θ§c(H2)ΈΣ1.5molΓΛLΘ≠1Θ§c(CO)ΈΣ1molΓΛLΘ≠1Θ§c(H2O)ΈΣ3molΓΛLΘ≠1Θ§‘ρœ¬“Μ ±ΩΧΘ§Ζ¥”ΠΫΪ________(ΧνΓΑ’ΐœρΓ±ΜρΓΑΡφœρΓ±)Ϋχ––ΓΘ
ΓΨ¥πΑΗΓΩ7 ![]() Έϋ»» BC 830 Ρφœρ
Έϋ»» BC 830 Ρφœρ
ΓΨΫβΈωΓΩ
Θ®ΔώΘ©Μ·―ßΦΤΝΩ ΐΈΣ±Ε ΐΙΊœΒ ±ΤΫΚβ≥Θ ΐΈΣΤΫΖΫΙΊœΒΘΜ
Θ®ΔρΘ©ΤΫΚβ≥Θ ΐΈΣ…ζ≥…Έο≈®Ε»Οί÷°Μΐ”κΖ¥”ΠΈο≈®Ε»Οί÷°ΜΐΒΡ±»Θ§ΗυΨίΈ¬Ε»…ΐΗΏΘ§ΤΫΚβ≥Θ ΐ±δ¥σά¥≈–Εœ»»–ß”ΠΘ§άϊ”ΟΤΫΚβΒΡΧΊ’ςΓΑ»ñʢΓΑΕ®Γ±ά¥≈–Εœ «Ζώ¥οΤΫΚβΉ¥Χ§Θ§ΗυΨί≈®Ε»ΚΆΤΫΚβ≥Θ ΐά¥ΦΤΥψΤΫΚβ≥Θ ΐΘ§¥”Εχ»ΖΕ®Έ¬Ε»Θ§ΗυΨί800Γφ ±Θ§Qc”κK±»Ϋœ≈–ΕœΖ¥”ΠΒΡΖΫœρΓΘ
Θ®IΘ©Θ°448Γφ ±Θ§Ζ¥”ΠH2(g)+I2(g)2HI(g)ΒΡΤΫΚβ≥Θ ΐK1ΈΣ49Θ§Ζ¥”Π![]() H2(g)ΘΪ
H2(g)ΘΪ![]() I2(g)
I2(g)![]() HI(g)ΒΡΤΫΚβ≥Θ ΐK2ΈΣ
HI(g)ΒΡΤΫΚβ≥Θ ΐK2ΈΣ![]() Θ§Ι ¥πΑΗΈΣΘΚ7ΘΜ
Θ§Ι ¥πΑΗΈΣΘΚ7ΘΜ
Θ®IIΘ©Θ®1Θ©ΤΫΚβ≥Θ ΐΈΣ…ζ≥…Έο≈®Ε»Οί÷°Μΐ”κΖ¥”ΠΈο≈®Ε»Οί÷°ΜΐΒΡ±»Θ§‘ρCO2(g)+H2(g)CO(g)+H2O(g)ΒΡΤΫΚβ≥Θ ΐK=![]() Θ§Ι ¥πΑΗΈΣΘΚ
Θ§Ι ¥πΑΗΈΣΘΚ![]() ΘΜ
ΘΜ
Θ®2Θ©”…Έ¬Ε»…ΐΗΏΘ§ΤΫΚβ≥Θ ΐ±δ¥σΩ…÷ΣΘ§…ΐΗΏΈ¬Ε»Θ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§‘ρ’ΐΖ¥”ΠΈΣΈϋ»»Ζ¥”ΠΘ§Ι ¥πΑΗΈΣΘΚΈϋ»»ΘΜ
Θ®3Θ©AΘ°ΗΟΖ¥”ΠΈΣΤχΧεΒΡΈο÷ ΒΡΝΩ≤Μ±δΒΡΖ¥”ΠΘ§‘ρ»ίΤς÷–―Ι«Ω Φ÷’≤Μ±δΘ§≤ΜΡήΉςΈΣ≈–Ε®ΤΫΚβΒΡΖΫΖ®Θ§Ι A¥μΈσΘΜ
BΘ°ΜλΚœΤχΧε÷–c(CO)≤Μ±δΘ§‘ρ¥οΒΫΜ·―ßΤΫΚβΘ§Ι B’ΐ»ΖΘΜ
CΘ°v(H2)’ΐ=v(H2O)ΡφΘ§‘ρΕ‘”Ύ«βΤχά¥ΥΒ’ΐΡφΖ¥”ΠΥΌ¬ œύΒ»Θ§‘ρ¥οΒΫΤΫΚβΘ§Ι C’ΐ»ΖΘΜ
DΘ°c(CO2)=c(CO)Θ§ΗΟΖ¥”Π≤Μ“ΜΕ®¥οΒΫΤΫΚβΘ§≈®Ε»ΙΊœΒ»ΓΨω”ΎΖ¥”ΠΈοΒΡΤπ ΦΝΩΚΆΉΣΜ·¬ Θ§Ι D¥μΈσΘΜΙ ¥πΑΗΈΣΘΚBCΘΜ
Θ®4Θ©c(CO2)c(H2)=c(CO)c(H2O) ±Θ§ΤΫΚβ≥Θ ΐK=1Θ§‘ρΗΟΈ¬Ε»ΈΣ830ΓφΘ§Ι ¥πΑΗΈΣΘΚ830ΘΜ
Θ®5Θ©‘Ύ800Γφ ±Θ§K=0.9,Qc=![]() =
=![]() =1>KΘ§Υυ“‘Μ·―ßΖ¥”ΠœρΡφΖ¥”ΠΖΫœρΫχ––Θ§Ι ¥πΑΗΈΣΘΚΡφœρΓΘ
=1>KΘ§Υυ“‘Μ·―ßΖ¥”ΠœρΡφΖ¥”ΠΖΫœρΫχ––Θ§Ι ¥πΑΗΈΣΘΚΡφœρΓΘ


 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥÷÷ΒγΕΤΖœΥ°Κ§A“θάκΉ”Θ§≈≈Ζ≈«ΑΒΡ¥ΠάμΙΐ≥Χ»γœ¬ΘΚ
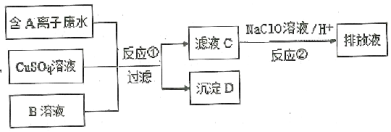
ΦΚ÷ΣΘΚ4.5g≥ΝΒμD‘Ύ―θΤχ÷–ΉΤ…’ΚσΘ§≤ζ…ζ4.0gΚΎ…ΪΙΧΧεΘ§…ζ≥…ΒΡΈό…ΪΈόΈΕΤχΧεΆ®ΙΐΉψΝΩ≥Έ«ε ·Μ“Υ° ±Θ§≤ζ…ζ5.0gΑΉ…Ϊ≥ΝΒμΘ§ΉνΚσΒΟΒΫΒΡΜλΚœΤχΧε≥ΐ»Ξ―θΤχΚσΘ§ΜΙ Θ”ύ±ξΉΦΉ¥Ωωœ¬ΟήΕ»ΈΣ1.25gΓΛL-1ΒΡΒΞ÷ ΤχΧεE 560mLΓΘ
(1)EΒΡΫαΙΙ ΫΈΣ____________ΓΘ
(2)–¥≥ω≥ΝΒμD‘Ύ―θΤχ÷–ΉΤ…’ΖΔ…ζΒΡΜ·―ßΖΫ≥Χ Ϋ_______________________________ΓΘ
(3)»ή“ΚBΨΏ”––‘÷ ____________(ΧνΓΑ―θΜ·–‘Γ±ΜρΓΑΜΙ‘≠–‘Γ±)ΓΘ
(4)¬Υ“ΚC÷–ΜΙΚ§”–ΈΔΝΩΒΡAάκΉ”Θ§Ά®ΙΐΖ¥”ΠΔΎΘ§Ω…ΫΪΤδΉΣΜ·ΈΣΕ‘ΜΖΨ≥ΈόΚΠΒΡΈο÷ Θ§”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΗΟΖ¥”ΠΈΣ______________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß≤…”ΟΝρΧζΩσ±Κ…’»ΓΝρΚσΒΡ…’‘ϋ(÷ς“Σ≥…Ζ÷ΈΣFe2O3ΓΔSiO2ΓΔAl2O3Θ§≤ΜΩΦ¬«ΤδΥϊ‘”÷ )÷Τ»ΓΤΏΥ°ΚœΝρΥα―«Χζ(FeSO4ΓΛ7H2O)Θ§…ηΦΤΝΥ»γœ¬Νς≥ΧΘΚ

œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A. »ήΫβ…’‘ϋ―ÔϹψΝΩΝρΥαΘ§ ‘ΦΝX―Γ”ΟΧζΖέ
B. ΙΧΧε1÷–“ΜΕ®Κ§”–SiO2Θ§ΩΊ÷ΤpH «ΈΣΝΥ ΙAl3+ΉΣΜ·ΈΣAl(OH)3Θ§Ϋχ»κΙΧΧε2
C. ¥”»ή“Κ2ΒΟΒΫFeSO4ΓΛ7H2O≤ζΤΖΒΡΙΐ≥Χ÷–Θ§–κΩΊ÷ΤΧθΦΰΖά÷ΙΤδ―θΜ·ΚΆΖ÷Ϋβ
D. »τΗΡ±δΖΫΑΗΘ§‘Ύ»ή“Κ1÷–÷±Ϋ”Φ”NaOH÷ΝΙΐΝΩΘ§ΒΟΒΫΒΡ≥ΝΒμ”ΟΝρΥα»ήΫβΘ§Τδ»ή“ΚΨ≠ΫαΨßΖ÷άκ“≤Ω…ΒΟΒΫFeSO4ΓΛ7H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩI.NO «“Μ÷÷≥ΘΦϊΜ·ΚœΈοΘ§Ε‘ΤδΫχ––―–ΨΩΨΏ”–÷Ί“ΣΒΡΦέ÷ΒΚΆ“β“εΓΘ
Θ®1Θ©2NO(g)+O2(g)=2NO2(g) ΓςH=akJ/molΒΡΖ¥”Πάζ≥Χ”κΡήΝΩ±δΜ·ΙΊœΒ»γΆΦΥυ ΨΓΘ
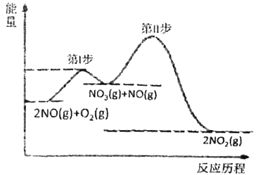
ΔΌa___0(ΧνΘΨΜρΘΦ)
ΔΎ“―÷ΣΘΚΒΎΔρ≤ΫΖ¥”ΠΈΣΘΚNO3(g)+NO(g)=2NO2(g) ΓςH=bkJ/mol
ΒΎI≤ΫΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ___ΓΘ
Θ®2Θ©Τϊ≥ΒΈ≤Τχ÷–≥ΘΚ§”–NOΓΘNH3‘ΎΦ”»»ΚΆ¥ΏΜ·ΦΝ¥φ‘ΎΒΡΧθΦΰœ¬Ρήœϊ≥ΐNOΒΡΈέ»ΨΓΘ
“―÷ΣΘΚ4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΓςH=ΓΣ905kJ/mol
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΓςH=ΓΣ1268kJ/mol
NH3”κNOΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ___ΓΘ
Θ®3Θ©ΙΛ“Β…œNOΒΡ÷Ί“Σά¥‘¥ «NH3Θ§NH3“≤Ω…ΉςΈΣ»ΦΝœ…ηΦΤ≥…Φν–‘»ΦΝœΒγ≥ΊΘ§‘ΎΦν–‘ΧθΦΰœ¬Θ§»ΦΝœΒγ≥Ί≤ζΈο÷ς“ΣΈΣN2ΓΘ»ΦΝœΒγ≥ΊΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ___ΓΘΑ±ΤχΉςΈΣ»ΦΝœΒΡΒγ≥ΊΚΆΚ§ΧΦΜ·ΚœΈοΉςΈΣ»ΦΝœΒΡΒγ≥Ίœύ±»Θ§÷ς“ΣΒΡ”≈Βψ «___ΓΘ
II.Κ§““ΥαΡΤΚΆΕ‘¬»Ζ”![]() ΒΡΖœΥ°Ω…Ά®Ιΐ»γœ¬ΉΑ÷Ο¥ΠάμΘ§Τδ‘≠άμ»γΆΦΥυ ΨΘΚ
ΒΡΖœΥ°Ω…Ά®Ιΐ»γœ¬ΉΑ÷Ο¥ΠάμΘ§Τδ‘≠άμ»γΆΦΥυ ΨΘΚ
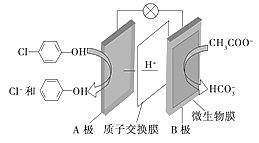
Θ®1Θ©–¥≥ωHCO3-ΒΡΒγΉ” Ϋ___ΓΘ““ΥαΡΤ÷–Κ§”–ΒΡΜ·―ßΦϋάύ–Ά”–___ΓΘ
Θ®2Θ©Βγ≥ΊΒΡ’ΐΦΪ «___Θ§»ή“Κ÷–H+ΒΡ“ΤΕ·ΖΫœρ «___(ΧνAΓζBΜρBΓζA)
Θ®3Θ©BΦΪΖΔ…ζΒΡΒγΦΪΖ¥”ΠΖΫ≥Χ ΫΈΣ___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΓΑΟΚ÷Τ”ΆΓ±ΒΡΙΊΦϋΦΦ θ «ΟΚΒΡΤχΜ·Θ§ΡΩ«ΑΟΚΒΡΤχΜ·÷ς“Σ «ΟΚ÷–ΒΡΧΦΚΆΥ°’τΤχΖ¥”ΠΘΚ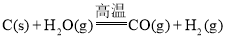 Θ§ΗΟΖ¥”Π «Έϋ»»Ζ¥”ΠΘ§Ζ¥”ΠΥυ–ηΡήΝΩ «”…Φδ–ΣΫχ––ΒΡΧΦΒΡ»Φ…’Θ®―θΤχ”ΟΩ’Τχ¥ζΧφΘ©ά¥ΧαΙ©ΒΡΘΚ
Θ§ΗΟΖ¥”Π «Έϋ»»Ζ¥”ΠΘ§Ζ¥”ΠΥυ–ηΡήΝΩ «”…Φδ–ΣΫχ––ΒΡΧΦΒΡ»Φ…’Θ®―θΤχ”ΟΩ’Τχ¥ζΧφΘ©ά¥ΧαΙ©ΒΡΘΚ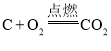 ΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
ΓΘœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.ΟΚΒΡΤχΜ·Ω…“‘Φθ…ΌΟΚ÷±Ϋ”»Φ…’Ε‘ΜΖΨ≥‘λ≥…ΒΡΖέ≥ΨΈέ»Ψ
B.ΒΎ“ΜΗωΖ¥”Π–η“ΣΈϋ»»Θ§Υυ“‘ΟΚΒΡΤχΜ·¥”ΡήΝΩΫ«Ε»ά¥Ω¥Θ§ΒΟ≤Μ≥Ξ ß
C.ΟΚΤχΜ·ΚσΉςΈΣ»ΦΝœΘ§»Φ…’≥δΖ÷Θ§»»άϊ”Ο¬ ΗΏ
D.…œ ωΝΫΗωΖ¥”ΠΘ§Ζ¥”ΠΚσΒΡΜλΚœΤχΧε÷–≥ΐ»Ξ![]() ΓΔ
ΓΔ![]() Κσ÷ς“Σ «Κœ≥…Α±ΒΡΝΫ÷÷‘≠ΝœΤχΧε
Κσ÷ς“Σ «Κœ≥…Α±ΒΡΝΫ÷÷‘≠ΝœΤχΧε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΓΑΧΦ≤ΕΉΫΦΦ θΓ± «÷ΗΆ®Ιΐ“ΜΕ®ΒΡΖΫΖ®ΫΪΙΛ“Β…ζ≤ζ÷–≤ζ…ζΒΡCO2Ζ÷άκ≥ωά¥≤Δάϊ”ΟΓΘ»γΩ…άϊ”ΟNaOH»ή“Κά¥ΓΑ≤ΕΉΫΓ±CO2Θ§ΤδΜυ±ΨΙΐ≥Χ»γΆΦΥυ Ψ(≤ΩΖ÷ΧθΦΰΦΑΈο÷ Έ¥±ξ≥ω)ΓΘ
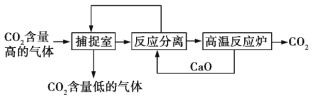
œ¬Ν–”–ΙΊΗΟΖΫΖ®ΒΡ–π ω÷–’ΐ»ΖΒΡ «
ΔΌΡήΚΡ–Γ «ΗΟΖΫΖ®ΒΡ“Μ¥σ”≈Βψ
ΔΎ’ϊΗωΙΐ≥Χ÷–Θ§”–ΝΫ÷÷Έο÷ Ω…“‘―≠ΜΖάϊ”Ο
ΔέΓΑΖ¥”ΠΖ÷άκΓ±ΜΖΫΎ÷–Θ§Ζ÷άκΈο÷ ΒΡΜυ±Ψ≤ΌΉς «Ιΐ¬ΥΓΔ’τΖΔΓΔΫαΨß
ΔήΗΟΖΫΖ®Ω…Φθ…ΌΧΦ≈≈Ζ≈Θ§ΓΑ≤ΕΉΫΓ±ΒΫΒΡCO2ΜΙΩ…”Οά¥÷Τ±ΗΦΉ¥ΦΒ»≤ζΤΖ
A.ΔΌΔέB.ΔΎΔήC.ΔέΔήD.ΔΌΔή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25Γφœ¬Θ§≤ΩΖ÷»θΥαΒΡΒγάκ≥Θ ΐ»γ±μΓΘœ¬Ν–”–ΙΊΥΒΖ®≤Μ’ΐ»ΖΒΡ «
»θΥα | HCOOH | HClO | H2S |
ΒγάκΤΫΚβ≥Θ ΐ(Ka) | Ka=1.0ΓΝ10-4 | Ka=2.0ΓΝ10-8 | Ka1=1.3ΓΝ10-7 Ka2=7.1ΓΝ10-15 |
A. »τ HCOONaΚΆ HCOOHΒΡΜλΚœ»ή“ΚΒΡpH=3Θ§‘ρc(HCOOH)/c(HCOO-)=10
B. œύΆ§≈®Ε»ΒΡ HCOONaΚΆ NaClO»ή“Κ÷–άκΉ”Ήή≈®Ε»«Α’Ώ¥σ
C. »ΈΚΈ≈®Ε»NaHS»ή“Κ÷–Ήή¥φ‘ΎΘΚc(H2S)+c(H+)=c(OHΘ≠)+c(S2Θ≠)
D. œρ NaClO»ή“Κ÷–Ά®»κH2SΖΔ…ζΒΡΖ¥”ΠΈΣ2C1OΘ≠+H2S===S2Θ≠+2HClO
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Μ·―ß―–ΨΩ–‘―ßœΑ–ΓΉιΡΘΡβΙΛ“Β…œ¥”≈®ΥθΒΡΚΘΥ°÷–Χα»Γ“ΚδεΒΡΙΐ≥ΧΘ§…ηΦΤΝΥ»γœ¬ Β―ιΉΑ÷ΟΘ®Φ–≥÷ΉΑ÷Ο¬‘»ΞΘ©ΚΆ≤ΌΉςΝς≥ΧΓΘ“―÷ΣΘΚ![]() ΒΡΖ–ΒψΈΣ59ΓφΘ§ΈΔ»ή”ΎΥ°Θ§”–ΕΨΓΘ
ΒΡΖ–ΒψΈΣ59ΓφΘ§ΈΔ»ή”ΎΥ°Θ§”–ΕΨΓΘ
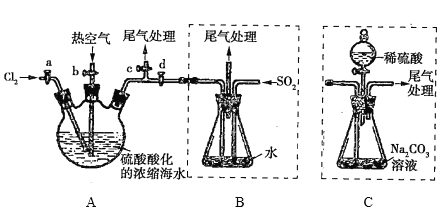
ΔΌΝ§Ϋ”A”κBΘ§ΙΊ±’Μν»ϊbΓΔdΘ§¥ρΩΣΜν»ϊaΓΔcΘ§œρA÷–ΜΚ¬ΐΆ®»κ![]() ÷ΝΖ¥”ΠΆξ»ΪΘΜ
÷ΝΖ¥”ΠΆξ»ΪΘΜ
ΔΎΙΊ±’Μν»ϊaΓΔcΘ§¥ρΩΣΜν»ϊbΓΔdΘ§œρA÷–ΙΡ»κΉψΝΩ»»Ω’ΤχΘΜ
ΔέΫχ––≤Ϋ÷ηΔΎΒΡΆ§ ±Θ§œρB÷–Ά®»κΉψΝΩ![]() ΘΜ
ΘΜ
ΔήΙΊ±’Μν»ϊbΘ§¥ρΩΣΜν»ϊaΘ§‘ΌΆ®ΙΐAœρB÷–ΜΚ¬ΐΆ®»ΥΉψΝΩ![]() ΘΜ
ΘΜ
ΔίΫΪB÷–ΥυΒΟ“ΚΧεΫχ––ίΆ»ΓΓΔΖ÷“ΚΓΔ’τΝσ≤Δ ’Φ·“ΚδεΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1) Β―ι “÷–÷Τ±Η¬»ΤχΒΡΜ·―ßΖΫ≥Χ ΫΈΣ________________________________________________ΓΘ
(2)≤Ϋ÷ηΔΎ÷–ΙΡ»κ»»Ω’ΤχΒΡΉς”Ο «_______________________________________ΓΘ
(3)≤Ϋ÷ηΔέ÷–ΖΔ…ζΒΡ÷ς“ΣΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_______________________________________ΓΘ
(4)Ϋχ––≤Ϋ÷ηΔέ ±Θ§B÷–Έ≤ΤχΩ…”Ο_____Θ®Χν–ρΚ≈Θ©Έϋ ’¥ΠάμΓΘ
a.Υ° b.≈®ΝρΥα c. ![]() »ή“Κ d.±ΞΚΆ
»ή“Κ d.±ΞΚΆ![]() »ή“Κ
»ή“Κ
(5)≤Ϋ÷ηΔί÷–Θ§”Οœ¬ΆΦΥυ ΨΉΑ÷ΟΫχ––’τΝσΘ§ ’Φ·“ΚδεΘ§ΫΪΉΑ÷ΟΆΦ÷–»±…ΌΒΡ÷ς“Σ“«Τς≤ΙΜ≠≥ωά¥___________ΓΘ
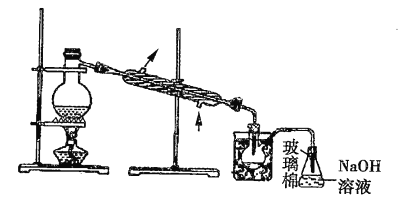
(6)»τ÷±Ϋ”Ν§Ϋ”A”κCΘ§Ϋχ––≤Ϋ÷ηΔΌΚΆΔΎΘ§≥δΖ÷Ζ¥”ΠΚσΘ§œρΉΕ–ΈΤΩ÷–ΒΈΦ”œΓΝρΥαΘ§‘ΌΨ≠≤Ϋ÷ηΔίΘ§“≤Ρή÷ΤΒΟ“ΚδεΓΘΒΈΦ”œΓΝρΥα÷°«ΑΘ§C÷–Ζ¥”Π…ζ≥…ΝΥ![]() Β»Έο÷ Θ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_______________ΓΘ
Β»Έο÷ Θ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_______________ΓΘ
(7)”κBΉΑ÷Οœύ±»Θ§≤…”ΟCΉΑ÷ΟΒΡ”≈ΒψΈΣ______________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–”–ΙΊΜ·―ß”Ο”οΒΡ”ΟΖ®÷–Θ§’ΐ»ΖΒΡ «
A. BaCO3ΒΡΒγάκΖΫ≥Χ Ϋ:BaCO3![]() Ba2++CO32ΓΣ
Ba2++CO32ΓΣ
B. œρΖ–Υ°÷–ΒΈΦ”±ΞΚΆ¬»Μ·Χζ»ή“ΚΒΟΒΫΚλΚ÷…Ϊ“ΚΧεΒΡΜ·―ßΖΫ≥Χ Ϋ:3H2O+FeCl3=3HCl+Fe(OH)3Γΐ
C. œρΥα–‘KI»ή“Κ÷–Ά®»κ≥τ―θ(O3)ΒΡάκΉ”ΖΫ≥Χ ΫΘΚ2IΓΣ+O3+H2O==I2+O2+2OHΓΣ
D. œρBa(OH)2»ή“Κ÷–ΒΈ»κ NaHSO4»ή“Κ÷Ν«ΓΚΟΆξ»Ϊ≥ΝΒμ ±Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫBa2++OHΓΣ+SO42ΓΣ+H+==BaSO4Γΐ+H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com