
【题目】某研究小组拟合成染料X和医药中间体Y。

已知:

回答下列问题:
(1)A的系统命名为________________。
(2)C的结构简式为 ____________。
(3)B到C的反应类型是________________。
(4)C+D→E的化学反应方程式为________ 。
(5)F的分子式为____________。
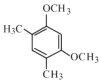
(6)G与A互为同分异构体,请写出满足下列条件的任意两种G的结构简式______________。
①核磁共振氢谱显示G分子中有4个吸收峰;
②红外光谱显示G分子中含有苯环、甲氧基(![]() ),没有羟基、过氧键(-O-O-)
),没有羟基、过氧键(-O-O-)
(7)设计以![]() 和
和![]() 为原料制备Y(
为原料制备Y( )的合成路线(用流程图表示,无机试剂任选)_______________________________________________________。
)的合成路线(用流程图表示,无机试剂任选)_______________________________________________________。
【答案】1,4-苯二酚  还原反应
还原反应 
![]()
 、
、 、
、 、
、![]()
【解析】
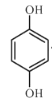 与氯乙烷反应生成A:
与氯乙烷反应生成A: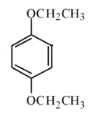 ,A与硝酸反应生成B:
,A与硝酸反应生成B: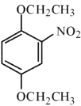 ,B和硫化钠生成C:
,B和硫化钠生成C: ,C和D生成E:
,C和D生成E: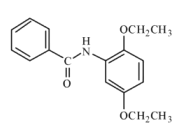 ,E和硝酸生成F:
,E和硝酸生成F: ,F和亚硫酸钠生成X
,F和亚硫酸钠生成X 。
。
(1)A分子中苯环的对位有两个羟基,系统命名为1,4-苯二酚,
故答案为:1,4-苯二酚;
(2) 化合物B的结构简式为 ,发生硝基的还原反应生成C,故C的结构简式为
,发生硝基的还原反应生成C,故C的结构简式为  ,
,
故答案为: ;
;
(3)根据以上分析,B到C的反应类型是还原反应,
故答案为:还原反应;
(4) 利用已知信息分析C和D发生取代反应,所以C+D→E的化学方程式为 ,
,
故答案为: ;
;
(5)由F的结构简式 可知,其分子式为C17H18N2O5,
可知,其分子式为C17H18N2O5,
故答案为:C17H18N2O5;
(6)化合物A的结构简式为 ,其同分异构体要求有四种氢原子,同时含有苯环和甲氧基,满足条件的有四种,分别为:
,其同分异构体要求有四种氢原子,同时含有苯环和甲氧基,满足条件的有四种,分别为: 、
、 、
、 、
、![]() ,
,
故答案为: 、
、 、
、 、
、![]() ;
;
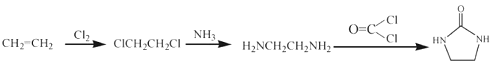
(7)乙烯和氯气加成生成ClCH2CH2Cl,ClCH2CH2Cl中的氯原子可以和氨气发生取代反应生成H2NCH2CH2NH2,H2NCH2CH2NH2与![]() 发生取代反应生成
发生取代反应生成 ,总的合成路线为:
,总的合成路线为: ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | 新制氯水滴入Na2S 溶液中 | 乙醇滴入K2Cr2O7酸性溶液中 | 饱和FeCl3溶液滴入沸水中 | 草酸滴入KMnO4 酸性溶液中 |
现象 | 产生黄色浑浊 | 溶液由橙色变为绿色 | 液体变为红褐色且澄清透明 | 产生无色气体,溶液紫红色褪去 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修3:物质结构与性质]铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业。其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
(1)基态K原子核外电子排布简写式为___________。 K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是_________,各元素的第一电离能由大到小的顺序为_________。
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为_______。KCN与盐酸作用可生成HCN,HCN的中心原子的杂化轨道类型为_________。
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于_____晶体。
(4)下图是金属单质常见的两种堆积方式的晶胞模型。

①铁采纳的是a堆积方式.铁原子的配位数为_____,该晶体中原子总体积占晶体体积的比值为____(用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为_____g·cm-3(用含有r、NA的最简代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置制备并检验Cl2的性质,下列说法正确的是( )


A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完
B.Ⅱ图中:充分光照后,量筒中剩余气体约为10mL(条件相同)
C.Ⅲ图中:生成蓝色的烟,若在集气瓶中加入少量水,所得溶液呈蓝绿色
D.Ⅳ图中:干燥的有色布条不褪色,湿润的有色布条能褪色,说明Cl2有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳循环”引起各国的高度重视,而如何降低大气中![]() 的含量及有效地开发利用
的含量及有效地开发利用![]() ,引起了全世界的普遍重视。将
,引起了全世界的普遍重视。将![]() 转化为甲醇:CO2(g)+3H2(g)
转化为甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),此研究对
CH3OH(g)+H2O(g),此研究对![]() 的深度开发应用和构建生态文明社会具有重要的意义。
的深度开发应用和构建生态文明社会具有重要的意义。
(1)在一恒温恒容密闭容器中充入1 mol ![]() 和3 mol
和3 mol ![]() 进行上述反应。测得
进行上述反应。测得![]() (g)和
(g)和![]() (g)浓度随时间变化如图所示。
(g)浓度随时间变化如图所示。

①0—10 min内,氢气的平均反应速率为____________,第10min后,保持温度不变,向该密闭容器中再充入2 mol![]() (g)和2mol
(g)和2mol ![]() (g),则平衡______________(填“正向”“逆向”或“不”)移动。
(g),则平衡______________(填“正向”“逆向”或“不”)移动。
②一定温度下,若此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是_______。
a.容器中压强不变 b.![]() 的体积分数不变 c.c(
的体积分数不变 c.c(![]() )=3c(
)=3c(![]() )
)
d.容器中密度不变 e.2个C=O断裂的同时有3个H-H断裂
(2)若已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) ![]()
2H2(g)+O2(g)=2H2O(g) ![]()
![]()
![]()
![]()
![]()
则表示![]() (l)燃烧热的热化学方程式为_______________________________。
(l)燃烧热的热化学方程式为_______________________________。
(3)如图,25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解600 mL 一定浓度的NaCl溶液。

①U形管内发生的化学反应方程式为__________________________________。
②在电解一段时间后,NaCl溶液的pH变为12(假设电解前后NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为____________mol。若向U形管内电解后的溶液中通入![]() 气体,使所得溶液c(
气体,使所得溶液c(![]() ):c(
):c(![]() )=2:1,则此时溶液中的c(
)=2:1,则此时溶液中的c(![]() )= ________________
)= ________________![]() 。(室温下,H2CO3的
。(室温下,H2CO3的![]() ;
;![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,A的简单离子焰色反应为黄色。B的最高价氧化物对应水化物B(OH)2 5.8 g恰好能与100 mL 2 mol·L-1盐酸完全反应;且B原子核中质子数和中子数相等。E2在黄绿色气体C2中燃烧产生苍白色火焰。D原子的最外层电子数是次外层电子数的3倍,F和D同主族。 根据上述条件回答:
(1)写出元素B的名称 ,元素C在元素周期表中的位置 。
(2)A、D形成淡黄色化合物,该物质中含有的化学键类型为 。
(3)C2与ADE溶液反应的离子方程式为 。
(4)用电子式表示BC2的形成过程 。
(5)由元素D和E构成的9e-微粒名称是 。
(6)比较元素C和F的气态氢化物的稳定性 > (用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:

实验室用干燥而纯浄的二氧化硫和氯气合成硫酰氯,反应的热化学方程式为:SO2(g)+Cl2(g)![]() SO2Cl2(l) △H=-97.3 kJ· mol-1
SO2Cl2(l) △H=-97.3 kJ· mol-1
反应装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器B的名称为________;
(2)仪器A的作用是_______;
(3)装置乙中盛放的试剂为______,在实验室用氢氧化钠溶液吸收多余硫酰氯的离子反应方程式为______;
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_______(填序号);
①先通冷凝水,再通气体 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①分解产物中分离出硫酰氯的实验操作名称为____。
②某同学为检验硫酰氯产品中是否混有硫酸设计实验如下:取少量产品溶于水,加入盐酸酸化的氯化钡溶液,振荡,观察到有白色沉淀生成,则认为产品中含有硫酸。该同学的结论是否正确,请说明理由____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种正投入生产的大型蓄电系统如图所示。放电前,被交换膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述不正确的是

A. 放电时,负极的电极反应式为2S22――2e-===S42-
B. 充电时,阳极的电极反应式为3Br--2e-===Br3-
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 充电时,M接电源负极,N接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠( Na2MoO4)可与重金属盐产生沉淀,是目前应用较多的一种新型水处理剂。利用精钼矿(主要成分是MoS2,含少量PbS等)来制取钼酸钠晶体的工艺流程如下图所示。

请回答下列问题:
(1)混合气A中含有一种大气污染物,其化学式为___________。
(2)焙烧的过程中采用如图1所示的“多层逆流焙烧”。

①多层逆流焙烧的优点是___________(任答两点)。
②依据如图2,写出第6~12层MoO2参加反应的化学方程式___________。
(3)写出碱浸时发生反应的离子方程式___________。
(4)PbS与H2O2反应时,温度高于40℃后,反应速率反而减慢,原因是___________。
(5)流程图中“除SO42-”的过程中,当 BaMoO4开始沉淀时,SO42-的去除率为97.0%,已知原 Na2MoO4溶液中c(MoO42-)=0.48mol/L, c(SO42-)=0.040mol/L, Ksp(BaSO4)=1.0×10-10, 则Ksp(BaMoO4)=___________。(过程中溶液体积变化忽略不计)
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2![]() Lix(MoS2)n,则电池放电时的正极反应式是___________。
Lix(MoS2)n,则电池放电时的正极反应式是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com