
科目: 来源: 题型:
【题目】常温下,向10 mL0.1mol/LHR溶液中逐滴滴入0.1mol/L的氨水,所得溶液pH 及导电能力与加入氨水体积的关系如图。下列说法不正确的是

A. 常温下,电离平衡常数 Ka(HR)≈Kb(NH3 H2O)
B. b点溶液pH=7,此时HR溶液与氨水恰好完全反应
C. c 点溶液中存在 c(NH4+ )>c(R- )>c(OH- )>c(H+)
D.a、b、c三点中,c点NH3 H2O的电离程度最大
查看答案和解析>>
科目: 来源: 题型:
【题目】Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙错误的是
A. 负极反应式为Mg-2e-=Mg2+
B. 正极反应式为Ag+e-=Ag
C. 电池放电时Cl-由正极向负极迁移
D. 电池放电时,外电路中,电子由负极向正极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. 凡是放热反应都是自发的,吸热反应都是非自发的
B. 自发反应一定是熵增大,非自发反应一定是熵减小或不变
C. 自发反应在恰当条件下才能实现
D. 自发反应在任何条件下都能实现
查看答案和解析>>
科目: 来源: 题型:
【题目】2g碳与水蒸气反应生成CO和H2,需吸收21.88kJ热量,此反应的热化学方程式为
A. C + H2O ==CO + H2ΔH =+131.3kJ·mol—1
B. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH =+10.94kJ·mol—1
C. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = -131.3kJ·mol—1
D. C(s)+ H2O(g) ==CO(g) + H2(g)ΔH = +131.3kJ·mol—1
查看答案和解析>>
科目: 来源: 题型:
【题目】体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量( )。
A. 相同 B. 中和HCl的多 C. 中和CH3COOH的多 D. 无法比较
查看答案和解析>>
科目: 来源: 题型:
【题目】已知K2Cr2O7溶液中存在平衡: Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。保持温度不变,用K2Cr2O7溶液进行下列实验:
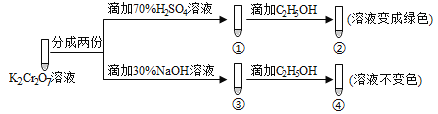
结合实验,下列说法正确的是
A. ①中溶液变黄,③中溶液橙色加深
B. 上述可逆反应的平衡常数:①<③
C. K2Cr2O7溶液的氧化性在酸性条件下更强
D. 若向④中加入70%H2S04溶液至过量,溶液变为橙色
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是_________,放电时发生_________(填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________(填“增大”、“减小”或“不变”),电解质溶液中阴离子移向_________(填“正”或“负”)极。
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______________________________________(用离子方程式表示)。
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为____________________。该电池工作时,外电路每流过1×103 mol e-,消耗标况下氧气_________m3。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D、E、F、G、H、I、J在周期表中的位置如下:

按要求回答下列问题。
(1)上表元素中,形成气态氢化物最稳定的是____元素(填元素符号)。
(2)32Ge与B同族,32Ge的最高价的氧化物与氢氧化钠反应的化学方程式为
_______________________________________________________________。
(3)等电子的D、F、G、H四种元素形成的离子,离子半径由大到小的顺序是(填离子符号)
_____> > > 。
(4)D、I元素形成的氢化物中,沸点较高的是_____________,理由__________________。
(5)34Se非金属性比D______(填“强”或“弱”),从原子结构的角度解释其原因为______________。
(6)用电子式表示E、G形成化合物的过程_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com