
科目: 来源: 题型:
【题目】短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍。m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物。下列说法正确的是

A. 原子半径Y<Z<W
B. 简单气态氢化物的稳定性Y>Z>W
C. 简单气态氢化物沸点Y>Z
D. X、Z、W三种元素可以形成离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,FeS和ZnS的饱和溶液中,金属阳离子与S2-的物质的量浓度的负对数关系如图所示。下列说法正确的是

A. 溶解度S(FeS)<S(ZnS)
B. a点表示FeS的不饱和溶液,且c(Fe2+)>c(S2-)
C. 向b点对应溶液中加入Na2S溶液,可转化为c点对应的溶液
D. 向c点对应的溶液中加入Na2S溶液,ZnS的KSP增大
查看答案和解析>>
科目: 来源: 题型:
【题目】以甲醛和苯酚为主要原料,经下图所示系列转化可合成酚醛树酯和重要有机合成中间体D(部分反应条件和产物略去):

已知:
(1)反应①的类型是_________;CH3OH的名称是____________。
(2)C中所含官能团的名称是________;物质 D的分子式是____________。
(3)反应②的方程式是________。
(4)下列关于A的性质,能反映支链对苯环结构产生影响的是_____________。
a.能与氢氧化钠溶液反应 b.能使酸性高锰酸钾溶液褪色 c.稀溶液中加浓溴水产生沉淀
(5)E(C8H10O2)与B的水解产物互为同分异构体,1molE可与2molNaOH反应,其核磁共振氢谱显示有3种峰且峰面积之比为3:1:1,符合条件的E共有_______种,写出其中一种的结构简式________。
(6)写出以CH3OH为原料(其他无机试剂任选)制备化合物CH3COCH2COOCH3的合成路线:![]() _____________。
_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰氯(ClNO)参与大气平流层和对流层的化学,气相的ClNO光解和水解都可产生Cl自由基。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及的化
学反应、对应的反应热和平衡常数如表:
化学反应 | 反应热 | 平衡常数 |
①2NO2(g)+NaC1(s) | △H1 | K1 |
②2NO(g)+C12(g) | △H2 | K2 |
③4NO2(g)+2NaC1(s) | △H3 | K3 |
则K1,K2,K3之间的关系为K2=______________,△H3=_____________
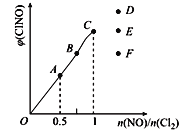
(2)已知2NO(g)+Cl2(g)![]() 2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
2ClNO(g),一定条件下在恒温恒容的密闭容器中按一定比例,充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图,则A、B、C三状态中,NO的转化率最大的是___点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____点。
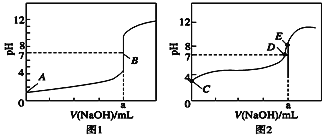
(3)常温下,用0.100 0 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 0 mol·L-1 HBr溶液和20.00 mL0.100 0 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示:
①根据图1和图2判断,滴定HBr溶液的曲线是______________(填“图1”或“图2”);
②a=______ mL; ③c(Na+)=c(CH3COO-)的点是______点;
④E点对应溶液中离子浓度由大到小的顺序为_______________。
(4) 氨气燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式_____________。
(5) 已知:CdCO3、NiCO3溶度积分别为6.0×10-12、1.0×10-7。p(CO32-)=-lg c(CO32-) 。在含Cd2+、Ni2+浓度均为0.01 mol/L的废水中滴加稀碳酸钠溶液。为了分离这两种阳离子,需要控制p(CO32-)范围为_____________(忽略溶液体积的变化)
A.4≤p(CO32-)≤6
B.5<p(CO32-)≤ 7-lg6
C.7-lg6<p(CO32-)≤ 8
D.7<p(CO32-)≤8
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧乙酸(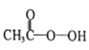 )是一种常见消毒剂,具强氧化性,减压蒸馏法制备过氧乙酸的步骤及装置如下:
)是一种常见消毒剂,具强氧化性,减压蒸馏法制备过氧乙酸的步骤及装置如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃一段时间。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。

不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),请回答相关问题:
反应物比例 CH3COOH/H2O2 | 反应时间(小时) | ||||
0.5 | 1 | 3 | 5 | 7 | |
2:1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
1:1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
1:2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
(1)C仪器中冷水流入口是_____(填a或b),生成过氧乙酸的化学方程式是__________。
(2)反应物最佳比例(CH3COOH/H2O2)是______,反应所需时间约________(选填1、3、5、7)小时。
(3)为更好控制反应温度,应增加的措施是________。
(4)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率。
可供选择的试剂和器材有:a.过氧乙酸溶液;b.1mol/L的FeCl3溶液;c.0.5mol/L的Fe2(SO4)3溶液;d. 0.5mol/L的CuCl2溶液;e.1mol/L的CuSO4溶液;f.计时器;g.测量气体体积的针筒。
你选择的试剂及器材是a、________、f、g(选填序号)实验方案是____________。
(5)产品含量测定。
取2.00mL过氧乙酸试样稀释成100mL,从中取出5.00mL,滴加酸性KMnO4溶液至恰好粉红色,以除去残余H2O2,加入10mL10%KI溶液和几滴淀粉溶液,摇匀,用0.1000mol/L的Na2S2O3标准液达到至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗13.20mL,Na2S2O3标准液。该样品中过氧乙酸的物质的量浓度是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以某种软锰矿(主要成分MnO2,同时含有FeCO3、Al2O3、SiO2等)为主要原料生产KMnO4的一种流程图如下:
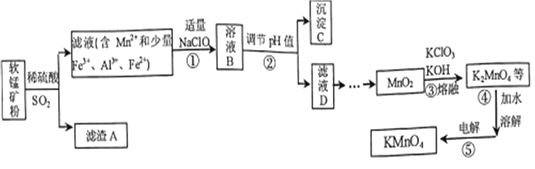
已知:Mn(OH)2极易被空气氧化;Fe(OH)3、Al(OH)3的溶度积常数依次为4.0×10-38、1.3×10-33。
(1)滤渣A的化学式是_________;溶液B中的主要阴离子有______________。
(2)为避免引入杂质,②步调节pH加入的物质是____________;调节pH除杂过程中,后析出的
沉淀是________________。
(3)浓硫酸与MnO2反应也能生成Mn2+,其化学方程式是___________________。
(4) K2MnO4在酸性、中性环境下都会歧化生成MnO4-和MnO2,则③步原料应保证_______________。
④步溶解水应煮沸的目的是_____________________。
(5)⑤步的阳极电极反应式是____________;该法电解时要产生污染,其原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:
①![]()
②![]()
③苯环上原有的取代基对新引入的取代基进入的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图:

(1)A转化为B的化学方程式是____________________;
C转化为D的化学方程式是___________________;
(2)图中“苯![]() ①
①![]() ②”省略了反应条件。根据图中已有的转化关系,请仔细观察苯环上原有取代基对新引入取代基进入的位置的影响,试写出①、②物质的结构简式:
②”省略了反应条件。根据图中已有的转化关系,请仔细观察苯环上原有取代基对新引入取代基进入的位置的影响,试写出①、②物质的结构简式:
①_______________,②_______________。
(3)在上述关系图中,共有_______步反应不属于取代反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究性学习小组为了模拟工业流程从浓缩的海水中提取液溴,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。设计了如下操作步骤及主要实验装置(夹持装置略去):
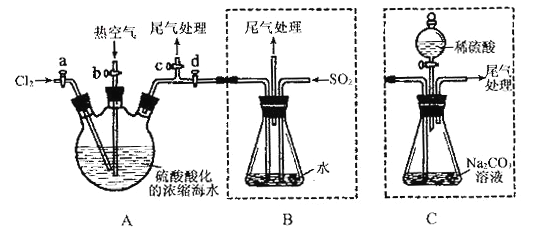
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入至反应结束;②关闭a、c,打开b、d,向A中鼓入足量热空气;③进行步骤②的同时,向B中通入足量SO2 ;④关闭b,打开a,再通过A向B中缓慢通入足量Cl2 ;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:(1)实验室中采用固液加热制备氯气的化学方程式为______________________;
(2)步骤②中鼓入热空气的作用为_________________________;
(3)步骤③B中发生的主要反应的离子方程式为_____________________。
(4)此实验中尾气可用______________(填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
(5)步骤⑤中,用下图所示装置进行蒸馏,收集液溴,将装置图中缺少的必要仪器补画出来。
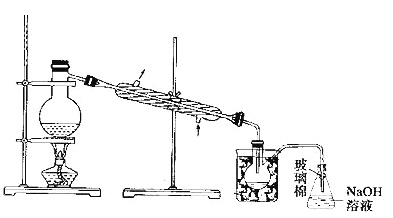
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBrO3等,请写出滴加稀硫酸时发生反应的离子方程式_________________。
(7)与B装置相比,采用C装置的优点为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】燃煤烟气中的SO2、NOx是形成酸雨的有害物质。应设法吸收利用。
I.吸收SO2:通入氨水将其转化为NH4HSO3,NH4HSO3溶液呈_____性(填“酸”、“碱”、“中”);再通空气将NH4HSO3氧化,溶液pH将__________(填“增大”、“减小”、“不变”)
Ⅱ.处理NO:先用O3处理,再用Na2SO3溶液吸收。O3处理的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=akJ·mol-1
NO2(g)=NO(g)+1/2O2(g) △H=bkJ·mol-1
(1)反应NO(g)+O3(g)=3NO2(g)的△H=_______kJ·mol-1。
(2)用Na2SO3溶液吸收时,溶液中SO32-将NO2转化为NO2-,反应的氧化产物是_________。
Ⅲ.利用SO2:分离出SO2可用于生产硫酸,反应之一:2SO2(g)+O2(g)![]() 2SO3(g) △H<0。
2SO3(g) △H<0。
(3)恒温恒容下,改变SO2、O2的物质的量之比[n(SO2)/n(O2)],平衡时测定Y的值,Y与[n(SO2)/n(O2)]的关系如图所示,则Y可能是______________。
A.正反应速率 B.SO3的体积分数 C.SO2的转化率 D.SO2的体积分数
a→b段y变化的原因是___________。

(4)Kp是以各气体平衡分压(各气体的分压=总压×各气体的体积分数)代替平衡浓度表示的平衡常数。
①Kp与温度(T/K)的关系是㏒Kp=![]() -4.86(R为常数),请判断R___0(填“>”或“<”),原因是________。
-4.86(R为常数),请判断R___0(填“>”或“<”),原因是________。
②在10.0%SO2、13.5%O2、76.5%N2(体积分数)时,SO2平衡转化率与温度、压强的关系如图。

则x_____1.0(填“>”或“<”);计算550℃、1.0atm下,2SO2(g)+O2(g)![]() 2SO3(g)的Kp=____。(精确到1位小数)
2SO3(g)的Kp=____。(精确到1位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com